Кто открыл закон Бойля-Мариотта?
Одним из ассистентов Р. Бойля был молодой физик Роберт Гук. Они посвятили свои исследования в основном газам и развитию корпускулярной теории. Узнав из научных публикаций о работах немецкого физика Отто Герике, Бойль решил повторить его эксперименты и для этой цели изобрел оригинальную конструкцию воздушного насоса. Первый образец этой машины был построен с помощью Гука.
В 1660 году в своем поместье Бойль завершил свою первую большую научную работу — «Новые физико-механические эксперименты относительно веса воздуха и его проявления».
Новым ассистентом у него в лаборатории Оксфорда становится молодой физик Ричард Таунли. Вместе с ним Бойль открыл один из фундаментальных физических законов, установив, что изменение объема газа обратно пропорционально изменению давления. Бойль впервые описал его в 1662 году («В защиту учения относительно эластичности и веса воздуха») и скромно назвал гипотезой.
Интересно, что выводы из исследований сделал не Бойль, а Таунли. Бойль указывает, что Ричард Таунли, читая первое издание его сочинения высказал гипотезу, что «давления и протяжения обратно пропорциональны друг другу».
Пятнадцать лет спустя после опубликования этих исследований Бойлем, т. е. в 1679 году, во Франции появилась «Речь о природе воздуха» аббата Эдма Мариотта, в которой наряду с другими вопросами описывались аналогичные экспериментам Бойля опыты по изучению зависимости между давлением воздуха и занимаемым объемом. Мариотт ни словом не упоминает о своем предшественнике, словно ему совершенно неизвестны работы Бойля по пневматике. Между тем работы Бойля были широко известны: они публиковались на латинском и английском языке. Впрочем, Мариотт не впервые забыл упомянуть своего предшественника, ведь точно так же в 1673 году в труде о соударениях он ни словом не сказал о работе Гюйгенса, позаимствовав у последнего не только методику эксперимента, но и основы теории.
|
|
|
Работа Мариотта значительно уступает работе Бойля в отношении тщательности эксперимента. Бойль измеряет высоты ртутного столба с точностью до шестнадцатых долей дюйма, сопоставляет реально наблюдаемые значения с вычислениями и указывает на неизбежную погрешность в измерениях. Мариотт измеряет высоты ртутного столба в целых дюймах и ограничивается сообщением, что опытные данные строго согласуются с расчетными. Осторожный и критически настроенный, Бойль называет открытый им закон только «гипотезой», требующей экспериментального подтверждения. Мариотт провозглашает его законом или правилом природы. Так что по справедливости «закон Бойля — Мариотта» должен именоваться «законом Бойля—Таунли» или «Бойля—Таунли—Гука».
|
|
|
В настоящее время в англичане этот закон называют законом Бойля, французы придерживаются противоположной точки зрения – это закон Марриота. А в тех странах, где не знают ни английского, ни французского языков этот закон называют законом Бойля-Мариотта.
Не будем воинствующими атеистами, несколько скептическое отношение к Эдму Мариотту вызвано не тем, что он аббат. Бойль также не был атеистом.
Яркой стороной жизни Бойля была религиозная и миссионерская деятельность. В юности пылкое воображение увлекало его в сторону крайних идей. Находясь под влиянием сильных впечатлений, он выражался следующим образом о своём настроении: «Демон воспользовался моей меланхолией, наполнил душу ужасом и внушил сомнения в основных истинах религии». В таком состоянии он додумался до самоубийства, от которого его удержала только мысль, что душа его попадёт в ад. Он решился рассеять свои сомнения чтением Библии в подлиннике и потому занялся изучением еврейского и греческого языков.
По завещанию (1661) Бойль оставил капитал для финансирования ежегодных чтений о Боге и религии, знаменитых «Лекций Бойля», первая из которых состоялась в 1692 г. Целью лекций Бойль определил защиту христианской религии от "печально известных неверных, а именно атеистов, деистов, язычников, иудеев и мусульман".
|
|
|
Сам Бойль написал о согласовании разума с религией, о натуралисте-христианине и т. п.
«Лекции Бойля» продолжались регулярно вплоть до 1905 г. С 2004 г. их возобновили в Лондоне, в церкви St. Mary Le Bow. Они проходят ежегодно, в феврале.
Воздадим должное и французскому монаху – у него также есть неоспоримые заслуги (хотя бы в том, что он познакомил с законом Бойля французов).
 Эдм Мариотт (фр. Edme Mariotte) — аббат, французский физик XVII века, родился в Бургундии в 1620 году.
Эдм Мариотт (фр. Edme Mariotte) — аббат, французский физик XVII века, родился в Бургундии в 1620 году.
Проживал вблизи Дижона и был приором в городке St. Martin sous Beaune. Mариотт был один из основателей (1666) и первых членов Академии наук, основанной в Париже. Умер в Париже в 1684 г.
Важнейшие работы Мариотта собраны в его «Essais de Physique» (4 выпуска, 1676—1681); из них наиболее известен второй выпуск: «De la rature de l’aire» (1679), содержащий изложение известной зависимости между упругостью газа и его объёмом; тот же закон найден был на 17 лет раньше Бойлем и называется обыкновенно «законом Бойля-Мариотта».
Другие «Essais» касаются вопросов природы и движения жидкостей, падения тел и т. д.; четвёртый представляет любопытную монографию о цветах и красках с физической и физиологической стороны вопроса; среди множества интересных наблюдений Мариотта следует отметить открытие им слепого пятна в глазу.
|
|
|
У каждого есть в слепое пятно, может именно оно мешает иногда видеть библейское «бревно в своем глазу» и не мешает «увидеть соринку в чужом глазу».
Слепое пятно.

Слепо́е пятно́ (оптический диск) — имеющаяся в каждом глазу здорового человека область на сетчатке, которая не чувствительна к свету. В этой области из глаза выходит зрительный нерв. Слепые пятна в двух глазах находятся в разных местах (симметрично), поэтому при нормальном использовании обоих глаз они незаметны.
Чтобы наблюдать у себя слепое пятно, закройте правый глаз и левым глазом посмотрите на правый крестик, который обведён кружочком. Держите лицо и страницу горизонтально. Не сводя взгляда с правого крестика, приближайте (или отдаляйте) лицо от монитора и одновременно следите за левым крестиком (не переводя на него взгляд). В определённый момент он исчезнет.
Слепое пятно открыл Эдм Мариотт в 1668 году. Говорят, король Франции Людовик XIV развлекался со слепым пятном, наблюдая своих подданных, как будто у них не было голов.
Если вам удался этот эксперимент, то задумайтесь, все ли вы видите вокруг себя. Если вам этот эксперимент не удался, то задумайтесь, если у вас зрительный нерв, и то с чем он соединен.
Подведем предварительный итог: в 1662 году окончательно появилась левая часть уравнения (1) – произведение давления на объем есть величина постоянная
 . (2)
. (2)
Но чему равна эта константа, или хотя бы от чего она зависит? Сейчас ответить на этот вопрос легко – от температуры, массы газа и его состава.
Критиковать легко…
 С позиций современной науки легко критиковать ученых прошлых веков. Досталось и английскому ученому Роберту Бойлю. Возможно, авторов до сих пор обижает название одной из его книг книга «Химик — скептик» (1662), в которой автор Бойль камня на камне не оставил от учения Аристотеля о четырех элементах, существовавшего без малого две тысячи лет, декартова «эфира» и трех алхимических начал. Естественно, этот труд вызвал резкие нападки со стороны последователей Аристотеля и картезианцев. Однако Бойль опирался в нем на опыт, и потому доказательства его были неоспоримы. Большая часть ученых — последователи корпускулярной теории — с восторгом восприняли идеи Бойля. Многие из его идейных противников тоже вынуждены были признать открытия ученого.
С позиций современной науки легко критиковать ученых прошлых веков. Досталось и английскому ученому Роберту Бойлю. Возможно, авторов до сих пор обижает название одной из его книг книга «Химик — скептик» (1662), в которой автор Бойль камня на камне не оставил от учения Аристотеля о четырех элементах, существовавшего без малого две тысячи лет, декартова «эфира» и трех алхимических начал. Естественно, этот труд вызвал резкие нападки со стороны последователей Аристотеля и картезианцев. Однако Бойль опирался в нем на опыт, и потому доказательства его были неоспоримы. Большая часть ученых — последователи корпускулярной теории — с восторгом восприняли идеи Бойля. Многие из его идейных противников тоже вынуждены были признать открытия ученого.
А что же современные критики? Несколько примеров на заданную тему.
…В изучении природы он был последователем Бэкона, противником схоластической философии и давал предпочтение опыту перед умозрением; иногда это направление мешало ему делать обобщения смысла замеченных им явлений.
…Весьма важный физический закон сжатия газов, который носит теперь его имя, остался бы, может быть, незамеченным Бойлем, если б не первоначальное указание его ученика Ричарда Таунли на правильность сжатия газов с увеличением давления …
…Бойль показал, что тёплая вода закипает при разрежении окружающего её воздуха, но не обобщил значения этого важного опыта, то есть не показал, что температура кипения воды вообще зависит от давления воздуха и паров воды на её поверхности.
… После появления сочинения Герике, в котором описаны его опыты над электричеством и магнетизмом, Бойль занялся воспроизведением этих опытов и внёс в них, как всегда, нечто новое; однако он иногда ошибался, как, например, в том случае, когда полагал, что железо отпадает от магнита под колоколом воздушного насоса вследствие разрежения воздуха.
…Бойль принимает, подобно своим предшественникам, существование в природе абсолютно пустого пространства, в котором находятся материальные частицы определённой величины и формы; атомы жидкостей находятся в постоянном движении, а твёрдых тел — в покое, промежутки же между частицами наполнены некоторым очень тонким веществом. Для объяснения сцепления твёрдых тел он ошибочно принимает давление на них воздуха — общераспространённое тогда мнение.
…Хотя он и показал, что воздух изменяется от горения в нём тел, и что некоторые металлы увеличиваются в весе при накаливании, и что действием уксуса на мел или соляной кислотой на железо получаются газы, но не извлёк из своих работ никаких теоретических заключений.
Понадобилось более ста лет, чтобы «появился» следующий газовый закон. В Европе гремели войны; Русь стала Российской империей, вышла к Балтийскому, а затем и к Черному морям, не смотря на многочисленные дворцовые перевороты; провозглашена независимость Соединенных Штатов Америки; описаны путешествия Лемюэля Гулливера и мир потешается то ли над неудачливым врачом, то ли над могучей Англией.
А что же физики – исследователи свойств газов? Ученый мир пытается осмыслить понятия теплоты и температуры, пусть даже в рамках «традиционных» представлений: теплота – количество теплорода в теле, а температура высота уровня этого теплорода. Главное же - пытаются научиться измерять температуру. Заметим, что первый прибор для наблюдения степени нагретости сконструировал и изготовил еще Г. Галилей. Назывался этот прибор «термоскоп». В чем он отличался от термометра? Тем же, чем всякий
«-скоп» отличается от своего «-метра» Например, электроскоп от электрометра, спектроскоп от спектрометра, микроскоп от микрометра (кажется, этот пример не слишком удачен, лучше телескоп от … тоже неудача) – первые позволяют только наблюдать, а вторые – измерять.
Не следует также думать, что никто не видел влияния степени нагретости на упругость воздуха. Сам Бойль описывал свои наблюдения (но не измерения): «Когда воздух был сжат настолько, что он был сгущен в объеме, составлявшем одну четверть первоначального, мы попробовали, насколько холод от льняной ткани, смоченной водой, сгустит воздух. И порой казалось, что воздух несколько сжимается, однако не настолько, чтобы на этом можно было строить какие-то заключения. Затем мы также попробовали, будет ли жар... расширять воздух; при приближении пламени свечи к той части, где был заключен воздух, обнаружилось, что теплота оказывает более заметное действие, нежели ранее действовавший холод».
А пока практически весь XVIII век, век Просвещения ученые пытаются просветить себя в термометрии. Первая успешная попытка осуществлена немецким (или голландским) изобретателем, стеклодувом и ученым Даниэлем Фаренгейтом.
 ФАРЕНГЕЙТ, ДАНИЭЛЬ ГАБРИЭЛЬ (нем. Fahrenheit, Daniel Gabriel) , немецкий физик. Родился 24 мая 1686 в Данциге (ныне Гданьск, Польша). Изучал физику в Германии, Голландии и Англии. Почти всю жизнь прожил в Голландии, где занимался изготовлением точных метеорологических приборов. В 1709 изготовил спиртовой, в 1714 – ртутный термометр, использовав новый способ очистки ртути. Для ртутного термометра Фаренгейт построил шкалу, имеющую три реперные точки: 0° соответствовал температуре смеси вода – лед – нашатырный спирт, 96° – температуре тела здорового человека, а в качестве контрольной температуры было принято значение 32° для точки таяния льда. Температура кипения чистой воды по шкале Фаренгейта составила 212°. Шкала Фаренгейта применяется во многих англоязычных странах, хотя постепенно уступает место шкале Цельсия. Помимо изготовления термометров, Фаренгейт занимался усовершенствованием барометров и гигрометров. Исследовал также зависимость изменения температуры кипения жидкости от атмосферного давления и содержания в ней солей, обнаружил явление переохлаждения воды, составил таблицы удельных весов тел. Умер Фаренгейт в Гааге 16 сентября 1736.
ФАРЕНГЕЙТ, ДАНИЭЛЬ ГАБРИЭЛЬ (нем. Fahrenheit, Daniel Gabriel) , немецкий физик. Родился 24 мая 1686 в Данциге (ныне Гданьск, Польша). Изучал физику в Германии, Голландии и Англии. Почти всю жизнь прожил в Голландии, где занимался изготовлением точных метеорологических приборов. В 1709 изготовил спиртовой, в 1714 – ртутный термометр, использовав новый способ очистки ртути. Для ртутного термометра Фаренгейт построил шкалу, имеющую три реперные точки: 0° соответствовал температуре смеси вода – лед – нашатырный спирт, 96° – температуре тела здорового человека, а в качестве контрольной температуры было принято значение 32° для точки таяния льда. Температура кипения чистой воды по шкале Фаренгейта составила 212°. Шкала Фаренгейта применяется во многих англоязычных странах, хотя постепенно уступает место шкале Цельсия. Помимо изготовления термометров, Фаренгейт занимался усовершенствованием барометров и гигрометров. Исследовал также зависимость изменения температуры кипения жидкости от атмосферного давления и содержания в ней солей, обнаружил явление переохлаждения воды, составил таблицы удельных весов тел. Умер Фаренгейт в Гааге 16 сентября 1736.
Непривычная для нас шкала, но ею до сих пор пользуются, например, в США.
О роли простудных заболеваний…
Нам, считающим «очевидной» шкалу Цельсия, кажется странным выбор Фаренгейта. Действительно, почему лед плавится при температуре  , а вода кипит при температуре
, а вода кипит при температуре  ? Для тех, кто с детства привык к шкале Фаренгейта, температура человеческого тела в
? Для тех, кто с детства привык к шкале Фаренгейта, температура человеческого тела в  кажется нормальной только в морге.
кажется нормальной только в морге.
Существует несколько легенд о выборе реперных точек температурной шкалы Фаренгейта. Так диапазон в  между температурами плавления льда и кипения воды напоминает о величине развернутого угла (в угловых градусах, конечно, а не в радианах). Бытует расхожее мнение, что Фаренгейт изначально выбрал температуру в
между температурами плавления льда и кипения воды напоминает о величине развернутого угла (в угловых градусах, конечно, а не в радианах). Бытует расхожее мнение, что Фаренгейт изначально выбрал температуру в 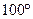 как нормальную температуру человеческого тела, но ему попался человек, которого слегка лихорадило. Так сочетание равенства температурного и углового градуса и неудача с выбором «эталонного» человека привело к шкале Фаренгейта.
как нормальную температуру человеческого тела, но ему попался человек, которого слегка лихорадило. Так сочетание равенства температурного и углового градуса и неудача с выбором «эталонного» человека привело к шкале Фаренгейта.
Однако, в действительности эти истории далеки от правды. Выбор Фаренгейта был логичным и строго обоснованным. В результате тщательных измерений теплового расширения хорошо очищенной ртути Фаренгейт установил, что в диапазоне температур от плавления льда до кипения воды ртуть расширяется на 180 миллионных своего объема. Поэтому выбор числа 180 для величины этого диапазона более обоснован, чем число пальцев на двадцати руках. Так может, и углы стоит измерять в градусах Цельсия?
В качестве нуля Фаренгейтом была выбрана температура смеси вода – лед – нашатырный спирт также далеко не случайно, это была минимальная температура, которую удавалось устойчиво воспроизводить в лаборатории, «абсолютный нуль» начала XVIII века.
 Не всем понравилась шкала Фаренгейта, стали появляться и другие температурные шкалы. Возможно, сыграла свою роль и чувство национальной гордости, почему в Германии есть своя шкала, а у нас нет! Если каждое государство чеканит свою монету, то почему нельзя использовать свои градусы? Вот и появились: во Франции шкала Реомюра, в России – шкала Делиля (ей пользовался Ломоносов)… Но все-таки на первое место вышли шведы, наиболее популярной до настоящего времени остается шкала Цельсия.
Не всем понравилась шкала Фаренгейта, стали появляться и другие температурные шкалы. Возможно, сыграла свою роль и чувство национальной гордости, почему в Германии есть своя шкала, а у нас нет! Если каждое государство чеканит свою монету, то почему нельзя использовать свои градусы? Вот и появились: во Франции шкала Реомюра, в России – шкала Делиля (ей пользовался Ломоносов)… Но все-таки на первое место вышли шведы, наиболее популярной до настоящего времени остается шкала Цельсия.
 Цельсий, Андерс
Цельсий, Андерс
Андерс Цельсий (швед. Anders Celsius)— шведский астроном, геолог и метеоролог (в те времена геология и метеорология считались частью астрономии). Профессор астрономии Упсальского университета (1730—1744). Предложил шкалу Цельсия, в которой температура тройной точки воды (эта температура практически совпадает с температурой плавления льда при нормальном давлении) принималась за 100, а температура кипения воды — за 0. Как видно, Цельсий предложил измерять «градусы холода»
После смерти Цельсия году шкала была перевернута (за 0 стали принимать температуру плавления льда, а за 100 - кипения воды), и в таком виде используется до нашего времени. Возможно, в этом участвовал Карл Линней (он преподавал медицину и естествознание в том же Упсальском университете, где Цельсий - астрономию),
Вместе с французским астрономом Пьером Луи Моро де Мопертюи участвовал в экспедиции с целью измерения отрезка меридиана в 1 градус в Лапландии (тогда — часть Швеции). Аналогичная экспедиция была организована на экватор, на территории нынешнего Эквадора. Сравнение результатов подтвердило предположение Ньютона, что Земля представляет собой эллипсоид, сплюснутый у полюсов.
Наблюдал Северное сияние и описал более 300 своих и чужих наблюдений. Обнаружил, что отклонения стрелки компаса коррелируют с интенсивностью сияния. На этом основании сделал правильное заключение, что природа Северного сияния связана с магнетизмом.
Весьма точно измерил яркость 300 звёзд, используя систему одинаковых стеклянных пластин, поглощавших свет.
Отец Андерса Цельсия, Нильс, и оба деда, Магнус Цельсий и Андерс Споул, тоже были профессорами. Учёными были и многие другие родственники Андерса Цельсия.
Умер в 1744 году от туберкулёза.
 К концу века Просвещения температура стала знакомой, привычной и легко измеряемой физической величиной. Накануне Великой французской революции в небо взмывают воздушные шары-монгольфьеры, они становятся популярными, почти все наши следующие герои покоряют воздушный океан, о чем мы будем обязаны рассказать далее. Но одним из пионеров воздухоплавания стал Жак Шарль, чье имя украсило следующий по времени открытия газовый закон.
К концу века Просвещения температура стала знакомой, привычной и легко измеряемой физической величиной. Накануне Великой французской революции в небо взмывают воздушные шары-монгольфьеры, они становятся популярными, почти все наши следующие герои покоряют воздушный океан, о чем мы будем обязаны рассказать далее. Но одним из пионеров воздухоплавания стал Жак Шарль, чье имя украсило следующий по времени открытия газовый закон.
 Жак Александр Сезар ШАРЛЬ
Жак Александр Сезар ШАРЛЬ
Жак Александр Сезар ШАРЛЬ
(Jacques Alexandre César Charles), французский физик, химик, инженер и воздухоплаватель родился в Божанси (Beaugency) в 1746. В молодости служил чиновником в Министерстве финансов в Париже. Заинтересовавшись воздухоплаванием, разработал монгольфьеры современной конструкции, подъемная сила которых обусловлена расширением нагретого горелкой воздуха внутри шара. Он же одним из первых стал наполнять воздушные шары водородом (который во много раз легче воздуха и обеспечивает значительно большую подъемную силу, нежели горячий воздух), установив благодаря этому рекорды высоты подъема (более 3 000 м) и дальности полета (43 км). Один из пионеров воздухоплавания Жак Александр Сезар Шарль пришел в науку в результате своего увлечения строительством монгольфьеров — больших воздушных шаров, заполненных разогретым воздухом, — которые тогда только-только появились. Конструкция современных воздушных шаров с использованием открытой газовой горелки, разработанная Шарлем более двух столетий назад, не претерпела принципиальных изменений и используется до наших дней. Нет ничего удивительного в том, что научные интересы Шарля лежали в области исследования свойств газов. Закон, носящий его имя, Шарль сформулировал в 1787 году после ряда опытов с кислородом, азотом, водородом и углекислым газом.
Умер в 1823 году.
 Монгольфьер, или шарльер?
Монгольфьер, или шарльер?
Полет воздушного шара братьев Монгольфье вызвал большой интерес в Париже. Академия наук пригласила их повторить свой опыт в столице. В то же время молодому французскому физику профессору Жаку Шарлю было предписано подготовить и провести демонстрацию своего летательного аппарата. Шарль был уверен, что Монгольфьеров газ, как называли тогда дымный воздух, — это не лучшее средство для создания аэростатической подъемной силы. Он был хорошо знаком с последними открытиями в области химии и считал, что гораздо большие выгоды сулит использование водорода, так как он легче воздуха. Но избрав водород для наполнения оболочки летательного аппарата, Шарль оказался перед рядом технических проблем. В первую очередь, из чего изготовить легкую оболочку, способную длительное время держать летучий газ? Справиться с этой проблемой ему помогли механики братья Робер. Они изготовили материал необходимых качеств, использовав легкую шелковую ткань, покрытую раствором каучука в скипидаре.
27 августа 1783 года на Марсовом поле в Париже стартовал летательный аппарат Шарля. На глазах 300 тысяч зрителей он устремился ввысь и вскоре стал невидимым. Когда кто-то из присутствовавших воскликнул: «Какой же во всем этом смысл?!» — известный американский ученый и государственный деятель Бенджамин Франклин, находившийся среди зрителей, заметил: «А какой смысл в появлении на свет новорожденного?» Замечание оказалось пророческим. На свет появился «новорожденный», которому было предопределено великое будущее.
Успешный полет аэростата Шарля не остановил братьев Монгольфье в их намерении воспользоваться предложением Академии наук и продемонстрировать в Париже аэростат собственной конструкции. Стремясь произвести наибольшее впечатление, Этьенн использовал весь свой талант, недаром он считался также отличным архитектором. Построенный им воздушный шар был в определенном смысле произведением искусства. Его оболочка высотой более 20 метров имела необычную бочкообразную форму и была разукрашена снаружи вензелями и красочными орнаментами. Продемонстрированный официальным представителям Академии наук воздушный шар вызвал у них такое восхищение, что было решено повторить показ в присутствии королевского двора.
Демонстрация состоялась в Версале (под Парижем) 19 сентября 1783 года. Правда, воздушный шар, вызвавший восхищение французских академиков, не дожил до этого дня: его оболочку размыло дождем, и он пришел в негодность. Однако это не остановило братьев Монгольфье. Работая день и ночь, они построили к намеченному сроку шар, который по своей красоте не уступал предыдущему. Чтобы произвести еще больший эффект, братья прицепили к воздушному шару клетку, куда посадили барана, утку и петуха. Это были первые пассажиры в истории воздухоплавания.
Воздушный шар оторвался от помоста и устремился ввысь, а через восемь минут, проделав путь в четыре километра, благополучно опустился на землю. Братья Монгольфье сделались героями дня, были удостоены наград, а все воздушные шары, в которых для создания подъемной силы использовался дымный воздух, стали с того дня именоваться монгольфьерами.
Каждый полет воздушных шаров братьев Монгольфье приближал их к заветной цели — полёту человека. Построенный ими новый шар был крупнее: высота 22,7 метра, диаметр 15 метров. В нижней его части крепилась кольцевая галерея, рассчитанная на двух человек. В середине галереи был подвешен очаг для сжигания крошеной соломы. Находясь под отверстием в оболочке, он излучал тепло, подогревавшее воздух внутри оболочки во время полета. Это позволяло сделать полет более длительным и в какой-то мере управляемым.
Король Франции Луи XVI запретил авторам проекта принимать личное участие в полете. Столь рискованную для жизни задачу, по его мнению, следовало поручить двум преступникам, приговоренным к смертной казни. Но это вызвало бурные протесты Пилатра де Розье, активного участника постройки монгольфьера. Он не мог смириться с мыслью о том, что в историю воздухоплавания войдут имена каких-то преступников, и настаивал на личном участии в полете. Разрешение было получено. Другим «пилотом» стал поклонник воздухоплавания маркиз д'Ар-ланд. И вот 21 ноября 1783 года человек наконец-то смог оторваться от земли и совершить воздушный полет. Монгольфьер придержался в воздухе 25 минут, пролетев около девяти километров.
Стремясь доказать, что будущее воздухоплавания принадлежит шарльерам (так называли аэростаты с оболочками, наполненными водородом), а не монгольфьерам, профессор Шарль понимал, что для этого нужно осуществить полет людей на шарльере, причем более эффектный, чем полет братьев Монгольфье. Построенный им шарльер имел сетку, обтягивавшую верхнюю полусферу оболочки аэростата, и стропы, с помощью которых к этой сетке подвешивалась гондола для людей. В оболочке была сделана специальная отдушина для выхода водорода при падении наружного давления. Для управления высотой полета использовались специальный клапан в оболочке и балласт, хранящийся в гондоле. Был предусмотрен и якорь для облегчения посадки на землю.
1 декабря 1783 года шарльер диаметром более девяти метров взял старт в парке Тюильри. На нем отправились профессор Шарль и один из братьев Робер, принимавших активное участие в работах по постройке шарльеров. Пролетев 40 километров, они благополучно опустились возле небольшой деревеньки. Затем Шарль в одиночку продолжил путешествие. Шарльер пролетел пять километров, забравшись на небывалую для того времени высоту — - 2750 метров. Пробыв в заоблачной вышине около получаса, исследователь благополучно приземлился, завершив, таким образом, первый в истории воздухоплавания полет на аэростате с оболочкой, наполненной водородом.
Наступает новый XIX век. Очередная Великая революция, на этот раз французская завершается, уничтожив французский абсолютизм. По традиции, казнены, уже цивилизованно, с помощью новейшего изобретения – гильотины: король, королева, тысячи аристократов, выдающейся химик Лавуазье, изобретатель Гильотен (который в прямом смысле испытал свое изобретение на собственной шее). В конце – концов, революция, как Сатурн, пожирает и собственных детей во главе с «неподкупным» Робеспьером. К власти приходит генерал Буонапарте, ставший вскорости, нет, не королем, а просто императором.
Но наука подобно библейскому блудному сыну (уже изображенному Рембрандтом) с триумфом возвращается во Францию, чему в немалой степени способствует сам император, покровительствуя ученым. В друзьях у Наполеона – знаменитый Алесандро Вольта и не менее знаменитый Пьер Лаплас. Последний преподносит императору свою трехтомную «Небесную механику» и на вопрос «Где в вашей теории место бога?» скромно отвечает: «Я не нуждался в этой гипотезе!». Лучше всего отношение Наполеона к ученым характеризует его знаменитая команда времен египетского похода, когда он был еще Первым консулом: «Ослов и математиков в середину колоны!» Что может быть важнее для армии, чем транспорт и наука!
Появляется метрическая система мер, Французская академия наук по праву именуется академией Великих. Среди них достойное место занимает автор очередного газового закона Жозеф Луи Гей-Люссак.
 Жозеф Луи Гей-Люссак
Жозеф Луи Гей-Люссак
Ф ранцузский физик и химик Жозеф Луи Гей-Люссак (фр. Joseph Louis Gay-Lussac) родился в Сен-Леонар-де-Нобла (департамент Верхняя Вьенна). Получив в детстве строгое католическое воспитание, в 15 лет он переехал в Париж; там, в пансионе, юноша продемонстрировал незаурядные математические способности. В 1797 – 1800 гг. Гей-Люссак учился в Политехнической школе в Париже, где химию преподавал Клод Луи Бертолле. После окончания школы Гей-Люссак был ассистентом Бертолле. В 1809 г. он почти одновременно стал профессором химии в Политехнической школе и профессором физики в Сорбонне, а с 1832 г. – ещё и профессором химии Парижского ботанического сада.
Научные работы Гей-Люссака относятся к самым разным областям химии. В 1802 г. независимо от Джона Дальтона Гей-Люссак открыл один из газовых законов – закон теплового расширения газов, позже названный его именем. В 1804 г. он совершил два полёта на воздушном шаре (поднявшись на высоту 4 и 7 км), во время которых выполнил ряд научных исследований, в частности измерил температуру и влажность воздуха, а также характеристики магнитного поля Земли[4]. В 1805 г. совместно с Гумбольдтом установил состав воды. В 1808 г. Гей-Люссак открыл закон объёмных отношений: «При взаимодействии газов их объёмы и объёмы газообразных продуктов соотносятся как простые числа». В 1809 г. он провел серию опытов с хлором, подтвердивших, что хлор – это элемент, а не кислородсодержащее соединение, а в 1810 г. установил элементарный характер калия и натрия, затем фосфора и серы.
Гей-Люссак выдвинул и обосновал концепцию водородных кислот, опровергающей чисто кислородную теорию Лавуазье.
Гей-Люссак работал во многих государственных комиссиях и составлял по поручению правительства доклады с рекомендациями по внедрению научных достижений в промышленность. В 1831-1839 гг. член палаты депутатов, где выступал только по научным и техническим вопросам. Прикладное значение имели и многие его исследования. Так, его метод определения содержания этилового спирта был положен в основу практических способов определения крепости алкогольных напитков. Гей-Люссак разработал в 1828 г. методику определения кислот и щелочей, а 1830 г. – объёмный способ определения серебра в сплавах, применяющийся и в настоящее время. Созданная им конструкция башни нашла применение в производстве серной кислоты. В 1825 г. Гей-Люссак получил патент на производство стеариновых свечей.
В 1806 г. Гей-Люссак был избран членом Французской академии наук и её президентом в 1822 и 1834 гг. Иностранный почётный член Петербургской АН (1826).
В 1839 г. он получил титул пэра Франции.
Умер 9 мая 1850 года в Париже.
Гей-Люссак в своей лаборатории проводит множество экспериментов с различными газами, тщательно исследует влияние температуры на их характеристики (давление и объем), переоткрывает закон Шарля и открывает закон Гей-Люссака (опередив буквально на несколько месяцев англичанина Дальтона, который в отместку долго критиковал француза за его закон кратных объемных отношений). Не случайно, зависимости давления и объема от температуры часто называют первым и вторым законом Гей-Люссака (такого названия законов придерживается, например, «Физическая энциклопедия»). Эти работы требуют полной самоотдачи, вплоть до потери глаза, что не мешает продолжать исследования.
Глаз-алмаз
Гей-Люссак во время одного из своих опытов лишился глаза. Епископ Сиезский недоумевал по этому поводу:
- Не понимаю, как можно быть ученым, имея всего один глаз? Что можно увидеть одним глазом?
- Да побольше вашего,- ухмыльнулся Гей-Люссак.- Вот, например, я вижу у вас два глаза, а вы у меня - только один.
Что же открыл пэр Франции и депутат Жозеф Луи Гей-Люссак. Почти очевидные закономерности: как давление (при постоянном объеме), так и объем (при постоянном давлении) газа линейно возрастают с ростом температуры. В современных обозначениях эти зависимости записываются в виде
 . (3)
. (3)
Здесь  и
и  давление и объем газа при температуре
давление и объем газа при температуре  .
.
Что в этом удивительного? Так же ведут себя и жидкости (это свойство жидкостей проверено и использовано Фаренгейтом, Реомюром … при создании термометров), и твердые тела. Удивительно и поразительно другое - коэффициенты  (называемые термический коэффициент давления в первом случае, и термический коэффициент объемного расширения – во втором) одинаковы, более того они одинаковы для всех исследованных газов! Газы различаются по составу, атомной массе, цвету, запаху … но эти коэффициенты одинаковы! Если бы так же вели себя и жидкости, то не возникло бы спора между Фаренгейтом и Реомюром. Теперь появилась возможность создать шкалу, не зависящую от рода термометрического вещества, только бы оно находилось в газообразном состоянии. Кстати, такая температурная шкала была разработана, и получила название газовой. До сих пор газовые термометры одни из самых точных и чувствительных.
(называемые термический коэффициент давления в первом случае, и термический коэффициент объемного расширения – во втором) одинаковы, более того они одинаковы для всех исследованных газов! Газы различаются по составу, атомной массе, цвету, запаху … но эти коэффициенты одинаковы! Если бы так же вели себя и жидкости, то не возникло бы спора между Фаренгейтом и Реомюром. Теперь появилась возможность создать шкалу, не зависящую от рода термометрического вещества, только бы оно находилось в газообразном состоянии. Кстати, такая температурная шкала была разработана, и получила название газовой. До сих пор газовые термометры одни из самых точных и чувствительных.
От законов Гей-Люссака совсем не далеко до абсолютной температурной шкалы. Действительно, измеренное значение коэффициента  . Поэтому можно преобразовать, например, для объема:
. Поэтому можно преобразовать, например, для объема:
 .
.
Теперь достаточно сместить нуль температуры, тем самым ввести новую температурную шкалу, связанную со шкалой Цельсия соотношением  , и получить не просто линейную зависимость, а еще более простую прямо пропорциональную зависимость между давлением, объемом и температурой. Эта новая шкала появилась, но только через 46 лет и получила название абсолютная температурная шкала, или шкала Кельвина, но об этом речь еще впереди. В законах Гей-Люссака неявно присутствует и абсолютный нуль температуры (настоящий), так как при температурах меньших
, и получить не просто линейную зависимость, а еще более простую прямо пропорциональную зависимость между давлением, объемом и температурой. Эта новая шкала появилась, но только через 46 лет и получила название абсолютная температурная шкала, или шкала Кельвина, но об этом речь еще впереди. В законах Гей-Люссака неявно присутствует и абсолютный нуль температуры (настоящий), так как при температурах меньших  не только давление (с чем еще можно смириться), но и объем (чего даже представить не возможно) становятся отрицательными.
не только давление (с чем еще можно смириться), но и объем (чего даже представить не возможно) становятся отрицательными.
Постоянство указанных коэффициентов позволяет очевидным образом объединить три газовых закона
 . (4)
. (4)
Что было сделано всего через 30 лет Клапейроном (об этом тоже впереди) – странно, что этого не сделал Гей-Люссак, но не появилось еще обобщающей идеи уравнения состояния.
Таким образом, к 1802 году уравнение (1) обрело еще один множитель, но самого уравнения еще не было – история сделала «зигзаг» и обратилась к поиску неизвестного коэффициента  в уравнении (4)
в уравнении (4)
Первое десятилетие XIX века оказалось богатым на новые газовые законы, открытые не только во Франции. Видно влияние Наполеона было сильным и в Италии, покоренной Наполеоном, и в Англии, которая в конце-концов победила его.
Бросим же беглый взгляд на эти страны. В Англии развивал атомистическое учение Джон Дальтон, обиженный Гей-Люссаком и вынужденным открывать свой собственный закон (без соавторов).
 Джон Дальтон
Джон Дальтон
Джон Дальтон (англ.John Dalton) английский химик и физик родился 6 сентября 1766 года в семье ткача. В школе проявил незаурядные способности к математике и физике. Так как семья бедствовала, продолжить учебу не удалось. Тогда двенадцатилетнему Джону предложили заменить уехавшего учителя, он согласился. По заданию одного популярного издания начал с 1787 года вести дневник метеонаблюдений. Изучение погоды стало его основным занятием, причем от простых наблюдений он перешел к анализу состава и свойств атмосферы. В 1793 году был приглашен в Манчестер преподавателем физики и математики в колледже.
В 1794 году сделал доклад о частичной световой слепоте, дефекте зрения, который в последствии был назван «дальтонизмом».
Исследуя свойства газовых смесей, в 1801 году открыл закон парциальных давлений (закон Дальтона), а в 1802 году – газовый закон, устанавливающий зависимость объема газа от его температуры (чуть ранее этот же закон был открыт Гей-Люссаком и сейчас носит его имя). В 1803 году открыл закон зависимости растворимости газов от их парциального давления (позже этот закон в более общей форме был сформулирован Генри, поэтому носит его имя).
Занимаясь химическими исследованиями, Дальтон ввел понятие атомного веса, определил атомные веса для целого ряда химических элементов. Большое значение в этой области имел открытый дальтоном в 1804 году закон кратных отношений в химических реакциях. Так, в 1804 в целом была сформулирована химическая атомистика. В 1808 году была опубликована книга «Новая система химической философии», содержащая основные положения атомистики. Дальтон внес существенный вклад в развитие химической символики. Ученый стал известен, в 1817 году он стал председателем Манчестерского литературно-философского общества. В 1822 году стал членом Лондонского королевского общества.
Умер Дальтон 27 июля 1844 года.
Его именем названа атомная единица массы (обозначение а. е. м.), она же дальто́н, — внесистемная единица массы, применяемая для масс молекул, атомов, атомных ядер и элементарных частиц.
Осознание того, что погода есть состояние атмосферы, а атмосфера есть смесь газов, привело Дальтона к открытию закона парциальных давлений. Поэтому законы Гей-Люссака справедливы и для любых смесей газов. Действительно, запишите уравнения (3) для каждой из компонент смеси и просуммируйте их. При выполнении этой операции не забудьте, что в смеси температуры всех ее компонент одинаковы. Кроме того, если в десятилитровом баллоне находится смесь газов, то каждый из них занимает объем в 10 литров. Идеальное мирное существование – никто никому не мешает! Вот смысл закона Дальтона. Итак, газ тело, собственной фигуры не имеющее, как поручик Киже.
А еще Дальтон прославил (или наоборот, ославил) свое имя названием дефекта зрения, учитесь собственные недостатки превращать в достоинства.
Джон Дальтон сам был дальтоником (но не знал этого термина), не различал красный цвет, он узнал о своей цветовой слепоте только в 26 лет. У него были три брата и сестра, и двое из братьев страдали цветослепотой на красный цвет. Дальтон подробно описал свой семейный дефект зрения в небольшой книге. Благодаря его публикации и появилось слово «дальтонизм», которое на долгие годы стало синонимом не только описанной им аномалии зрения в красной области спектра, но и любого нарушения цветового зрения.
Переместимся с туманного острова на солнечный Аппенинский полуостров и познакомимся с еще одним химиком, опередившим свое время, гипотеза которого стала законом уже после его смерти.
 Авогадро, Амедео
Авогадро, Амедео
Амедео Авогадро (граф итал. Lorenzo Romano Amedeo Carlo Avogadro di Quaregna e Cerreto) — итальянский физик и химик родился 9 августа 1776 в Турине.
Изучив право в Турине, он в 1796 получил учёную степень и был назначен секретарём префектуры департамента Эридано. Познакомившись самостоятельно с естественными науками, Авогадро решил посвятить себя им и в 1806 году поступил репетитором в Collegio delle provincie в Турине, а в 1809 перешёл учителем физики в гимназию.
В 1820 Авогадро был назначен профессором математической физики в Туринском университете. Спустя некоторое время эта кафедра была упразднена, и он поступил обратно в магистратуру на место советника счётной палаты, но был возвращён на кафедру и пробыл в Университете до 1850 г.
Авогадро впервые высказал гипотезу о том, что «одинаковые объёмы различных газов, при одинаковых температурах и давлениях, содержат одинаковое число молекул». Первая работа, в которой он изложил эту гипотезу, была напечатана Авогадро в 1811 г.
Гипотеза эта при своём появлении вызвала возражения и, не получив надлежащей оценки, вскоре была почти забыта. Лишь много лет спустя, особенно благодаря тем следствиям, которые вытекали из гипотезы Авогадро, она стала законом Авогадро, который, вместе с положениями термодинамики, лёг в основу теоретической химии.
Умер Авогадро 9 июля 1856.
Какое же значение имеет закон Авогадро для обсуждаемой нами темы? Вдумайтесь, ведь этот закон утверждает, что неизвестная постоянная в уравнении (4) просто пропорциональна числу частиц (молекул) в рассматриваемой порции газа, не важно каковы эти молекулы большие или маленькие, только надо уметь их сосчитать. К этому времени химики научились подсчитывать количества вещества (в молях), но не знали сколько частиц хотя бы в одном моле. Поэтому пришлось ввести неизвестную постоянную – постоянную Авогадро.
Одна из фундаментальных физических констант – постоянная Авогадро была введена в науку в 1811 на основе одноименного закона: «Один моль любого вещества содержит одинаковое число молекул». Однако понадобилось почти 100 лет, чтобы экспериментально определить численное значение этой постоянной. Эта задача впервые была решена французским физиком Ж. Перреном в начале XX века при кропотливом исследовании броуновского движения. Величина постоянной Авогадро оказалась громадной  , рекорд в таблице фундаментальных констант!
, рекорд в таблице фундаментальных констант!
К настоящему времени существует более 20 способов измерения постоянной Авогадро. Наиболее точное ее значение получено по экспериментальному измерению постоянной Фарадея. Как должно быть известно каждому старшекласснику, постоянная Фарадея равна произведению постоянной Авогадро на заряд электрона. Постоянную Фарадея в настоящее время измеряют при выполнении лабораторной работы в средней школе, а значение заряда электрона легко найти в … таблице фундаментальных физических констант.
Великая армия Наполеона еще не вторглась в Россию, но уже появились первые части «Фауста», а среди ученых еще не появилось человека, способного продать часть своей души Мефистофелю и понять смысл всех газовых законов, и объединить их в одном уравнении, и присвоить ему свое имя, а себе славу предшественников. Ведь к 1811 году вся подготовительная работа проведена, все необходимые законы открыты. Но не настало еще время великих обобщений: ученые говорят о сохранении «силы» и движения, но нет закона сохранения энергии; развит химический атомизм, но нет молекулярно кинетической теории; гремят паровые машины, превращая «теплоту в работу», но нет второго начала термодинамики; известны почти все законы электромагнетизма, но нет еще уравнений Максвелла. Продолжается эпоха кропотливого собирания фактов, но ждать остается не долго – до середины века. И вот она приближается и появляется уравнение состояния идеального газа, уравнение Клапейрона.
 Бенуа Поль Эмиль КЛАПЕЙРОН
Бенуа Поль Эмиль КЛАПЕЙРОН
Бенуа Поль Эмиль Клапейрон (Clapeyron), – французский физик и инженер, член Парижской АН (с 1858). Родился в Париже 26 января 1799 г. В 1818 г. окончил Политехническую школу. В 1820-1830 гг. работал в Петербурге в Институте инженеров путей сообщения. После возвращения во Францию был профессором (с 1844) Школы мостов и дорог в Париже. Осуществлял надзор над строительством первой французской железнодорожной линии от Парижа до Версаля и Сен-Жермена.
Физические исследования Клапейрона посвящены теплоте, пластичности и равновесию твердых тел. Он придал в 1834 г. математическую форму идеям C. Карно, первым оценив большое научное значение его труда «Размышления о движущей силе огня», содержащего фактически формулировку второго начала термодинамики. Исходя из этих идей, впервые ввёл в термодинамику графический метод – индикаторные диаграммы.
В 1834 г. вывел уравнение состояния идеального газа, объединяющее закон Бойля – Мариотта, законы Гей-Люссака и закон Авогадро, обобщённое в 1874 г. Д.И. Менделеевым (уравнение Менделеева – Клапейрона). Вывел уравнение, устанавливающее связь между температурой плавления и кипения вещества и давлением, которое было термодинамически обосновано в 1851 г. Р. Клаузиусом (уравнение Клапейрона – Клаузиуса ).
Умер 28 января 1864 г.
На первый взгляд заслуга Клапейрона в получении уравнения состояния не велика – подумаешь, объединил то ли 3, то ли 6 давно известных законов! Но не будем зазнаваться, он первый кто ввел само понятие уравнения состояния, осознал, что параметры любого тела, не только газообразного, но и жидкого, и твердого мы не в состоянии изменять произвольно: изменяешь один параметр неизбежно будут изменять другие и нет необходимости формулировать множество законов: зависимость давления от объема, зависимости давления и объема от температуры, странно, что не появилось законов типа зависимости давления от массы газа (а ведь зависит!) и т.д. достаточно записать одно уравнение состояния, из которого можно вывести все эти законы, как это и делают сейчас в том же школьном курсе физики!
Сейчас часто уравнение Клапейрона записывают в красивой форме
 , (5)
, (5)
но Клапейрон не мог записать его в такой форме, еще не появилась абсолютная температура, не построена шкала Кельвина, да и сам лорд Кельвин еще Уильям Томсон, и ему всего 10 лет.
 Уильям Томсон (лорд Кельвин)
Уильям Томсон (лорд Кельвин)
Уи́льям То́мсон, лорд Ке́львин (англ. William Thomson, 1st Baron Kelvin) один из величайших физиков родился 26 июня 1824 в Белфасте.. Уильям Томсон вместе со старшим братом, Джемсом учились в колледже в Глазго, а затем в в Кембридже, в котором Томсон закончил курс наук в 1845 г.
В 1846 г. двадцатидвухлетний Томсон занял кафедру теоретической физики в университете в Глазго.
Ещё студентом, Томсон опубликовал ряд работ по приложению рядов Фурье к вопросам физики и провёл важные аналогии между явлениями распространения тепла и электрического тока и показал, как решение вопросов из одной из этих областей применить к вопросам другой области. В другом исследовании Томсон развил принципы, которые затем плодотворно приложил ко многим вопросам динамической геологии, например, к вопросу об охлаждении земли.
В 1845 г. Томсон излагает свой метод электрических изображений, давший возможность просто решить многие труднейшие задачи электростатики.
С 1849 г. начинаются работы Томсона по термодинамике. Томсон, опираясь на исследования Джоуля, указывает, как следует изменить принцип Карно для того, чтобы принцип согласовался с современными данными; эта знаменитая работа содержит первую формулировку второго начала термодинамики. В 1852 г. Томсон даёт другую формулировку его, именно учение о рассеянии энергии. Входе этих работ Томсон вводит абсолютную шкалу температур (шкала Кельвина, градус Кельвина). Томсон совместно с Джоулем производит известное исследование над охлаждением газов при расширении без совершения работы, которое послужило переходной ступенью от теории газов идеальных к теории реальных газов.
В пятидесятых годах Томсон заинтересовывается вопросом о трансатлантической телеграфии; побуждаемый неудачами первых пионеров-практиков, Томсон теоретически исследует вопрос о распространении электрических импульсов вдоль кабелей и приходит к заключениям величайшей практической важности, давшим возможность осуществить телеграфирование через океан. Попутно, Томсон выводит условия существования колебательного электрического разряда, вновь найденные позже Кирхгоффом и легшие в основание всего учения об электрических колебаниях.
В 1866 г. Томсон возведён в дворянское достоинство, в 1892 г. королева Виктория пожаловала ему пэрство с титулом "барон Кельвин".
Умер лорд Кельвин 17 декабря 1907 года.
Велики заслуги ирландца Томсона, ставшим лордом Кельвином.
 Оцените…
Оцените…
Дадим перечень (далеко не полный) основных научных достижений лорда Кельвина.
Термодинамика:
- формулировка второго начала термодинамики;
- установление абсолютной шкалы температур (шкала Кельвина, градус Кельвина);
- охлаждение газов при дросселировании (эффект Томсона);
Электродинамика:
- открытие теплового эффекта при прохождении электрического тока по неоднородно нагретому проводнику (эффект Джоуля-Томсона);
- исследования электрических колебаний (в частности, в колебательном контуре – формула Томсона для периода колебаний);
- исследования прохождения импульсов по кабелям;
- разработка метода изображений в электростатике.
Кроме того, работы по гидродинамике и теории волн, динамической геологии, математической теории шаровых функций.
Не менее замечательна деятельность Томсона в практической физике и технике; ему принадлежит изобретение или улучшение многих инструментов: зеркального гальванометра, сифон-рекордера, квадрантного и абсолютного электрометров, нормального элемента компаса, лота и множества технических измерительных электрических приборов, между которыми "ампер-весы", на основании которых создан современный эталон единицы силы тока; между множеством патентов, взятых Томсоном, встречаются таковые и на чисто практические приспособления, как, например, на водопроводные краны.
Но и получил он всеобщее призвание: только два человека удостоились того, что их именем названа основная единица Международной системы единиц: Кельвин – единица температуры и Ампер – единица силы тока. Другие достижения Кельвина в теории газов выходят за рамки нашего затянувшегося рассказа, потихоньку переходящего в роман. Ограничимся одним указанием – он один из первых, кто показал, что обсуждаемое уравнение (1) является приближенным, обнаружил эффекты противоречащие ему. Но абсолютной шкале Кельвина ничего не грозит – она же абсолютная!
Вот и подошли мы к последней главе, покидаем западную Европу и направляемся в Санкт-Петербург, в Россию времен Александра II, царя, отменившего крепостное право. В условиях разумного либерализма бурно развивается российская промышленность, литература, искусство, наука. Всемирную славу получает выдающийся химик Д.И. Менделеев[5].
 Дмитрий Иванович Менделеев.
Дмитрий Иванович Менделеев.
Великий русский химик Д.И. Менделеев родился 8 февраля 1834 года в провинциальном Тобольске, он был семнадцатым ребенком в семье.
В 1850 году Д.И. Менделеев поступил в Петербургский педагогический институт на физико-математический факультет, который окончил в 1855 году с золотой медалью.
После окончания по совету врачей работал на юге в Симферополе и Одессе. После успешной защиты магистерской диссертации в 1857 году утвержден в должности приват- доцента в Петербургском университете. В течении двух лет работал за границей, принимал участие в работе Первого международного съезда химиков в Карсруэ.
В 1861 году издал первый русский учебник по органической химии.
В 1863 году Д.И. Менделеев получил место профессора Петербургского технологического института, не имея еще докторской степени. Докторскую диссертацию защитил в 1865 году.
В 1869 году появились знаменитые «Основы химии», где вслед за предисловием поместил таблицу «Опыт системы элементов, основанный на их атомном весе и химическом сходстве» - знаменитая периодическая система элементов, главное научное достижение Д.И. Менделеева. На основе открытого периодического закона предсказал существования и указал ряд свой неизвестных химических элементов, которые были открыты впоследствии.
Литературное наследие Д.И. Менделеева огромно, оно содержит 431 печатную работу по проблемам химии, физики, геофизики, техники и промышленности; экономическим и общественным проблемам. Ученый принял активное участие в издании «Энциклопедического словаря» Брокгауза и Эфрона, редактируя химико-технический и промышленный отделы и выступая как автор ряда статей.
В 1898 году был назначен хранителем Главной палаты мер и весов.
Умер Д.И. Менделеев 2 февраля 1907 года.
Именем Менделеева названы: подводный хребет в Ледовитом океане, вулкан на о. Кунашир, кратер на Луне, минерал менделеевит, 101-й химический элемент менделевий и др.
Грандиозный успех открытого Д.И. Менделеевым периодического закона, периодической таблицы, предсказание новых химических элементов и их свойств затмили другие его достижения. Многие ученые пытались нащупать закономерность в свойствах известных тогда 64 химических элементов, выдвигая различные исходные идеи, но увы…
О всеобщей связи явлений.
Английский химик Ньюлендс, человек, вероятно, верил, что те соотношения, которые существуют между химическими элементами, похожи на соотношения между музыкальным тоном и его октавой. Ньюлендс построил-таки свою систему, искусственно впихивая в нее элементы, подстругивая их под те размеры, которые сам же и уготовил. Система была, но системы элементов не было. Ньюлендсу пришлось пережить пренеприятные минуты, когда председатель британского съезда естествоиспытателей спросил его, не пряча иронии: «Не пробовал ли уважаемый джентльмен расположить элементы по алфавиту и не усмотрел ли он при этом каких-либо закономерностей?»
Менделеев смотрел в самую суть явлений и не пытался искать какую-то внешнюю связь, объединяющую все элементы в фундаменте мироздания. Он пытался понять - что их связывает и что определяет их свойства. Менделеев расположил элементы по возрастанию их атомного веса и стал нащупывать закономерность между атомным весом и другими химическими свойствами элементов. Он пытался понять способность элементов присоединять к себе атомы сородичей или отдавать свои. Он вооружился ворохом визитных карточек и написал на одной стороне название элемента, а на другой - его атомный вес и формулы его некоторых важнейших соединений. Он снова и снова перекладывал эти карточки, укладывая их по свойствам элементов. И в его сознании всплывали какие-то новые закономерности, и он со знакомым волнением, предшествующим открытию, осторожно продвигался дальше и дальше. Часами он сидел, склонившись над своим столом, снова и снова вглядываясь в записи, и ощущал, как начинала кружиться от напряжения голова и как глаза застилала дрожащая пелена... Говорят, что во сне к нему пришло озарение, и что ночью ему привиделось, как, в каком порядке надо разложить те карточки, чтобы все легло по своим местам по закону природы. Может быть. Мозг человека всегда бодрствует. Но шел-то Менделеев к этому прозрению годами! Он продвигался осмысленно, заранее намечая и рассчитывая каждый свой очередной шаг. Может, и было то озарение, но его нельзя назвать случайным. Менделеев нашел связь даже между самыми непохожими элементами. Он обнаружил, что свойства элементов, если их разместить в порядке возрастания атомных весов, через правильные промежутки повторяются. Менделеев понимал: случайностью это быть не могло. Тогда он сделал последний - решающий шаг: расположил все элементы еще и по группам, объединив в отдельные семьи ближайших родственников. Он настолько ясно видел стройность созданной им системы, что, заметив отсутствие элемента между алюминием и титаном, оставил ему свободное место.
В некотором смысле работа над периодической системой была личным делом ученого, которым он занимался в свободное «от работы» время.
В наибольшей степени Д. И. Менделеев выступал как химик-технолог, многие его работы посвящены проблемам производства, например, очень важного для России спирто-водочного.
О выборе темы…
Название докторской диссертации Д.И. Менделеева «О соединении спирта с водой». Д.И. Менделеев обнаружил, что раствор спирта в воде обладает «необычайными физико-химическими свойствами», в «Истории водки» к ним добавляются также свойства «биохимические и физиологические». Тем самым, русский ученый «научно доказал, что составление водки, то есть соединение хлебного спирта с водой, должно точным отвешиванием определенной части спирта». В «Кулинарном словаре» к этому добавляются новые подробности: «…только при таком смешении сивушные масла, остающиеся после ректификации, оказываются во взвешенном состоянии и могут быть убраны фильтром...»
Нет данных и о том, что Менделеев изучал биохимические свойства спиртоводных растворов различных концентраций, а также их физиологическое действие.
Легенда об изобретении водки
Дмитрий Менделеев в 1865 году защитил докторскую диссертацию на тему «Рассуждение о соединении спирта с водою», нисколько с водкой не связанную. Менделеев, вопреки сложившейся легенде, водку не изобретал; она существовала задолго до него.
На этикетке «Русского стандарта» написано, что данная водка «соответствует стандарту русской водки высшего качества, утверждённому царской правительственной комиссией во главе с Д. И. Менделеевым в 1894 году». С именем Менделеева связывают выбор для водки крепости в 40°. Согласно информации «Музея Водки» в Санкт-Петербурге, Менделеев считал идеальной крепостью водки 38°, но это число было округлено до 40, для упрощения расчёта налога на алкоголь.
Однако в трудах Менделеева отыскать обоснование этого выбора не удаётся. Диссертация Менделеева, посвящённая свойствам смесей спирта и воды, никак не выделяет 40° или 38°. «Царская правительственная комиссия» никак не могла установить данный стандарт водки уже хотя бы потому, что эта организация — Комиссия для изыскания способов к упорядочению производства и торгового обращения напитков, содержащих в себе алкоголь, — была образована по предложению С. Ю. Витте только в 1895 году. Причём Менделеев выступал на её заседаниях в самом конце года и только по вопросу об акцизах.
Откуда же взялся 1894-й год? По-видимому, из статьи историка Вильяма Похлёбкина, который написал, что «спустя 30 лет после написания диссертации… соглашается войти в комиссию». Изготовители «Русского стандарта» прибавили метафорические 30 к 1864 году и получили искомую величину.
Директор музея Д. И. Менделеева, Игорь Дмитриев, по поводу 40-градусной водки сказал следующее:
Ее изобрело русское правительство в то время, когда Менделееву было 9 лет от роду. В те времена акциз брали с градуса, его надо было измерять, а шкала измерений была не точной. Кроме того, оказывалось, что на пути от производителя к потребителям (розничная торговля) водка имело свойство снижать градусы. Тогда правительство издало указ, по которому водка должна была поступать к потребителю исключительно 40-градусной, минимум – 38-градусной. В противном случае участникам процесса грозила уголовная ответственность.
Множество работ Д.И. Менделеева посвящено другим отраслям промышленности.
Мы уже упоминали о введении сначала во Франции, затем и в других европейских странах метрической системы мер. Провести ту работу в России предстояло Д.И. Менделееву, который как настоящий ученый естествоиспытатель понимал важность проблемы установления единой системы мер и их эталонов. Впрочем, эта проблема важна не только для науки, без «правильно» обточенных гирь не может работать даже обычный рынок. К сожалению торговцев, в настоящее время широкое распространение получили электронные весы, «выверять» которые стало значительно труднее.
Дата добавления: 2020-12-12; просмотров: 282; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
