Олигосахариды. Их свойства и роль в пищевой промышленности
Лекция 7-8, 9-10
Изменения углеводов при технологической обработке
План лекции
1. Роль углеводов для организма человека. Классификация, состав и свойства углеводов
2. Моносахариды. Их свойства и роль в пищевой промышленности
3. Олигосахариды. Их свойства и роль в пищевой промышленности
4. Превращения моноз и олигосахаридов
4.1 Гидролиз ди- и трисахаридов
4.2 Брожение сахаров
4.3 Карамелизация сахаров
4.4 Реакция меланоидинообразования
5. Полисахариды пищевых продуктов и их свойства
5.1 Глюканы
5.2 Фруктаны
5.3 Гетерогликаны
6. Пищевые волокна
6.1 Источники и методы выделения
6.2 Обогащение пищевыми волокнами продуктов питания
Литература
1. Бобровник Л.Д., ЛезенкоГ.А. Углеводы в пищевой промышленности. - К.: Урожай, 1991. - 112 с.
1. Классификация, состав и свойства углеводов
Углеводы являются важным классом природных соединений. Они широко распространены в живых организмах, особенно в растениях - 90-80% на сухое вещество (в животных тканях - 2% на с.в.).
ü Ежегодно на нашей планете благодаря фотосинтезу образуется 40 млрд тонн углеводов.
Название “углеводы” возникло в начале знакомства с ними в прошлом столетии: их рассматривали как гидраты углерода. Общая формула углеводов С m H 2 n On может быть представлена в виде: Cm ( H 2 O ) n . Отсюда угле-воды.
В 1927 г. Комиссия по реформе химической номенклатуры предложила называть углеводы глицидами.
|
|
|
В 1978 г. им вернули первоначальное название - углеводы.
Роль углеводов для организма человека
n энергетическая - потребность человеческого организма в энергии покрывается в большей части именно за счет углеводов; окисление 1г углеводов даёт 4ккал энергии
n пластическая: производные углеводов - мононуклеотиды - это структурные компоненты нуклеиновых кислот, мукополисахариды - цементирующее веещство рыхлой соединительной ткани, смазка в суставах - рыхлое вещество углеводной природы;
n защитная - участвуют в процессах, препятствующих проникновению в организм болезнетворных м/о, липополисахариды - антигены - участвуют в формиров. иммунитета;
n опорная - входят в состав скелета высших растений, грибов, насекомых (целлюлоза и хитин);
n специфические функции:
- рецепторы для связывания токсинов(глюкуроновая кислота);
-гепарин - углеводсодержащий биополимер - предотвращает свертывание
крови - природный антикоагулянт;
- гетерополисахариды определяют группу крови
n резервная - гликоген в животных организмах; (крахмал в клубнях, зерновых)
Существует рациональная классификация углеводов. Рассмотрим схему подразделения углеводов на группы и подгруппы:
|
|
|
Классификация углеводов
| Группа | Подгруппа | Название | Число мономерных единиц |
| I Моносахариды | - | Монозы (триозы, тетрозы, пентозы, гексозы, гептозы, октозы, нонозы, декозы) и их производные Глюкоза, фруктоза | 1 |
| ІІ Голозиды 1) Олигосахариды ( oligos - греч. - немногий) | |||
| а) гомо- и гетероолигосахариды низшие | Олигозы (дисахариды или биозы, трисахариды или триаозы, тетраозы, пентаозы) сахароза(глюкоза+фр), трегалоза (2глюкозы), лактоза(глюк+галакт) | 2-5 | |
| б) гомо- и гетероолигосахариды высшие | Олигозы (гексаозы, гептаозы, октаозы, нонаозы, декаозы) | 6-10 | |
| 2) Полисахариды | а) гомополисахариды | Полиозы - гомогликаны (глюкан, маннан, фруктозан) целлюлоза, инулин, крахмал | Больше 10 |
| б)гетерополисахариды | Полиозы – гетерогликаны пектиновые вещества | Больше 10 | |
| III Гликоконъюгаты (полисахариды находятся в связанном - конъюгированном - виде) | а) гликопротеины б) пептидогликаны в) гликолипиды г) гликолипопротеины | Клетчатка, пищевые волокна - | разное |
С6Н12О6 гексозы¸ С12Н22О11 дисахариды, (С6Н10О5)п полисахариды
Полисахариды (голозиды) - сложные углеводы, молекулы которых при гидролизе распадаются на моносахариды. Гомо- , гетеро- п составу моносахаридных остатков
|
|
|
Моносахариды. Их свойства и роль в пищевой промышленности
Моносахариды (простые сахара) - кристаллические бесцветные вещества, хорошо растворимы в воде, сладкие на вкус. Обладают сильными восстанавливающими (редуцирующими) свойствами.
Восстановление меди в оксиде меди, серебра в оксиде серебра (реакция серебряного зеркала), раствора Фелинга - качественные реакции на моносахариды. Сами они окисляются до кислоты.
Моносахариды представляют собой многоатомные альдегидо- и кетоноспирты. В зависимости от природы функциональных групп их подразделяют на:
альдозы и кетозы;
в зависимости от количества атомов углерода в молекуле -
на триозы, тетрозы, пентозы, гексозы и т.д. (см. таблицу).
Природных моносахаридов, имеющих более 9 углеродных атомов не выявлено. Углеродные атомы в молекулах моносахаридов нумеруют таким образом, чтобы атом С карбонильной группы имел наименьший номер
Наибольшее значение в перарабатывающей промышленности имеют пентозы:
               СНО
Н ОН
НО Н
Н ОН
СН2ОН
D - ксилоза СНО
Н ОН
НО Н
Н ОН
СН2ОН
D - ксилоза
|     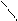        СНО
Н ОН
Н ОН
Н ОН
СН2ОН
D - рибоза СНО
Н ОН
Н ОН
Н ОН
СН2ОН
D - рибоза
|     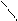    СНО
НО Н
Н ОН
Н ОН
СН2ОН
D - арабиноза СНО
НО Н
Н ОН
Н ОН
СН2ОН
D - арабиноза
|
гексозы:
|
|
|
     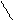 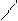                         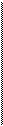        СНО
1
Н 2 ОН
НО 3 Н
Н 4 ОН
Н 5 ОН
6
СН2ОН
D - глюкоза СНО
1
Н 2 ОН
НО 3 Н
Н 4 ОН
Н 5 ОН
6
СН2ОН
D - глюкоза
|      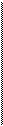        СНО
НО Н
Н ОН
НО Н
НО Н
СН2ОН
L - глюкоза СНО
НО Н
Н ОН
НО Н
НО Н
СН2ОН
L - глюкоза
|      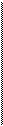        СНО
НО Н
НО Н
Н ОН
Н ОН
СН2ОН
D - манноза СНО
НО Н
НО Н
Н ОН
Н ОН
СН2ОН
D - манноза
|
        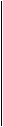              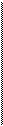       СНО
Н ОН
НО Н
НО Н
Н ОН
СН2ОН
D - галактоза СНО
Н ОН
НО Н
НО Н
Н ОН
СН2ОН
D - галактоза
| СН2ОН О О НО Н Н ОН Н ОН СН2ОН D - фруктоза |
ü Моносахариды причисляются к D- или L- ряду по конфигурации последнего хирального (асимметрического) атома углерода монозы (метод Фишера). В качестве образца при этом используется глицериновый альдегид. Чаще встречается D - форма.
О С Н Н - С - ОН
СН2ОН D - глицериновый альдегид | 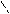 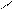 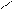 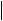 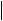 О
С
Н
НО - С - Н
СН2ОН
L - глицериновый альдегид
О
С
Н
НО - С - Н
СН2ОН
L - глицериновый альдегид
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
В природе моносахариды обычно существуют в виде циклических форм:
Водород гидроксильной группы (у 5 атома углерода), имеющий частично положительный заряд, переходит к кислороду альдегидной группы с частично отрицательным зарядом. В результате этого у первого углеродного атома и у атома кислорода при 5 атоме углерода освобождается по одной валентности, за счёт которых эти атомы связываются между собой кислородным мостиком.
 | |||
 | |||
фуранозная форма 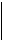




 пиранозная форма
пиранозная форма
(может быть в конфор - (форма лодки или кресла)
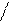








 мации “твист”или конверт)
мации “твист”или конверт)
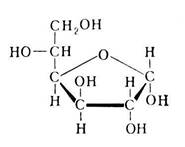
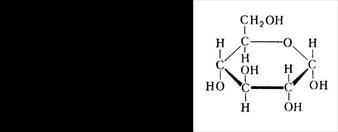
Циклічна форма. D-глюкофураноза D-глюкопіраноза. Циклічна форма.
ü Термодинамически наиболее устойчива пиранозная (шестичленная) форма.
К важнейшим моносахаридам относятся глюкоза и фруктоза.
D - глюкоза, или виноградный сахар, чрезвычайно широко представлена в животных и растительных организмов.
Содержится в семенах, корнях, цветах, листьях и плодах большинства растений как в свободном виде, так и в составе многих олигосахаридов (мальтозы, сахарозы, лактозы, раффинозы) и ряда гликозидов. Из глюкозы построены основные полисахариды растительной клетки - целлюлоза, крахмал, гликоген.
Особенно много глюкозы в винограде, сладких яблоках, ягодах и др.
Глюкоза характеризуется правым вращением плоскополяризованного света (aD20 = + 52,3°), в связи с чем в зарубежной литературе она часто встречается под названием декстроза.
Глюкоза очень хорошо растворяется в воде, легко дает пересыщенные растворы (сиропы). В спирте глюкоза растворяется значительно хуже.
Из спирта и воды при слабом нагревании кристаллизуется в виде безводных кристаллов, а из воды при температуре 20 ° С – в виде кристаллогидрата с одной молекулой воды.
Кристаллы глюкозы имеют белый цвет и приятный сладкий вкус. Она менее сладкая, чем сахароза, и не маскирует аромат и вкус других веществ в пищевых компонентах.
В чистом виде глюкоза усваивается организмом лучше всех других углеводов, поэтому ее широко используют в медицинской практике.
D - фруктоза, или плодовый сахар, - наиболее важный представитель кетоз, также широко распространенный в растительном мире. Левое вращение растворов D-фруктозы (aD20 = - 93°) обусловливает другое ее название - левулоза.
Наряду с глюкозой фруктоза содержится во многих сладких плодах, арбузах, меде. Высокая сладость меда и арбузов (при относительно невысоком содержании сахаров - 7%) объясняется тем, что они представлены преимущественно фруктозой, которая в 1,4 раза слаще сахарозы.
Фруктоза очень трудно кристаллизуется в кристаллах состава 2С6Н12О6.Н2О.
Рассмотрим некоторые химические свойства моносахаридов, имеющие важное значение для пищевой промышленности.
1. Восстановление альдегидной или кетонной группы моноз с образованием многоатомных спиртов - альдитов.
Осторожным восстановлением D - глюкозы получают D - глюцит (сорбит); D - ксилозы - пентит (D - кислит), которые широко применяются в лечебном питании. При восстановлении D - фруктозы образуется смесь двух гекситов - D-глюцита и D-маннита.
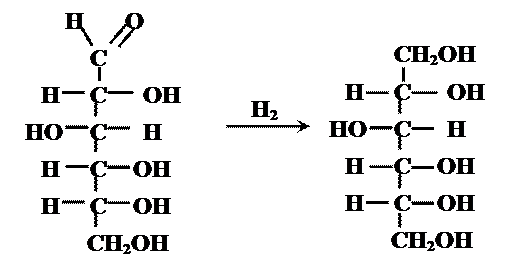 |
Восстановление глюкозы в сорбит - одна из стадий при синтезе витамина С (в промышленном масштабе), когда глюкозу каталитически гидрируют водородом.
2. Дегидратация под действием кислот.
Альдозы более устойчивы к действию кислот, чем щелочей. Однако в зависимости от условий и природы моносахарида он может в кислой среде подвергаться гидролизу.
Так, при упаривании растворов D-глюкозы (и других альдоз) в присутствии разбавленных минеральных кислот возможны реакции:
межмолекулярной конденсации (т.н. “реверсия”), которая приводит к образованию ди-, три-, тетра- и других олигосахаридов или
внутримолекулярной конденсации - с образованием 1,6 - ангидро b -пираноз.
В более жестких условиях в присутствии кислот происходит глубокая дегидратация, которая ведет к образованию оксиметил фурфурола, а затем (при кипячении) к дальнейшему разложению на левулиновую и муравьиную кислоты.
3. Взаимодействие со щелочами.
ü При разработке и осуществлении технологических схем с участием углеводов необходимо учитывать повышенную чувствительность моноз к действию щелочей.
При действии разбавленных щелочей на холоде D-глюкоза подвергается эпимеризации, частично превращаясь в стереоизомерную альдозу (D-маннозу), а также изомеризации - в D-фруктозу.
В более жестких условиях в присутствии щелочей происходит перегруппировка с образованием сахариновых кислот, а также сложные реакции распада моноз с образованием трехуглеродных фрагментов - пировиноградной, молочной кислот и др.
Изомерия моносахаридов
5 видов:
1. изомерия альдоз и кетоз с открытой цепью и с одинаковым числом атомов углерода в молекуле. Н-р: глюкоза, манноза, галактоза, фруктоза имеют одинаковую молекулярную формулу С6Н12О6, т.е.являются изомерами
2. оптическая изомерия (стереоизомерия) открытых форм моносахаридов обусловлена наличием асимметрических атомов углерода в молекуле. Природная глюкоза является D-изомером, вращает плоскость поляризации вправо, поэтому обозначается D(+)-глюкоза. Природная фруктоза – левовращающий изомер, поэтому обозначается D(-)-фруктоза
3.Моносахариды D- или L- ряда (по конфигурации последнего хирального атома углерода)
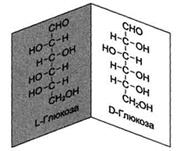
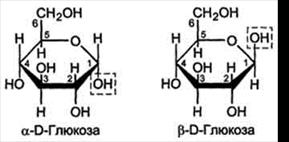
4. Стереоизомеры циклических форм в зависимости от расположения водорода и полуацетального гидроксила у первого атома углерода относительно плоскости кольца делят на α- и β- формы. В перспективных формулах (по Хеуорсу) полуацетальный гидроксид в α- форме направлен вниз от плоскости кольца, а в β- форме – вверх.
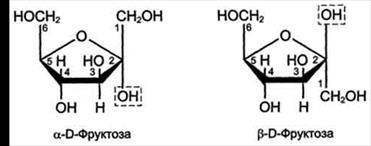
5. Циклоцепная таутометрия – обуславливается переходом открытых форм моносахаридов в циклические и наоборот. Открытая и циклическая формы моносахаридов представляют собой таутомерные формы и являются таутомерными изомерами. Таутомеры – это такие изомеры, которые способны самопроизвольно переходить друг в друга, образуя равновесную систему. Таутомерные превращения возможны, если вещество, способное ктаутометрии, находится в жидком состоянии.
ü Под действием щелочей и оксидов некоторых металлов из моносахаридов легко получаются сахараты - производные типа алкоголятов. Разная растворимость глюкозата и фруктозата кальция используется для разделения глюкозы и фруктозы.
Лекция №8
Олигосахариды. Их свойства и роль в пищевой промышленности
Олигосахариды относятся к классу голозидов. (табл) Все голозиды можно рассматривать , как продукты дегидратации двух и более молекул моносахаридов.
Олигосахариды обладают рядом свойств, сближающих их с простыми углеводами (монозами): они легко растворяются в воде, в большинстве случаев обладают сладким вкусом; их легко можно получить в виде хорошо образованных кристаллов.
Поэтому химики называют их сахароподобными сложными (состоящими из простых) углеводами.
Олигосахариды классифицируют по нескольким признакам:
- по числу молекул (см. таблицу);
- по составу моносахаридных остатков (гомо-, гетеро-);
- по характеру гликозидной цепи - линейные, разветвленные;
- по строению молекулы - восстанавливающие (редуцирующие), невосстанавливающие.
В молекулах олигосахаридов, как правило, остатки моносахаридов соединяются между собой за счет углерода полуацетального гидроксила одной молекулы и кислорода полуацетального или спиртового гидроксила другой молекулы.
Что такое полуацетальный гидроксил? (слайд) При образовании моносахаридом циклической формы появляется новый гидроксил (у глюкозы – возле первого атома углерода, у фруктозы – возле 2-го) называемый полуацетальным или глюкозидным. В реакциях он обычно более активен, чем остальные.
 |
В восстанавливающих олигосахаридах одна молекула моносахарида на образование связи затрачивает полуацетальный гидроксил, другая - спиртовой; тогда полуацетальный гидроксил остается свободным.
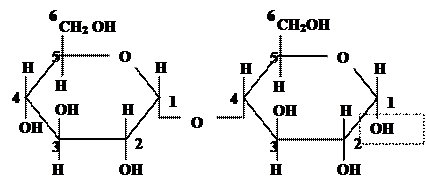 |
Мальтоза: Остатки молекул α- D-глюкозы
Мальтоза:





 О 1®4 О
О 1®4 О





 a-D-глю a-D-глю
a-D-глю a-D-глю



 О
О
Целлобиоза





 О 1®4 О
О 1®4 О
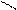





 b-D-глю О b-D-глю
b-D-глю О b-D-глю
 | |||
 | |||
Лактоза











 О 1®4 О
О 1®4 О
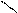
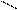





 b-D-гал О a-D-глю
b-D-гал О a-D-глю
 | |||
 | |||
В невосстанавливающих олигосахаридах два соседних моносахарида соединены за счет полуацетальных гидроксилов.
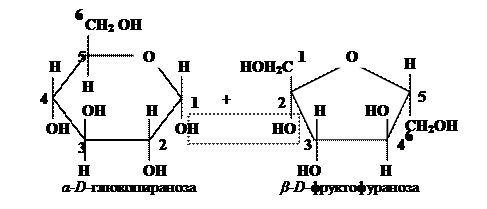 сахароза
сахароза
трегалоза
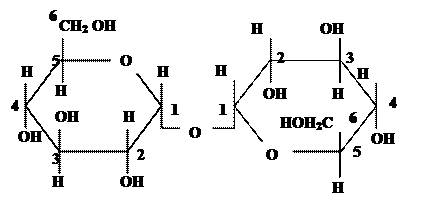 |
Раффиноза


 О 1®6
О 1®6




 a-D-гал О
a-D-гал О





 О 1®2 О
О 1®2 О


 a-D-глю
a-D-глю 

 О b-Dфр
О b-Dфр
Характеристика олигосахаридов
Дата добавления: 2021-03-18; просмотров: 163; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!