Внимательно читайте задание.
Лабораторная работа № 5
По теме « Химические свойства карбоновых кислот
На примере уксусной кислоты)»
(учебники- автор Г.Е. Рудзитис, стр. 107-108,
автор О.С. Габриелян,&12 )
I . Диссоциация
В пробирку с уксусной кислотой добавляю несколько капель индикатора:
Наблюдаю:(указать, какие изменения произошли)
1) универсальная индикаторная бумага – в кислой среде окрашивание в розовый цвет.
2) синий лакмус- в кислой среде красный
3) бесцветный фенолфталеин- в кислой среде бесцветный
4) метилоранж – красный (при наличии катиона Н+, который образуется при диссоциации кислот, поэтому метилоранж действует на кислоту). (4 б)
Составить уравнение реакции, дать название ионам.
| CH3COOH+C14H14N3NaO3S à C14H14N3NaO3S(CH3COO(-)) +H+ |
| уксусная кислота (этановая) + метиловый оранжевый à ион кислая форма + катион в одорода |
Вывод: реакция среды-кислая из-за наличия катиона H + (1б)
(2 б )
    O O O O
     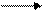 CH3 C CH3 C + H+
OH O -
уксусная кислота анион кислотного остатка катион в одорода CH3 C CH3 C + H+
OH O -
уксусная кислота анион кислотного остатка катион в одорода
|
II . Взаимодействие с активными металлами.
|
|
|
В пробирку с уксусной кислотой помещаю несколько гранул цинка и нагреваю.
Наблюдаю: Растворение окиси меди и образование раствора ярко-голубого цвета. Выделяется водород.
(указать, какие изменения произошли). (1б)
 Составить уравнение реакции, дать название веществам. (2 б )
Составить уравнение реакции, дать название веществам. (2 б )
CH3COOH + Zn à t℃à (CH3COO)2Zn+H2
уксусная кислота цинк ацетат цинка водород
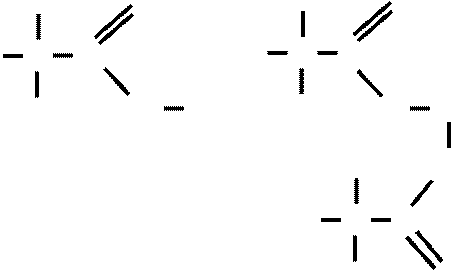 H O H O
t℃ H O H O
t℃
 2H C C + Zn à à H C C +H2
H O H H O Zn
H O
H C C
H O 2H C C + Zn à à H C C +H2
H O H H O Zn
H O
H C C
H O
|
III . Взаимодействие с оксидами металлов.
В пробирку с уксусной кислотой помещаю несколько крупинок оксида меди (II) и нагреваю.
Наблюдаю: растворение CuO и появление раствора ярко- голубого окраски цвета. (указать, какие изменения произошли). (2б)
Составить уравнение реакции, дать название веществам
|
|
|
2CH3COOH+CuO à t℃à (CH3COO)2Cu+H2O (2 б )
      H O H O H O H O
  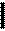    2H C C + Cu=O à H C C + H2O 2H C C + Cu=O à H C C + H2O
O H | |||||||||||
уксусная кислота оксид меди ацетат меди вода
IV. Взаимодействие с солями.
В пробирку с уксусной кислотой помещаю несколько кусочков мела.
Наблюдаю: образование средней соли ацетат кальция с выделением углекислого газа и воды, иначе говоря растворение мела и выделение пузырьков (указать, какие изменения произошли), (2б)
Составить уравнение реакции, дать название веществам. (2б)
|
|
|
2CH3COOH + CaCO3 à (CH3COO)2Ca + CO2 + H2O
уксусная кислота мел ацетат кальция углекислый газ вода
          H O O H O H O O H O

     2H C C + O C O à H C C + O=C=O 2H C C + O C O à H C C + O=C=O
 + +
   H O H H Ca H H H O H H Ca H H
  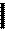 O O O O
     H C C
O H
H H C C
O H
H
|
V. Взаимодействие со спиртами.
В пробирку наливаю 2 мл уксусной кислотой и добавляю 2 мл этилового спирта. Затем осторожно добавляю 1 мл концентрированной серной кислоты и речной песок. Смесь нагреваю.
|
|
|
Наблюдаю: (указать, какие изменения произошли). (2б)
1) Составить уравнение реакции;
2) дать название веществам;
t℃, H2SO4
CH3COOH+CH3CH2OH à CH3COOC2H5 + H2O (5 б)
уксусная кислота этанол этиловый эфир вода
уксусной кислоты (этилацетат)




 O t℃, H2SO4 O
O t℃, H2SO4 O



 CH3 C + H - OC2H5 à CH3 C + O - H + H
CH3 C + H - OC2H5 à CH3 C + O - H + H
O-H OC2H5
Песок в реакции не участвовал. Его добавляют, чтобы не было образования центров локального вскипания смеси.
3) указать условия протекания реакции: кислая среда, нагревание.
4) указать механизм протекания реакции: данный процесс классифицируют как реакцию присоединение-отщепление (нуклеофильное замещение)
5) дать название реакции: этерификация.
   H H H O H H H O
 
      H C C O H + H C C à H C C O H + H C C à
H
H H H |
Критерии оценивания:
За работу выставляется две оценки:
за наблюдения – баллы чёрным цветом, за уравнения- красным.
Пояснения к работе:
1) Печатайте описание работы и наблюдения.
2) От руки пишете уравнения реакций (если получится, то печатайте). Все формулы в структурном виде!
3) Отправляйте напечатанную выполненную работу почтой: ZSBurina@gmail.com до 17.04.2020г.
Внимательно читайте задание.
Дата добавления: 2021-03-18; просмотров: 54; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!



 H O
H O


 H C C
H C C




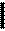

 O H H
O H H
 O C C H
O C C H