Энергия активации: 38 кДж/моль
Лабораторная работа № 2 Вариант 1
Кинетика химических реакций
Цель работы:
Изучение кинетики химической реакции: H 2 SO 4 + Na 2 S 2 O 3 ® Na 2 SO 4 + SO 2 + H 2 O + S ¯
1. Выявление зависимости скорости реакции взаимодействия раствора серной кислоты постоянной концентрации и раствора соли [тиосульфат натрия ( Na 2 S 2 O 3 )] переменной концентрации от концентрации соли. Определение кинетического порядка реакции по соли.
2. Установление зависимости скорости реакции от температуры. Определение энергии активации (Еа) и температурного коэффициента (g ) реакции.
Для выполнения и защиты лабораторной работы студент должен знать:
1. Зависимость скорости реакции от концентрации реагирующих веществ при постоянной температуре (ЗДМ – закон действующих масс):
v = k ( T ) × C к x × Ccy , где
v – скорость реакции; k ( T ) – константа скорости реакции (постоянная величина при Т= const); C к и Cc – концентрация кислоты и соли [ 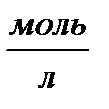 ]; x, y – кинетический порядок реакции по кислоте и соли (стехиометрические коэффициенты в молекулярном уравнении); (x + y ) - суммарный кинетический порядок реакции
]; x, y – кинетический порядок реакции по кислоте и соли (стехиометрические коэффициенты в молекулярном уравнении); (x + y ) - суммарный кинетический порядок реакции
2. Зависимость константы скорости реакции от температуры (уравнение Аррениуса):
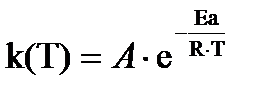 , где
, где
Еа – энергия активации реакции [  ]; Т – температура [К]; R = 8,314 [
]; Т – температура [К]; R = 8,314 [ 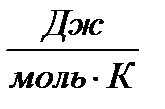 ] - универсальная газовая постоянная, А – частотный фактор
] - универсальная газовая постоянная, А – частотный фактор
3. Понятие температурного коэффициента (Вант-Гоффа) реакции g :g = 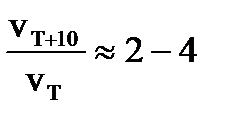
|
|
|
Выполнение работы
Измерение скорости реакции v : v = 1 / t (с-1) - скорость реакции
t (с) – время протекания реакции - время между моментом сливания растворов кислоты и соли, и моментом визуальной регистрации образования осадка серы (помутнение раствора). Измеряется секундомером с точностью ±0.5 с.
Поскольку скорость исследуемой реакции является функцией трех параметров (температура, концентрации реагентов - соли и кислоты), то, изучая кинетику реакции, определяют влияние на скорость реакции только одного параметра, два других не меняют, оставляя их постоянными.
1. Экспериментальное определение зависимости скорости реакции от концентрации соли (Ск– const ; Т– const ).
- Расчет объемов реагентов. Суммарный объем растворов реагентов во всех опытах равен 25 см3. Объем раствора кислоты во всех опытах равен V к = 5 см3 (Ск– const ).
Для приготовления различных значений концентрации водных растворов соли, остальной объем (20 см3) будут составлять раствор соли V с, с концентрацией С0= 0.5 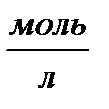 , и объем воды V в, т.е. V с + V в = 20 см3. Из соотношения Сс( Vc + V в + V к) = С0 Vc следует, что С c = 0,02 Vc . Зная значение концентрации раствора соли С c необходимое для приготовления и выполнения опыта, объём соли Vc определяют из соотношения Vc = С c / 0,02. Объём воды V в, необходимый для добавления к Vc , чтобы приготовить раствор соли нужной концентрации Сс, находят из соотношения V в = 20 - Vc [ см3 ].
, и объем воды V в, т.е. V с + V в = 20 см3. Из соотношения Сс( Vc + V в + V к) = С0 Vc следует, что С c = 0,02 Vc . Зная значение концентрации раствора соли С c необходимое для приготовления и выполнения опыта, объём соли Vc определяют из соотношения Vc = С c / 0,02. Объём воды V в, необходимый для добавления к Vc , чтобы приготовить раствор соли нужной концентрации Сс, находят из соотношения V в = 20 - Vc [ см3 ].
|
|
|
- Выполнение измерений. При помощи бюреток с водой, раствором соли и кислоты помещают:
- в измерительный стакан соответствующие объемы воды и раствора соли (V с + V в = 20 см3)
- в пробирку раствор кислоты (V к = 5 см3)
- приливают раствор кислоты из пробирки в измерительный стакан и по секундомеру определяют время протекания реакции.
- результаты измерений и расчетов вносят в таблицу 1
- по экспериментальным точкам строят график v= f( Cc)
- по виду графика определяют кинетический порядок реакции по соли (y)
Таблица 1
| № | Сс | Vc = С c / 0,02 | Vв = 20 - Vc | Vк | t | v = 1 / t | v ·102 |
| моль/л | см3 | см3 | см3 | с | с-1 | с-1 | |
| 1 | 0,09 | 5 | |||||
| 2 | 0,19 | 5 | |||||
| 3 | 0,30 | 5 | |||||
| 4 | 0,38 | 5 |
Пример заполнения данными табл.1
| № | Сс | Vc | Vв | Vк | t | v = 1 / t | v ·102 |
| моль/л | см3 | см3 | см3 | с | с-1 | с-1 | |
| 1 | 0,10 | 5 | 15 | 5 | 82 | 0,01219 | 1,22 |
Пример построения графика по данным табл.1
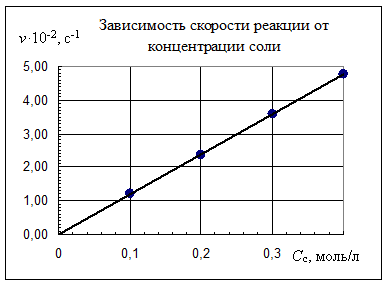 Кинетический порядок реакции по соли y =1.
Кинетический порядок реакции по соли y =1.
2. Экспериментальное определение зависимости скорости реакции от температуры [Ск – const ; Сс – const , Сс =0,09 моль/л].
|
|
|
- Выполнение измерений. Объем раствора кислоты во всех опытах равен V к = 5 см3 (Ск– const). Измерение скорости реакции определяют так же, как и в первой части работы, при выполнении следующих условий:
- определение скорости одной и той же реакции (Ск – const ; Сс – const ) проводят при различных температурах, что приводит к изменению константы скорости реакции k ( T ). Для этого перед измерением t – времени протекания реакции, стакан с раствором соли(Сс =0,09 моль/л) и пробирку с раствором кислоты помещают в водяной термостат(баню) на 3-5 мин для нагревания или охлаждения реагентов до определенной температуры (диапазон температур трех водяных бань 0°C - 80°C). Температура водяной бани контролируется по термометру;
-после стабилизации температуры растворов соли и кислоты в водяной бане (через 3-5 мин) их сливают и по секундомеру определяют t - время протекания реакции, а температуру реакции t(°C)принимают равной температуре водяной бани.
- результаты измерений и расчетов заносят в таблицу 2;
- по экспериментальным точкам строят график v=f(Т), из которого определяют температурный коэффициент реакции g;
|
|
|
- по экспериментальным точкам строят график ln v=f(1/Т), из которого определяют энергию активации реакции Еа
Таблица 2
| № | t | T= t+273 | 1/T | (1/T)·103 | t | v = 1 / t | ln v | v ·102 |
| °C | K | K-1 | K-1 | c | с-1 | - | с-1 | |
| 1 | ||||||||
| 2 | ||||||||
| 3 | ||||||||
| 4 |
Пример заполнения данными табл.2
| № | t | T | 1/T | (1/T)·103 | t | v = 1 / t | ln v | v ·102 |
| оC | K | K-1 | K-1 | c | с-1 | - | с-1 | |
| 3 | 40 | 313 | 0,003195 | 3,20 | 33 | 0,03030 | -3,50 | 3,03 |
Пример построения графиков по данным табл.2

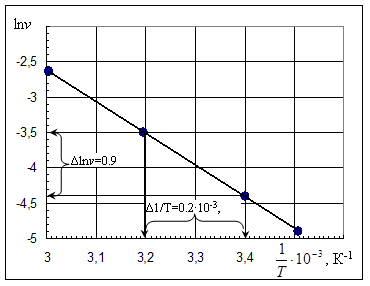 3.Расчетно-графическая часть
3.Расчетно-графическая часть
Нахождение температурного коэффициента реакции γ: (среднее из 3-х значений γ i).
Например,из графика v=f(Т) для V40 и V30 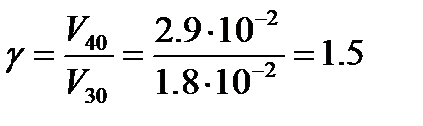 . Также находят γ для V30 / V20 и V50 / V40, а затем γ, как среднее из 3-х найденных значений.
. Также находят γ для V30 / V20 и V50 / V40, а затем γ, как среднее из 3-х найденных значений.
Нахождение энергии активации Еа: 
Например, из графика ln v=f(1/Т)
lnv2 = - 4,4, lnv1 = - 3,5; 1/Т2 = 3,4∙10-3, 1/Т1 = 3,2∙10-3
Еа = 8,314 ∙│-4,4 – (-3,5)│/│3.4 – 3,2│∙10-3 =8,314 ∙ 0.9/0.2∙10-3 = 37900 Дж/моль ≈ 38кДж/моль
Энергия активации: 38 кДж/моль
На основании полученных результатов делают выводы согласно цели проведенной работы.
ПРИМЕР ОФОРМЛЕНИЯ ОТЧЕТА (что должен содержать отчет)
ОТЧЕТ
по лабораторной работе
Дата добавления: 2021-02-10; просмотров: 115; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
