Центральные (стволовые) анестезии в челюстно-лицевой хирургии
Бугорный (туберальный) способ крылонёбной анестезии. Путь, идущий вдоль бугра задней поверхности верхней челюсти и через крылонёбную ямку к круглому отверстию, был впервые предложен американским хирургом Матасом (Маtas R.) в 1900 г. Его сообщение, напечатанное в малоизвестном журнале, прошло незамеченным. В практику этот способ ввел Браун (1909), давший простое и ясное описание. Методика Матас-Брауна, при которой игла подводится к круглому отверстию, чревата серьезными осложнениями, в первую очередь, возможностью попадания конца иглы в верхнюю глазничную щель и повреждения кавернозного синуса или попадания близко к зрительному отверстию и повреждения зрительного нерва. В 1929 г. С.Н. Вайсблат усовершенствовал бугорный путь крылонёбной анестезии, подводя конец иглы не к круглому отверстию, а только в крылонёбную ямку.
Глазничный путь. Доступ через глазницу предложил в 1909 г. В.Ф. Войно-Ясенецкий, его применяли и другие авторы (Нartel, Рауr, Сhevrier). В отличие от указанных авторов В.Ф. Войно-Ясенецкий предложил вводить иглу не по нижней стенке орбиты, а по наружной, считая этот путь менее опасным и более доступным для попадания концом иглы в круглое отверстие. С.Н. Вайсблат (1930) усовершенствовал глазничный путь, предлагая вводить иглу через нижний край глазницы на несколько миллиметров медиальнее от его середины. При проведении иглы по дну глазницы анестетик через нижнюю глазничную щель проникает в крылонёбную ямку, что достаточно для обезболивания верхнечелюстного нерва. В 1956 г. С.Н. Вайсблат предложил использовать путь через глазницу также и для обезболивания нижнечелюстного нерва у овального отверстия. Для этого иглу по нижнему краю глазницы вблизи ее нижненаружного угла проводят через нижнеглазничную щель в подвисочную ямку и далее "в контакте с наружной пластинкой крыловидного отростка" - к овальному отверстию.
На возможность доступа к проксимальному отделу верхнечелюстного нерва через крылонёбный канал первым указал В.Ф. Войно-Ясенецкий в 1915 г. Однако он не испытал этого пути на больном, считая его неприемлемым ввиду невозможности при нем проникнуть концом иглы в круглое отверстие. Путь через большое нёбное отверстие и крылонёбный канал был предложен и применен на больном в 1921 г. Карреа (Саrrеа), а в 1924 г. разработан и внедрен С.Н. Вайсблатом. Он, в частности, предложил погружать иглу в канал не на 4-5 см, а на 2,5-3 см. Не продвигая иглу до круглого отверстия, а вводя обезболивающий раствор только в крылонёбную ямку, автору удавалось обезболивать всю верхнюю челюсть с меньшим риском серьезных осложнений (поломка иглы, попадание в орбиту и ранение глазного яблока или зрительного нерва). К 1954 г. С.Н. Вайсблат располагал опытом 1397 случаев успешного проведения крылонёбной анестезии нёбным путем.
|
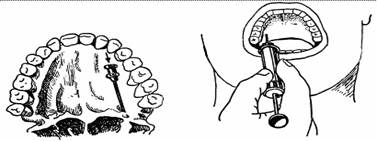
| Нёбный путь крылонёбной анестезии (начало инъекции). Конец иглы попадает в большое нёбное отверстие |
| Нёбный путь крылонёбной анестезий (конец инъекции). Конец иглы в крылонёбном канале |
Одним из наименее сложных доступов к проксимальным отделам верхне- и нижнечелюстного нервов является поперечный или подскуловой (подскулокрыловидный, по С.Н. Вайсблату), когда после вкола непосредственно под нижним краем скуловой дуги игла направляется перпендикулярно к поверхности щеки через вырезку нижней челюсти по направлению к основанию наружной пластинки крыловидного отростка. Позади этой пластинки, у ее основания, находится овальное отверстие и, следовательно, выходящий из него нижнечелюстной нерв, впереди, в той же плоскости - вход в крылонёбную ямку. На этом основании путь, который раньше использовали для обезболивания только нижнечелюстного нерва (Braun, 1907; Offerhaus, Sicher), С.Н. Вайсблат в 1941 г. предложил и для обезболивания верхнечелюстного нерва . При разработке поперечного доступа в крылонёбную ямку необходимо было уточнить место вкола иглы и глубину ее продвижения. По исследованиям С.Н. Вайсблата (1934) проекция середины ширины наружной пластинки крыловидного отростка на кожу под нижним краем скуловой дуги (ориентир Брауна) соответствует середине расстояния от основания козелка ушной раковины до нижненаружного угла глазницы (траго-орбитальная линия).
|
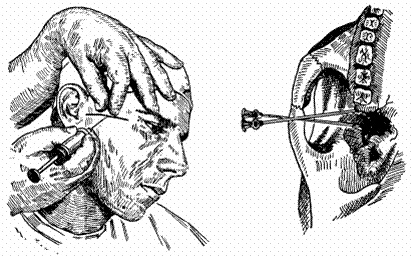
| Подскулокрыловидный путь крылонёбной анестезии (Ил. по С.Н. Вайсблату, 1962) |
| Положение иглы при крылонёбной анестезии подскулокрыловидным путем: а - конец иглы упирается в наружную пластинку крыловидного отростка; б - конец иглы находится в крылонёбной ямке |
А.В. Вишневский (1932) описал следующий метод обезболивания по способу ползучего инфильтрата при операциях на головном мозге и резекции челюстей: "Под скуловой дугой, приблизительно по середине, делают вкол длинной иглой, которую направляют слегка кверху и кпереди. При постепенном продвигании иглы в глубину сюда вводят 40-50 мл раствора". Способ рассчитан на пропитывание обезболивающим раствором тканей в подвисочной ямке, откуда он должен диффундировать в крылонёбную ямку и воздействовать на проксимальный отдел верхнечелюстного нерва и крылонёбный узел. Одновременно раствор распространяется к овальному отверстию и вызывает выключение нижнечелюстного и ушного нервов.
М.Д. Дубов (1959) после изучения на препарате черепа предложил видоизменить способ А.В. Вишневского, делая вкол не по середине скуловой дуги, а под основанием височного отростка скуловой кости. Если после этого продвинуть иглу медиальнее, кверху и несколько кпереди, то на глубине 3,5-4 см кончик иглы достигнет наружной поверхности большого крыла клиновидной кости под подвисочным гребнем, который отделяет височную поверхность большого крыла от подвисочной. Тем самым, по мнению М.Д. Дубова, был упрощен и сделан более доступным способ А.В. Вишневского.
|
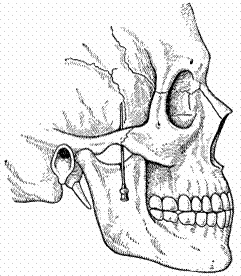
| Место укола и направление иглы при обезболивании по способу А.В. Вишневского - М.Д. Дубова |
Lindemann в 1926 г. предложил надскуловой путь для обезболивания верхне- и нижнечелюстного нервов в случае недоступности подскулового пути и через нижний край нижней челюсти. Прокалывая кожу у верхнего края скуловой дуги, он достигает подвисочного гребешка на глубине приблизительно 2 см. Отклоняя иглу назад и обходя гребешок, он скользит ею по кости, проходит еще 3-3,25 см, пока не почувствует сопротивления наружной пластинки крыловидного отростка или угловой ости большого крыла основной кости, spina angularis, и тут находит нижнечелюстной нерв. С.Н. Вайсблат в 1955г. усовершенствовал надскуловой путь крылонёбной анестезии по Пайру (1920) и у овального отверстия по Линдеману. Место вкола: по середине траго-орбитальной линии по верхнему краю скуловой дуги. Иглу проводят также во фронтальной плоскости, но с небольшим наклоном книзу, до упора в поверхность наружной пластинки крыловидного отростка. Дальнейшая техника как при подскуловом доступе.Основными достоинствами такой анестезии являются удаленность места вкола иглы от патологического очага в челюсти, уменьшение возможности образования гематомы, при необходимости одновременного обезболивания обоих нервов (например, у пострадавших, раненных в лицо) можно успешно провести обе центральные анестезии.
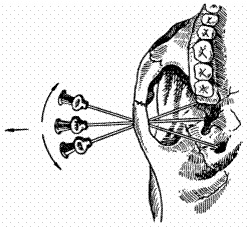
| Положение и направление иглы при крылонёбной анестезии (по Пайру - Вайсблату) и анестезии у овального отверстия (по Линдеману - Вайсблату) надскуловым путем: а - конец иглы упирается в наружную пластинку крыловидного отростка; б - конец иглы находится у овального отверстия; в - конец иглы находится в крылонёбной ямке |
Внутрикостная анестезия
В стоматологии внутрикостное введение анестезирующих веществ для удалении зубов и других операций известно с конца XIX века. Впервые внутрикостная (спонгиозная) анестезия была применена в 1891 г. норвежцем Otte. Он вводил местный анестетик в кость через отверстие в кортикальной пластинке, сделанное бором.
Английские и американские исследователи отдают первенство своим соотечественникам А.С. Раrrot (1910) и G.N. Hein (1906). Было предложено несколько методов перфорации кортикальной пластинки челюсти с целью введения анестетика в губчатую ткань кости: бормашиной и шаровидным бором (Оttе, 1891; Дитерихс М.М., 1907), бормашиной и дрильбором (Ing, 1907; Lilienthal В., 1975), инъекционной иглой (Поллак Н.А., 1936; Вайсблат С.Н., 1962), шиловидным граненым инструментом (Петрикас А.Ж., 1974), инъекционной иглой и бормашиной (Бережной В.П., 1977; Конобевцев О.Ф., Макиенко М.А., Бережной В.П., 1979). Так, Н.А. Поллак успешно провел 81 тыс. операций удаления зубов, вводя внутрикостно 2% раствор новокаина с адреналином в количестве 1,0-1,5 мл возле удаляемого зуба. Он дал высокую оценку данному методу обезболивания при удалении зубов, указывая на простоту выполнения и немедленное наступление анестезии. Однако этот метод обезболивания не получил распространения.
С 1973 г. Б.Н. Ланкин произвел удаление 870 зубов и корней у 630 больных в возрасте от 14 до 75 лет. Уколы 2% раствором новокаина без адреналина автор производил шприцем "Рекорд" с обычной инъекционной иглой в сосочки десны с медиальной и дистальной сторон удаляемого зуба. У 18 больных анестезия была неполной из-за значительного сопротивления кости продвижению иглы.
Детальное изучение механизма дентальной внутрикостной анестезии было проведено А.Ж. Петрикасом (1974,1983,1997), который на основании результатов клинических, гистологических и рентгенологических исследований сформулировал представление о механизме действия внутрикостной анестезии, что нашло подтверждение в результатах последующих работ других авторов. Один из путей состоит в диффузии раствора в костной ткани, окружающей лунку зуба: по костномозговым пространствам межзубной перегородки и периапикальной области. Второй путь состоит в проникновении раствора в сосудистое русло.
В последующие годы вновь, но не очень активно вернулись к внутрикостной анестезии с помощью специально разработанных сверл-игл для внутрикостных вливаний В.П. Бережной (1978), а в дальнейшем R. Landrean (1984), А.Villette (1984), предложившие коммерческие их варианты.
Недавно внутрикостная анестезия вновь обрела популярность среди стоматологов США благодаря внедрению системы для местной анестезии Stabident (Fairfax, Мiami, Fla). Она состоит из перфоратора, твердой иглы, которая перфорирует кортикальную пластинку кости с помощью обычного низкоскоростного углового наконечника, и иглы 27 размера длиной 8 мм, которая вводится в предварительно сделанное отверстие для инъекции анестетика (Маламед С., 1998).
Интралигаментарная анестезия
Способу интралигаментарной анестезии около века. Его разработка в 1907 г. связана с именем французского дантиста D. No g ue. Американский анестезиолог S. Malamed датой рождения анестезии считает 1904 год. Своим вторым рождением способ обязан совершенствованиям инструментального обеспечения местного обезболивания, а точнее, изобретению Lafargue (1965 г.) инъектора, создающего во время анестезии достаточно высокое давление (35-70 кг/см 3 ) для продвижения раствора в ткани пародонта. Его аппарат состоял из насоса с ножным приводом, который нагнетал раствор местного анестетика под давлением в периодонтальную щель. За рубежом интралигаментарная анестезия получила широкое распространение в 80-е годы, в России - в 90-е
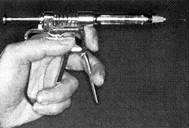
|
| Современный инъектор для интралигаментарной анестезии |
Этому способствовали возможности индустрии, позволившие внедрение в стоматологическую практику специальных шприцев и тонких канюль (Walton R.E., Abbot B.J., 1981; Evers H., 1981; Frenkel G., 1989; Lipp M.; 1992; Malamed S.F., 1997; Федосеева Т.Д., 1992; Столяренко П.Ю., Кравченко В.В., Киселева Т.А., Беланов Г.Н., 1998 и др.).
Значительному расширению возможностей внутрисвязочной анестезии должна способствовать компьютерная система WAND, обеспечивающая введение анестетика малым потоком, независимо от плотности тканей.
Местно-анестезирующие средства (от греч. anaesthesia — нечувствительность) — это лекарственные вещества временно подавляющие возбудимость окончаний чувствительных нервов и блокирующие проведение импульсов по нервным волокнам (проводникам), а также способные вызывать местную или регионарную потерю чувствительности. В отличие от общих анестетиков (средства для наркоза) они не вызывают потерю сознания.
Группа местно-анестезирующих средств объединяет различные классы органических веществ, большинство из них — азотистые соединения. Как уже было сказано выше, первым анестезирующим средством, примененным в медицинской практике, был кокаин. Анестезирующее действие кокаина обусловлено наличием в его молекуле азотсодержащего комплекса основного характера — экгонина и бензоильной группы. На этой основе были синтезированы анестезин, новокаин и большое число эфиров и амидов бензойной, парааминобензойной, парааминосалициловой, парааминонафтойной и других кислот. В настоящее время местные анестетики по химической структуре делят на две группы: сложные эфиры и сложные амиды кислот.
I. Сложные эфиры:
1. Новокаин. 2. Анестезин. 3. Дикаин.
II. Сложные (замещенные) амиды кислот:
1. Лидокаин. 2. Тримекаин. 3. Мепивакаин.
4. Прилокаин. 5. Бупивакаин. 6. Этидокаин.
7. Артикаин (ультракаин, септанест, убистезин и др.).
Важная характеристика анестетиков — длительность действия препарата, которая должна быть достаточной для выполнения различных стоматологических вмешательств, сопровождающихся болью.
В соответствии с продолжительностью действия все анестетики могут быть условно подразделены на три основные группы:
· с коротким периодом действия — новокаин;
· со средним периодом действия — лидокаин, артикаин;
· с продолжительным периодом действия — бупивакаин.
Фармакологическое действие анестезирующих средств обусловлено их строением — характер ароматического или гетероциклического ядра, длина и структура боковой цепи, радикалы при азоте боковой цепи — и физико-хими-ческими свойствами — растворимость, константа ионизации, коэффициент распределения, полярность, поверхностная и межфазная активность, влияние на мономолекулярные слои липидов и др. В механизме действия анестезирующих средств главную роль играет их влияние на процесс генерации возбуждения и проведение нервного импульса. Имеет значение также их способность проникать через различные биологические среды к нервным волокнам и в мембрану нервного волокна и адсорбироваться на их поверхности, их «поведение» в возбудимой мембране и взаимодействие со специфическими (в химическом отношении) структурами рецептора. Местом действия анестезирующих средств выступает возбудимая мембрана аксона. Анестезирующие средства проникают в мембрану, изменяя при этом ориентацию ее белковых и липидных молекул. В действии анестезирующих средств принимают участие обе формы его молекул — катион и неионизированное основание. Анестезирующее средство фиксируется в мембране благодаря взаимодействию катиона с полярными группами фосфолипидов и фосфопротеидов и в результате гидрофобных взаимодействий неионизированного основания. При этом анестезируещее средство вступает в конкурентное взаимодействие с ионами кальция, имеющими важное значение в механизме транспорта ионов. Проникновение молекул анестезирующих средств в возбудимую мембрану и включение их в структуры ее белков и липидов вызывает нарушение обмена ионов натрия и калия. Реакции между катионом анестезирующего средства и анионными структурами рецептора вызывают инактивацию системы перемещения ионов натрия. Происходящие в мембране реакции перемещения подразумевают временное образование комплексов анестезирующих средств с различными биохимическими системами мембраны. Вмешательство анестезирующих средств в метаболизм мембраны вызывает дефицит энергии, в результате чего блокируется транспорт ионов, ответственный за генерацию и передачу нервного импульса по чувствительным нервным волокнам, падает электрическая активность мембраны без деполяризации.
Чувствительность нервных волокон к действию местных анестетиков тем выше, чем меньше их диаметр. По-видимому, это объясняется относительным увеличением поверхности волокна при уменьшении его диаметра. Поскольку информация с рецепторов различных видов чувствительности передается в центральную нервную систему по волокнам различного строения и диаметра, к действию местных анестетиков наиболее чувствительны безмиелиновые и тонкие миелиновые волокна. Поэтому под действием местных анестетиков сначала происходит утрата болевой, затем температурной, тактильной, проприоцептивной чувствительности, и только после этого наступает двигательный паралич.
Зная механизм действия анестетиков, можно сделать вывод, что латентное время распространения полной анестезии зависит и от фармако-химических свойств анестетика (прежде всего, от способности к активной диффузии), в какой-то мере от вводимого количества и его концентрации. Концентрация анестетика имеет существенное значение, хотя сведения по этому поводу достаточно противоречивы. С одной стороны, указывается, что при возрастании концентрации обезболивающий эффект препарата не усиливается (J.G. Travell, 1955), с другой, — что повышение концентрации удлиняет время обезболивания на 30 %.
Следует помнить, что на все эти параметры оказывает достаточно большое влияние организм пациента, с его индивидуальной толерантностью к данному фармакологическому средству, специфическими местными реакциями раздражения на общее болезненное повреждение (вкол иглы), общая и/или локальная гипертермия.
Важно помнить о том, что в воспаленных тканях среда кислая, pH обычно ниже 6,5–6 и такого гидролиза соли анестетика не происходит, анестетик в форме оснований не накапливается в достаточных количествах. Поэтому в воспаленных тканях их анестезирующий эффект обычно значительно ослаблен.
Местные анестетики группы сложных эфиров Анестетики группы сложных эфиров быстрее подвергаются гидролизу в тканях, поскольку эфирные связи нестойки. В крови гидролиз их ускоряется псевдохолинэстеразой. Анестетики этой группы действуют коротко. ДИКАИН. Синонимы: Amethocaine, Anethaine, Decicain, Felicain, Foncaine, Intercain, Medicain, Pantocain, Pontocaine hydrochloride, Rexocaine, Tetracaini hydrochloridum, Tetracaine hydrochloride и др. В связи с высокой токсичностью (в 10 раз токсичнее новокаина) препарат применяют только для аппликационной анестезии слизистой оболочки полости рта и носа. Целесообразно использовать 0,25 %-ный, 0,5 %-ный и 1 %-ный растворы. В отдельных случаях, чаще всего при анестезии небольших участков, можно применять 2–3 %-ные растворы дикаина. Высшая разовая доза препарата для взрослых 0,09 г (3 мл 3 %-ного раствора). Так как препарат легко всасывается и небольшое превышение терапевтической дозы может стать причиной тяжелой интоксикации и даже смертельного исхода, в детской стоматологии он не используется. АНЕСТЕЗИН. Синонимы: Бензокаин, Aethylis aminobenzoas, Anaesthalgin, Anaesthicin, Anaesthin, Benzocain, Ethoforme, Ethylis aminobenzoas, Ethyl aminobenzoate, Norcain, Parathesine, Rhaetocain, Topanalgin и др. Вещество не растворяется в воде. Может быть использован для поверхностной анестезии в виде присыпок или 5–20 %-ных масляных растворов. Для обезболивания раневых и язвенных поверхностей может применяться в виде 5–10 %-ной мази. Высшая доза для взрослых: разовая 0,5 г, суточная 1,5 г. НОВОКАИН. Синонимы: Aethocain, Allocaine, Ambocain, Aminocaine, Anesthocaine, Atoxicain, Cerocain, Chemocain, Citocain, Ethocaine, Genocaine, Herocaine, Isocain, Jenacain, Marecaine, Minocain, Naucain, Neocaine, Pancain, Paracaine, Planocaine, Polocainum, Procaine, Procaini hydrochloridum, Procaine hydrochloride, Protocaine, Sevicaine, Syncaine, Syntocain, Topocaine и др. По активности новокаин в 4–5 раз уступает дикаину. Для инфильтрационной анестезии применяются 0,25 %-ный, 0,5 %-ный и 1 %-ный растворы, а для проводниковой анестезии используют 1 %-ный и 2 %-ный растворы. Необходимо учитывать, что при одной и той же общей дозе препарата токсичность тем выше, чем больше концентрация применяемого раствора. Препарат обладает умеренными сосудорасширяющими свойствами. Высшая разовая доза для взрослых: при применении 0,25 %-ного раствора не более 500 мл (1,25 г); 0,5 %-ный раствор — 150 мл (0,75 г); 1 %-ный раствор — 75–100 мл (0,75 г) и 25–30 мл 2 %-ного раствора (0,5 г). Общая доза не должна превышать 2 г. При резорбтивном действии (действие лекарственных средств или токсичных веществ, проявляющееся после всасывания их в кровь) новокаина отмечается угнетение центральной нервной системы, умеренное болеутоляющее, противошоковое действие. Препарат оказывает ганглиоблокирующий, сосудорасширяющий, противоаритмический эффект, улучшает микроциркуляцию. Новокаин малотоксичен, но часто вызывает аллергические реакции (стоматиты, дерматиты, отек Квинке и даже анафилактический шок). При повышенной чувствительности к новокаину у пациента наблюдается головокружение, слабость, падение кровяного давления, коллапс, шок. Поэтому при сборе анамнеза следует обращать внимание на переносимость пациентом не только новокаина, но и других анестетиков близких к новокаину по структуре (анестезина и дикаина), поскольку к ним может быть перекрестная аллергия. Новокаин снижает активность сульфаниламидных препаратов, так как один из его метаболитов — парааминобензойная кислота, а противомикробное действие сульфаниламидов основано на конкурентном антагонизме с парааминобензойной кислотой. ^ Местные анестетики группы сложных амидов Местные анестетики группы амидов медленнее инактивируются в организме, не разрушаются холинестеразой крови, действуют более длительно, следовательно более эффективны. Главное их достоинство — то, что они лучше диффундируют в ткани на месте инъекции, действуют быстрее, обладают большей зоной анестезии и более прочным взаимодействием с тканями, что препятствует поступлению местного анестетика в ток крови. ЛИДОКАИН. Синонимы: Ксикаин, Ксилокаин, Лидестин, Acetoxyline, Alocaine, Anestacon, Anestecain, Astracaine, Dolicaine, Dulcicaine, Esracaine, Fastocaine, Leostesin, Lidestin, Lidocaine, Lidocard, Lidocaton, Lignocain, Maricain, Nulicaine, Octocaine, Remicaine, Solcain, Stericaine, Xycain, Xylesin, Xylocain, Xylocard, Xylocitin, Xyloton, Xylotox и др. Лидокаин — первый амидный анестетик примененный в стоматологии, он в четыре раза эффективнее новокаина и приблизительно в два раза токсичнее, оказывает более глубокое и продолжительное анестезирующее действие, чем новокаин. Это позволило ему, в 50-е годы, стать одним из самых популярных анестетиков, используемых в стоматологии. По химической структуре лидокаин относится к производным ацетанилида. В отличие от новокаина он не является сложным эфиром, медленнее метаболизируется в организме и действует более продолжительно, чем новокаин. В связи с тем, что при его метаболизме в организме не происходит образования парааминобензойной кислоты, он не оказывает антисульфаниламидного действия и может, в отличие от новокаина, применяться у больных, получающих сульфаниламидные препараты. Наряду с местноанестезирующей активностью лидокаин обладает выраженными антиаритмическими свойствами. Лидокаин — сильное местноанестезирующее средство, вызывающее все виды местной анестезии: терминальную, инфильтрационную, проводниковую и считается родоначальником всех амидных препаратов. По сравнению с новокаином он действует быстрее, сильнее и продолжительнее. Относительная токсичность лидокаина зависит от концентрации раствора. В малых концентрациях (0,5 %) он существенно не отличается по токсичности от новокаина; с увеличением концентрации (1 % и 2 %) токсичность повышается (на 40–50 %). Для инфильтрационной и проводниковой анестезии в стоматологии используется 2 %-ный раствор анестетика, а для терминальной (аппликационной) анестезии слизистой оболочки полости рта — 10 %-ный аэрозольный раствор выпускаемый за рубежом (лидестин), в хирургии аэрозоль применяется при смене повязок, вскрытии абсцессов и т. п. Аэрозольный баллон содержит 750 доз по 10 мг лидокаина. Количество распыленного препарата зависит от поверхности, подлежащей обезболиванию. У взрослых не следует превышать дозу 200 мг, т. е. 20 распылений; у детей старше 2 лет назначают однократно 1–2 дозы препарата. Не следует допускать попадания аэрозоля в глаза. Лидокаин, применяемый в дозах не вызывающих судорог, обладает седативным эффектом. Препарат противопоказан пациентам с тяжелой патологией печени. Высшая разовая доза для взрослых — 2 % раствора до 20 мл. При быстром поступлении препарата в ток крови, могут наблюдаться понижение АД и коллапс; уменьшение гипотензивного эффекта достигается введением сосудосуживающих средств. Противопоказания для использования лидокаина следующие: синдром слабости синусового узла у больных пожилого возраста;
· выраженная брадикардия;
· кардиогенный шок;
· выраженные нарушения печени;
· повышенная чувствительность к препарату.
Беременным и кормящим женщинам лидокаин следует назначать по строгим показаниям. У детей до 2-х лет разрешается применение аэрозоля лидокаина только после его предварительного нанесения на ватный тампон. В случае передозировки наблюдаются психомоторное возбуждение, тремор, клонико-тонические судороги, коллапс, угнетение ЦНС. Для лечения этого осложнения применяют барбитураты короткого действия, транквилизаторы бензодиазепинового ряда. При одновременном назначении лидокаина и бета-адреноблокаторов (препаратов применяемых при пароксизмальной тахикардии, экстрасистолиях, стенокардии, гипертонической болезни — индерал, тразикоркор) резорбтивные эффекты (в том числе, токсические) лидокаина могут усиливаться в связи с ослаблением его инактивации в печени. Дозу препарата в этом случае снижают. Нерационально назначать лидокаин одновременно с антиаритмическими средствами — препаратами, применяемыми для лечения пароксизмальной тахикардии, мерцательной аритмии и экстрасистолии (аймалином, хинидином и др.) в связи с усилением кардиодепрессивного действия. Совместное применение с новокаинамидом (антиаритмическое средство) может вызвать возбуждение ЦНС и галлюцинации. Противопоказано также совместное введение лидокаина с ингибиторами МАО (антидепрессанты, например, ипразид), полимиксин В (антибиотик применяется при стафило-, стрепто-, пневмо-, гоно- и менингококковой инфекции), дифенином (противосудорожное средство применяемое для лечения эпилепсии). Хранение: препарат следует хранить в защищенном от света месте при комнатной температуре. МЕПИВАКАИН. Синонимы: Scandicain, Scandonest, Carbocain, Isocain, Mepivastesin, Mepicaton, Mepidont. Используется для инфильтрационной и проводниковой анестезии в виде 3 %-ного раствора, 2 %-ного раствора с адреналином (1/100000) и норадреналином (1/100000). По эффективности и токсичности 2 %-ный раствор мепивакаина приблизительно равен 2 %-ному раствору лидокаина (препарат не вызывает перекрестной аллергической реакции с эфирными анестетиками). В отличие от большинства активных веществ анестезирующих растворов, которые обладают сосудорасширяющими свойствами, мепивакаин имеет сосудосуживающее действие, что позволяет использовать раствор с пониженным содержанием вазоконстриктора. В связи с этим 3 %-ный раствор мепивакаина гидрохлорида в терапевтической стоматологии сегодня — препарат выбора для пациентов, которым противопоказано применения вазоконстрикторов. Противопоказания для использования мепивакаина следующие:
· аллергия на местные анестетики, принадлежащие к этой же группе;
· миастения тяжелой степени;
· низкий уровень содержания холинэстеразы в плазме;
· серьезные нарушения печени: цирроз, наследственная или приобретенная порфирия.
Максимальная однократная доза препарата составляет 2,7 мг на 1 кг массы тела или 162 мг (3 карпулы) при весе 60 кг. Для детей общая доза не должна превышать 1 карпулу и составляет 1,33 мг на 1 кг массы тела. При передозировке, в результате интоксикации нервной системы появляются клонические судороги. АРТИКАИН. Синонимы: ультракаин, картикаин, септонест, убистезин и т. д. Препарат для местной анестезии в стоматологии. Артикаин — местный анестетик амидного типа тиафеновой группы. Препарат обеспечивает надежный анестезирующий эффект. Заживление раны, после проведенных хирургических вмешательств, протекает без осложнений, что обусловлено хорошей тканевой переносимостью и минимальным сосудосуживающим действием. Вследствие низкого содержания адреналина в препаратах артикаина его влияние на сердечно-сосудистую систему выражено мало: почти не отмечается повышения АД и увеличения ЧСС. Препараты артикаина обладают низкой токсичностью. Однако, выпускаемые различными фирмами под разными торговыми названиями препараты артикаина в той или иной мере отличаются друг от друга по составу: ^ Ультракаин Д-С — в 1 мл препарата содержится: артикаина гидрохлорида 40 мг, адреналина гидрохлорида 6 мкг. Прочие ингредиенты: натрия метабисульфит, натрия хлорид, вода для инъекций. ^ Ультракаин Д-С Форте — в 1 мл препарата содержится: артикаина гидрохлорида 40 мг, адреналина гидрохлорида 12 мкг. Прочие ингредиенты: натрия метабисульфит, натрия хлорид, вода для инъекций. ^ Убистезин Форте — в 1 мл препарата содержится: артикаина гидрохлорида 40 мг, адреналина гидрохлорида 12 мкг. Прочие ингредиенты: натрия метабисульфит, натрия хлорид, вода для инъекций Септанест — в 1 мл препарата содержится: артикаина гидрохлорида 40 мг, адреналина гидрохлорида 10 мкг. ^ Прочие ингредиенты: натрия метабисульфит, натрия хлорид, ЭДТА, вода для инъекций Артикаин действует быстрее лидокаина, действие препарата начинается уже через 1–3 мин., продолжительность анестезии составляет 60–180 мин. Обладает высокой диффузной способностью и степенью связывания с белками плазмы (95 %), низкой жирорастворимостью. Артикаин хорошо проникает в ткани, может обеспечить обезболивание неба после щечной инфильтрационной анестезии и обезболивание пульпы после инфильтрационной анестезии на нижней челюсти от 35 до 45. Липофильность артикаина меньше, чем у других амидных анестетиков, однако низкая токсичность в сравнении с лидокаином и мепивакаином позволяет использовать этот препарат в виде 4 %-ного раствора артикаина гидрохлорида с адреналином (эпинефрином) в разведениях 1:100000 и 1:200000. В связи с тем, что препараты артикаина не содержат, как правило, парабена (антибактериального консерванта), эти анестетики могут быть использованы пациентам, подверженным аллергии на парагидроксибензоаты или на химически родственные структуры. Стабильность анестетика достигается высоким качеством упаковки (ампул и карпул) и высокой химической чистотой активного вещества. Однако, следует помнить, что «Ультракаин», выпускаемый во флаконах по 20 мл, содержит 0,05 мг метилпарабена. Максимальная разовая доза раствора препарата составляет 12,5 мл (7 карпул) для взрослого с массой тела 70 кг (7,0 мг/кг артикаина). При использовании препаратов артикаина возможны следующие побочные эффекты:
1. Со стороны центральной нервной системы: в зависимости от примененной дозы описаны случаи нарушения сознания вплоть до его потери; нарушения дыхания; мышечный тремор, непроизвольные подергивания мышц, иногда прогрессирующие вплоть до генерализованных судорог; тошнота, рвота.
2. Со стороны органов зрения: помутнение в глазах, преходящая слепота, диплопия (редко).
3. Со стороны сердечно-сосудистой системы: умеренно выраженные нарушения гемодинамики, проявляющиеся снижением АД, тахикардией или брадикардией.
4. Аллергические реакции: отек или воспаление в месте инъекции; в других областях — покраснение кожи, зуд, конъюнктивит, ринит, ангионевротический отек различной степени выраженности (включая отек верхней и/или нижней губы и/или щек, голосовой щели с затруднением глотания, крапивницу, затруднение дыхания). Все эти явления могут прогрессировать до развития анафилактического шока.
5. Местные реакции: отек или воспаление в месте инъекции.
6. Прочие: головные боли (связанные, вероятно, с наличием в составе препарата адреналина). Другие побочные явления, обусловленные действием адреналина (тахикардия, аритмия, повышение АД), проявляются редко, так как концентрация адреналина незначительна.
7. Лекарственное взаимодействие: гипертензивный эффект симпатомиметических аминов типа адреналина может быть усилен трициклическими антидепрессантами и ингибиторами МАО. Взаимодействия подобного типа описаны для адреналина и норадреналина при использовании их в качестве вазоконстрикторов в концентрациях 1:25000 и 1:80000 соответственно. Хотя концентрация адреналина в препаратах артикаина значительно ниже, следует тем не менее учитывать такую возможность. Иногда случайная внутрисосудистая инъекция может привести к развитию ишемических зон в месте введения препарата, в отдельных случаях прогрессирующих до тканевого некроза. Повреждения лицевого нерва, вплоть до развития паралича лицевого нерва, возникают только при нарушении техники инъекции. Абсолютные противопоказания:
· введение детям до 4-х лет;
· недавно перенесенный инфаркт миокарда;
· пароксизмальная тахикардия и другие тахиаритмии;
· неконтролируемое повышение артериального давления;
· закрытоугольная глаукома;
· не контролируемый препаратами гипертиреоз;
· не контролируемый препаратами сахарный диабет;
· бронхиальная астма, лечение которой проводится кортикостероидами;
· феохромоцитома (опухоль надпочечников);
· аллергические реакции на сульфиты или вспомогательные компоненты анестетика.
Говоря об аллергических реакциях на препараты артикаина, следует отметить, что аллергия на адреналин невозможна, т. к. он является гормоном, который вырабатывается у каждого человека. Что касается артикаина, то согласно данным литературы документально не зафиксировано случаев аллергической реакции на препарат в чистом виде. ^ Относительные противопоказания:
· одновременный прием трициклических антидепрессантов, ингибиторов МАО, ß-адреноблокаторов, кокаина.
Особые указания Препарат нельзя вводить внутривенно, не рекомендуется проводить инъекцию в область воспаления. Ввиду содержания сульфитов, у некоторых пациентов возможны развития острого приступа удушья, нарушение сознания, шок. У больных бронхиальной астмой риск развития этого осложнения очень высок. Беременным также показано щадящее применение данных препаратов, так как имеются данные о небольшом проникновении их через плаценту. В грудное молоко растворы артикаина не проникают в значительном количестве в связи с чем применяются во время лактации. При проведении инфильтрационной и проводниковой анестезии в стоматологии у больных с заболеваниями сердечно-сосудистой системы (хроническая сердечная недостаточность, патология коронарных сосудов, стенокардия, нарушения ритма, инфаркт миокарда в анамнезе, артериальная гипертония), цереброваскулярными расстройствами, с наличием паралича в анамнезе, хроническим бронхитом, эмфиземой, сахарным диабетом, гипертериозом, а также при наличии выраженного беспокойства целесообразно использовать препараты артикаина с низким содержанием адреналина, каковым выступает ультракаин Д-С (содержание адреналина 6 мкг в 1 мл). В специальных тестах не было выявлено отчетливого влияния препарата на операторскую деятельность. Однако в связи с тем, что предоперационное беспокойство больного и стресс, обусловленный оперативным вмешательством, могут оказывать влияние на эффективность деятельности, врач-стоматолог должен в каждом конкретном случае индивидуально решать вопрос о допуске пациента к управлению транспортным средством или к работе с механизмами. ^ Сравнительная характеристика местных анестетиков
Применение местных анестетиков в рекомендованных дозах — сравнительно безопасно (за исключением аллергических реакций). Статистика осложнений и побочных явлений при проведении местной анестезии не очень точна и связана скорее с погрешностью выбора препарата и его дозировке. Практика использования местных анестетиков должна учитывать индивидуальную максимальную дозу применяемых препаратов. Обычно она определяется в соответствии с массой тела пациента. Стоматолог должен всегда стремиться к достижению эффективного обезболивания, используя минимальное количество анестетика. Рекомендации, в этой связи, предлагают использовать дозу, не превышающую 50 % от максимального значения токсической дозы. · применялась ли ранее местная анестезия; · имелись ли осложнения местной анестезии; · имелись ли аллергические реакции на местные анестетики; · определить факторы риска (хронические заболевания).
|
Дата добавления: 2021-01-21; просмотров: 83; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
