Качественная реакция на галогенид-ионы
Свое название плавиковая кислота получила из-за уникального свойства взаимодействовать с оксидом кремния, входящим в состав стекла, как бы «плавить» его.
Эту реакцию используют для изготовления надписей и рисунков на стекле. На стекло наносят тонкий слой парафина, по которому процарапывают рисунок, а затем изделие погружают в раствор плавиковой кислоты. Таким образом, например, литовский художник М. Чюрленис создал около тридцати художественных произведений, хранящихся в музее его имени в г. Каунасе.
Галогены в природе.
 |
Галогены в природе существуют только в связанном состоянии. Среди них наиболее распространены хлор (0,19% от массы земной коры) и фтор (0,03% ).
Важнейшее природное соединение хлора — галит NaCl, с которым вы подробно знакомились в прошлом году. Его добывают путем разработки залежей каменной соли — твердого хлорида натрия.
Кроме галита, встречается природный хлорид калия KCl — минерал сильвин, сильвинит — смесь KCl и NaCl, состав которой отражают формулой KCl • NaCl.
Важнейший природный минерал фтора — это флюорит, или плавиковый шпат CaF2.
Бром и иод — рассеянные элементы, своих минералов они не образуют. Они концентрируются в водах океанов и морей, в водах буровых скважин, а также в водорослях.
Получение галогенов .
Фтор и хлор получают электролизом расплавов или растворов их солей. Например, процесс электролиза расплава хлорида натрия можно отразить уравнением:
|
|
|

Но если водород можно получить другими, более удобными и дешевыми способами, например из природного газа, то гидроксид натрия получают почти исключительно электролизом раствора поваренной соли, как и хлор.
Бром и иод получают в промышленности по реакции вытеснения их соответственно из бромидов и иодидов.
Биологическое значение галогенов. Их применение.
Вы не могли не обратить внимание, что на этикетках многих марок зубных паст указывается на содержание в них фтора — конечно, не свободного, а его соединений. Благодаря этому важному компоненту, участвующему в построении зубной эмали и костей, предотвращается такое заболевание, как кариес зубов. Кроме того, фтор является необходимым элементом в процессах обмена веществ в железах, мышцах и нервных клетках.
Важное значение имеет фтор и в промышленном производстве, где основные потребители его — ядерная промышленность и электротехника. Его соединение Nа3АlF6 используется для производства алюминия. А в быту все более широкое применение находит тефлоновая посуда, название которой дано по фторсодержащей пластмассе — тефлону.
Хлор — один из химических элементов, без которых немыслимо существование живых организмов. Основная форма его. поступления в организм — это хлорид натрия. Он стимулирует обмен веществ, рост волос, придает бодрость и силу. Больше всего NаСl содержится в плазме крови.
|
|
|
Особую роль в пищеварении играет соляная кислота НСl, которая входит в состав желудочного сока. Без 0,2%-ной НСl практически прекращается процесс переваривания пищи. И хотя почти все пищевые продукты содержат некоторое количество поваренной соли, человек вынужден добавлять к пище ежедневно около 20 г соли.
По масштабам промышленного применения хлор намного превосходит все галогены. Хлор и его соединения необходимы для отбеливания льняных и хлопчатобумажных тканей, бумаги и т. д. Особенно много его расходуется в органическом синтезе для производства пластмасс, каучуков, красителей и растворителей (рис. 20).
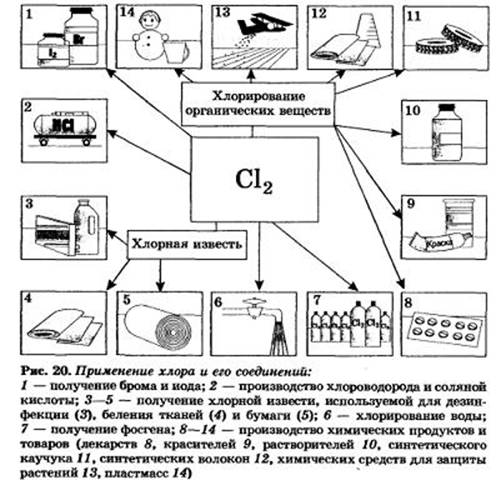
Многие хлорсодержащие соединения используют для борьбы с вредителями сельского хозяйства. В больших количествах хлор потребляется для обеззараживания питьевой воды, правда, далеко не без отрицательных последствий (какое вещество безопаснее применять для этой цели?). В цветной металлургии методом хлорирования руд извлекают из них некоторые металлы (титан, ниобий, тантал). Хлор нашел применение и в военных целях в качестве боевого отравляющего средства. Позднее он был заменен другими, более эффективными хлорсодержащими отравляющими веществами, например фосгеном СОСl2.
|
|
|
Хлор содержится в очень опасном для жизни и здоровья веществе — диоксине. Соединения хлора — одна из причин разрушения озонового слоя Земли.
Еще один галоген — бром также весьма важен для организма человека. Соединения этого элемента регулируют процессы возбуждения и торможения центральной нервной системы, поэтому для лечения нервных болезней (бессонницы, истерии, неврастении и т. д.) врачи прописывают «бром» — бромсодержащие препараты.
Бром активно накапливают некоторые растения, и в том числе морские водоросли. Именно в море сосредоточена большая часть брома на нашей планете, и море служит главным поставщиком брома. Подсчитано, что ежегодно вместе с морской водой в воздух переходит около 4 млн т брома. Понятно, что содержание его в воздухе приморских районов всегда больше, чем в районах, далеких от моря. Это одна из причин, почему так полезно дышать морским воздухом.
Не менее важную роль бром, а точнее, бромид серебра АgВr играет в фотографии. Те, кто занимается фотографией, вероятно, сразу же вспомнят названия сортов фотобумаги — «Унибром», «Бромпортрет» и др. Фотобумага содержит нанесенный на нее с помощью желатина слой бромида серебра, который легко разлагается под действием света:
|
|
|
2АgВr = 2Ag + Br2
И наконец, последний из рассматриваемых нами галогенов — иод — это тот элемент, без которого человек не может жить: недостаток его в воде и пище снижает выработку гормона щитовидной железы и приводит к заболеванию эндемическим зобом. Под регулирующим действием гормона щитовидной железы находятся мускульное возбуждение, биение сердца, аппетит, пищеварение, работа мозга и темперамент человека. Иод попадает в организм вместе с пищей: хлебом, яйцами, молоком, водой, морской капустой и с воздухом (особенно морским) при дыхании.
Спиртовой раствор иода (5—10% -ный), называемый йодной настойкой, применяется для обработки ран. Иод входит в состав многих лекарств.
Главными потребителями иода являются фармацевтичеcкая и химическая промышленность, а также производство светочувствительных фотоматериалов.
Дата добавления: 2021-01-20; просмотров: 119; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
