Ответ: выпадает осадок и выделяется газ
КОНЦЕНТРАЦИИ РАСТВОРОВ
Масса декагидрата сульфата натрия, необходимого для приготовления 1000 г раствора сульфата натрия с массовой долей растворенного вещества 7,1%, составляет ____ г (с точностью до целого значения).
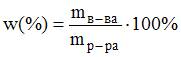
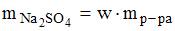
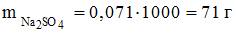
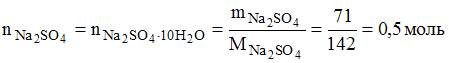
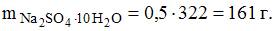
Объем 90%-ной серной кислоты (r = 1,815 г/см3), необходимый для приготовления 10 л раствора с молярной концентрацией эквивалентов 0,1 моль/л, равен ____ мл (с точностью до целого значения).
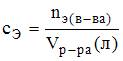
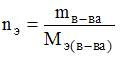
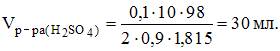
Навеску сульфата меди массой 80г разбавили водой до 500мл раствора
Молярная концентрация эквивалентов - 2 мол/л
Масса гидроксида натрия в растворе, если 4г оксида натрия прореагировало со 100мл воды. Ответ – 5,12 г
Массовая доля гидроксида натрия в растворе, полученном при растворении 4,0 г оксида в 100 см3 воды, равна _5____ %
Масса NaOH, если смешали 80г 2,5%-ного раствора и 120 г 5%-ного раствора. Ответ - 8г
Найти мольную долю метанола в воде, если к 1.6г метанола добавили 2.7г
Воды. Ответ -25
Мольная доля ацетона в растворе , полученном при смешении 11,6 г ацетона и 32,4 г воды, составляет __10%
100г 40%-ного раствора гидроксида натрия разбавили водой до 500мл
Найти молярную концентрацию эквивалентов. Ответ –2 моль/л
Объем 0.1молярного раствора КОН для нейтрализации 0,126г азотной кислоты. Ответ- 20 мл
Масса сульфата магния, которую необходимо растворить в 500 см3 воды для получения раствора с моляльной концентрацией 0,5 моль/кг, составляет ___ г (с точностью до целого значения). 30 г
|
|
|
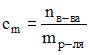
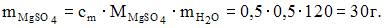
Масса осадка, полученного при взаимодействии растворов 20 мл 0.1- молярного раствора хлорида бария и 15 мл 0.2 –молярного раствора серной кислоты.
Ответ – 0.466
Масса азотной кислоты , содержащаяся в 5мл раствора , рН которого
равна 3
Ответ – 0.315
Объем 0.1молярного раствора КОН для нейтрализации 0,126г азотной кислоты. Ответ- 20 мл
Гидролиз солей ,рН
Формула соли, значение рН водного раствора которой практически равно 7, имеет вид 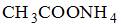
Концентрация ионов гидроксидных групп в растворе NaOH, если рН =10.
Ответ – 10-4
рН щелочного раствора, полученного растворением 1.2 г гидроксида натрия в 500мл воды. Ответ- 12
Значение рН раствора , полученного при смешении равных объемов 0,02 М раствора гидроксида натрия и 0,02 М раствора серной кислоты (α = 1), равно …
При смешении данных растворов происходит реакция
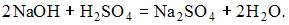
Избыточная концентрация серной кислоты равная 0,01 М, в результате увеличения объема уменьшится в 2 раза и станет равной 0.05 моль
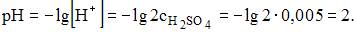
рН 0.05 молярного раствора серной кислоты, разбавленного в 10 раз
Ответ- 2
Продукт гидролиза хлорида алюминия, хлорида железа по второй стадии:
|
|
|
Ответ – Al(OH)2Cl, Fe(OH)2Cl
Метиловый оранжевый имеет желтый цвет в растворе :
Na 3 PO 4
При сливании водных растворов FeCl 3 и K 2 S наблюдаются следующие явления:
Ответ: выпадает осадок и выделяется газ
При гидролизе Cr 2 S 3 , Al 2 S 3 Al 2 ( CO 3 ) 3 наблюдаются следующие явления:
Ответ: выпадает осадок и выделяется газ
Масса уксусной кислоты, содержащаяся в 5 л ее раствора, значение рН которого равно 3,9, ___ 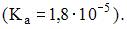 составляет _ 0,264г
составляет _ 0,264г
Растворы неэлектролитов
Водный раствор неэлектролита замерзает при –1,86°С. Концентрация вещества в растворе составляет ____ моль/кг 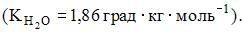
Молярная масса неэлектролита, раствор 60 г которого в 1000 г воды кипит при 101,04оС , 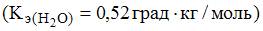 равна __30_____ г/моль.
равна __30_____ г/моль.
Соотношение температур кипения растворов глюкозы и сахарозы с одинаковой массовой долей растворенного вещества, равной 1%, подчиняется выражению …
Соотношение значений осмотического давления растворов глюкозы и сахарозы при 25оС с одинаковой массовой долей растворенного вещества, равной 0,1%, подчиняется выражению 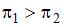 …
…
чем больше молярная масса растворенного вещества, тем меньше величина . 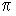 .Т.К. Молярная масса глюкозы меньше, то
.Т.К. Молярная масса глюкозы меньше, то 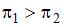
|
|
|
Соотношение между температурами кипения растворов этанола и метанола в воде с одинаковой массовой долей растворенного вещества, равной 0,2 %, определяется выражением …
Для соотношения значений осмотического давления растворов метанола 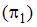 и этанола
и этанола 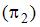 в воде при 20оС с одинаковой массовой долей растворенного вещества, равной 0,05 %, справедливо выражение …
в воде при 20оС с одинаковой массовой долей растворенного вещества, равной 0,05 %, справедливо выражение … 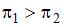
Согласно закону Вант-Гоффа 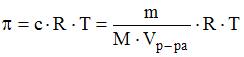
чем больше молярная масса растворенного вещества, тем меньше величина . 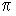 .Т.К. Молярная масса метанола меньше, то
.Т.К. Молярная масса метанола меньше, то 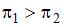
Если осмотическое давление раствора 4,6 г неэлектролита в 400 см3 воды при температуре25 0С составляет 619 кПа, то молярная масса растворенного вещества равна ______ г/моль (с точностью до целого числа; R = 8,31Дж/(моль∙К)).
Согласно закону Вант-Гоффа
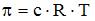
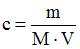
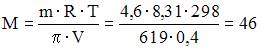 г/моль
г/моль
Давление пара над раствором, содержащим 16 г метанола в 81 г воды, если давление пара над чистой водой при той же температуре составляет 110,0 кПа, равно ____99___ кПа (с точностью до целого числа)
Согласно закону Рауля 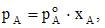 с учетом формулы
с учетом формулы 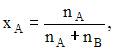
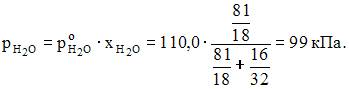
Масса воды, в которой необходимо растворить 60 г гидроксида натрия, чтобы полученный раствор кристаллизовался при -4,650С, составляет __960_ г (с точностью до целого числа; α = 0,60; ).
|
|
|
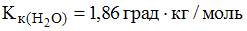
Согласно закону криоскопии (Рауля) для растворов электролитов
и формуле 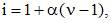 масса воды будет равна
масса воды будет равна 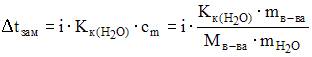
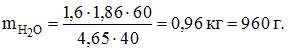
Степень диссоциации нитрата аммония в растворе, содержащем 12,0 г соли в 500 г воды, температура замерзания которого равна -,составляет 90%______ % (с точностью до целого числа; 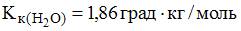 ).
).
Согласно закону криоскопии (Рауля) для растворов электролитов 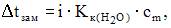
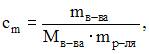
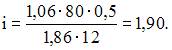
Тогда, согласно формуле 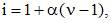
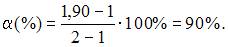
Дата добавления: 2021-01-20; просмотров: 353; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
