Витамин В6 (пиридоксин, антидерматитный)
Впервые витамин Вб был выделен в 1938 г. из дрожжей и печени и вскоре после этого был синтезирован химически. Он оказался производным 3-оксиниридина, в частности 2-метил-3-окси-4,5-диоксиметилгшридина. Термином «Витамин В6», по рекомендациям Международной комиссии по номенклатуре биологической химии, обозначают все три производных 3-оксипиридина, обладающие одинаковой витаминной активностью: пиридоксин (пиридоксол), пиридоксаль и пиридоксамин:

Оказалось, что хотя все три производных 3-оксипиридина наделены витаминными свойствами, коферментные функции выполняют только фосфорилированные производные пиридоксаля и пиридоксамина.
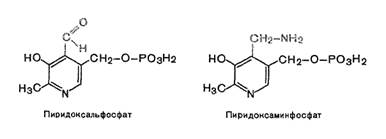
Фосфорилирование пиридокеаля и пиридоксамина является ферментативной реакцией, протекающей при участии специфических киназ. Синтез пиридоксальфосфата, например, катализирует пиридоксалькиназа, которая наиболее активна в ткани мозга. Эту реакцию можно представить следующим уравнением:
Пиридоксаль + АТФ -> Пиридоксальфосфат + АДФ
Кроме того, доказано, что в животных тканях происходят взаимопревращения пиридоксальфосфата и пиридоксаминфосфата, в частности в реакциях трансаминиро-вания аминокислот.
Биотин (витамин Н)
Биотин был впервые выделен в 1935 г. из яичного желтка. Молекула биотина является циклическим производным мочевины, а боковая цепь представлена валериановой кислотой: 
Карбонильная группа биотина связывается с е-аминогруппой лизина, образуя е-N-биотиниллизин (б и о ц и т и н), обладающий биологической активностью.
|
|
|
Известные к настоящему времени биотиновые ферменты (т. е. содержащие в качестве кофермента биотин) катализируют два типа реакций:
1) реакции карбоксилирования (с участием СО2 или HCOJ), сопряженные с распадом АТФ

2) реакции транскарбоксилирования (протекающие без участия АТФ), при которых субстраты обмениваются карбоксильной группой:
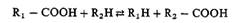
Получены доказательства двухстадийного механизма этих реакций с образованием промежуточного комплекса (карбоксибиотинилфермента).
К реакциям первого типа относятся, например, ацетил-КоА и пируваткарбокси-лазные реакции:
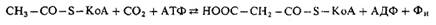
Пируваткарбоксилаза является высокоспецифичиым ферментом, катализирующим уникальную реакцию усвоения СО2 в организме животных. Сущность реакции сводится к пополнению запасов оксалоацетата (щавелевоуксуеная кислота) в лимоннокислом цикле Кребса (так называемые «анаплеротические», «пополняющие» реакции), т. е. его синтезу из СО, пирувата:

Реакция протекает в две стадии: на первой стадии, связанной с затратой энергии, СО2 подвергается активированию, т. е. ковалентному связыванию с биотином в активном центре фермента (Е-биотин):
|
|
|
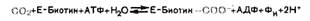
На второй стадии СО2 из комплекса переносится на пируват с образованием оксалоацетата и освобождением фермента:

Примером второго типа реакций является метилмалонил-оксалоацетат-транс-карбоксилазная реакция, катализирующая обратимое превращение пировиноградной и щавелевоуксусной кислот:
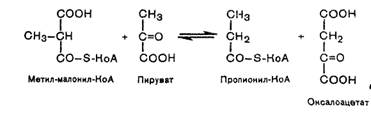
Реакции карбоксилирования и транскарбоксилирования имеют важное значение в организме при синтезе высших жирных кислот, белков, пуриновых нуклеотидов (соответственно нуклеиновых кислот) и др.
Фолиевая кислота
Фолиевая кислта состоит из трех структурных единиц: остатка птеридина (I), парааминобензойной (II) и L-глутаминовой ' (III) кислот, имеет следующую структуру:
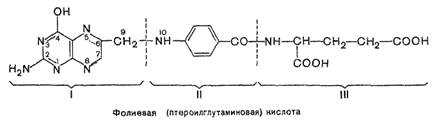
Коферментные функции фолиевой кислоты связаны не со свободной формой витамина, а с восстановленным его птеридиновым производным. Восстановление сводится к разрыву двух двойных связей и присоединению четырех водородных атомов в положениях 5, 6, 7 и 8 с образованием тетрагидро-фолиевой кислоты (ТГФК); оно протекает в две стадии в животных тканях при участии специфических ферментов, содержащих восстановленный НАДФ. На первой стадии при участии фолатредуктазы образуется дигидрофолиевая кислота (ДГФК), которая при участии второго фермента — дигидрофолатредуктазы - восстанавливайся в ТГФК:
|
|
|

Доказано, что коферментные функции ТГФК непосредственно связаны с переносом одноуглеродных групп, первичными источниками которых в организме являются Р-углеродный атом серина, сс-углеродный атом глицина, углерод метильных групп ме-тионина, холина, 2-й углеродный атом индольного кольца триптофана, 2-й углеродный атом имидазольного кольца гистидина, а также формальдегид, муравьиная кислота и метанол. К настоящему времени открыто шесть одноуглеродных групп, включающихся в разнообразные биохимические превращения в составе ТГФК: формальная ( — СНО), метильная ( —СН3), метиленовая ( —СН2 —), метенильная ( —СН = ), оксиметильная ( —СН2ОН) и формиминогруппа ( —CH = NH). Выяснено, что присоединение этих фрагментов к ТГФК является ферментативной реакцией ковалентного связывания их с 5-м или 10-м атомом азота (или с обоими атомами вместе). В качестве примера приводятся отдельные функциональные группы в активных участках ТГФК:

Имеются данные, что производные ТГФК участвуют в переносе одноуглеродных фрагментов при биосинтезе метионииа и тимина (перенос метильной группы), серина (перенос оксиметильной группы), образовании пуриновых нуклеотидов (перенос формильной группы) и т. д. . Поскольку перечисленные вещества играют исключительно важную роль в биосинтезе белков и нуклеиновых кислот, становятся понятными те глубокие нарушения обмена, которые наблюдаются при недостаточности фолиевой кислоты.
|
|
|
Дата добавления: 2020-12-12; просмотров: 176; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
