Классификация хроматографических методов анализа
Тема:ХРОМАТОГРАФИЧЕСКИЙ МЕТОД АНАЛИА
· Сущность метода
Хроматографические методы анализа основаны на цикличных актах сорбции‑десорбции, происходящих между подвижной фазой (элюентом) с растворенной пробой и неподвижным сорбентом. Компоненты сложных смесей имеют различную сорбируемость, и проходя вдоль неподвижной фазы, поглощаются с неодинаковой скоростью и в разном количестве. Последующее изучение результатов и их сравнение с эталоном позволяет установить точный состав реактива.
В традиционном методе в качестве неподвижной фазы используется материал с развитой поверхностью, а элюентом выступает поток инертного газа или жидкости. Фильтрация элюента через слой сорбента запускает многократное повторение сорбции и десорбции, что и отличает хроматографические методы анализа от других аналитических методик и обуславливает их эффективность.
· Основные понятия хроматографии
Хроматография – это процесс, который базируется на многократном повторении актов сорбции и десорбции вещества при перемещении ее в потоке подвижной фазы вдоль неподвижного сорбента.
Сорбция – процесс поглощения твердым веществом или жидкостью (сорбентом) газообразного или растворенного вещества (сорбата), обратный процесс называется десорбцией.
Сорбцию разделяют на:
-адсорбция – поглощение вещества (адсорбата) поверхностью твердого или жидкого адсорбента;
|
|
|
-абсорбция – поглощение вещества (абсорбата) всем веществом абсорбента;
-хемосорбция (химическая сорбция) – поглощение вещества сорбентом с образованием химических соединений.
Вещество подвижной фазы непрерывно поступает в контакт с новыми участками сорбента и частично сорбируется, а сорбированное вещество контактирует со свежими порциями подвижной фазы и частично десорбируется.
Подвижной фазой может служить жидкость или газ, протекающие под давлением через слой неподвижной фазы.
Элюент — это газ или жидкость, применяемые в качестве подвижной фазы в хроматографической системе, которые протекатют через неподвижную фазу
Элюирование — извлечение вещества из твердого носителя вымыванием его подходящим растворителем (
Неподвижная фаза (сорбент) представляет собой твёрдое пористое вещество с развитой поверхностью или плёнку жидкости, нанесённую на поверхность твёрдого инертного носителя.
При хроматографировании вещество поступает в слой сорбента вместе с потоком подвижной фазы. При этом вещество сорбируется, а затем при контакте со свежими порциями подвижной фазы – десорбируется.
Перемещение подвижной фазы происходит непрерывно, поэтому непрерывно происходит сорбция и десорбция вещества. При этом часть вещества находится в неподвижной фазе в сорбированном состоянии, а часть – в подвижной фазе и перемещается вместе с ней. В результате скорость движения вещества оказывается меньше, чем скорость движения подвижной фазы.
|
|
|
Чем сильнее сорбируется вещество, тем медленнее оно перемещается. Если хроматографируется смесь веществ, то скорость перемещения каждого из них различна из-за разного сродства к сорбенту, в результате чего вещества разделяются: одни компоненты задерживаются в начале пути, другие продвинутся дальше.
Хроматография впервые была введена в аналитическую практику русским ботаником М.С. Цветом (1903 г) В первых же работах с помощью этого метода М.С. Цвет установил, что считавшийся однородным зеленый пигмент растений хлорофилл на самом деле состоит из нескольких веществ. При пропускании экстракта зеленого листа через колонку, заполненную порошком мела, и промывании петролейным эфиром он получил несколько окрашенных зон, что, несомненно, говорило о наличии в экстракте нескольких веществ. Впоследствии это было подтверждено другими исследователями. Этот метод он назвал хроматографией, хотя сам же указал на возможность разделения и бесцветных веществ.
|
|
|

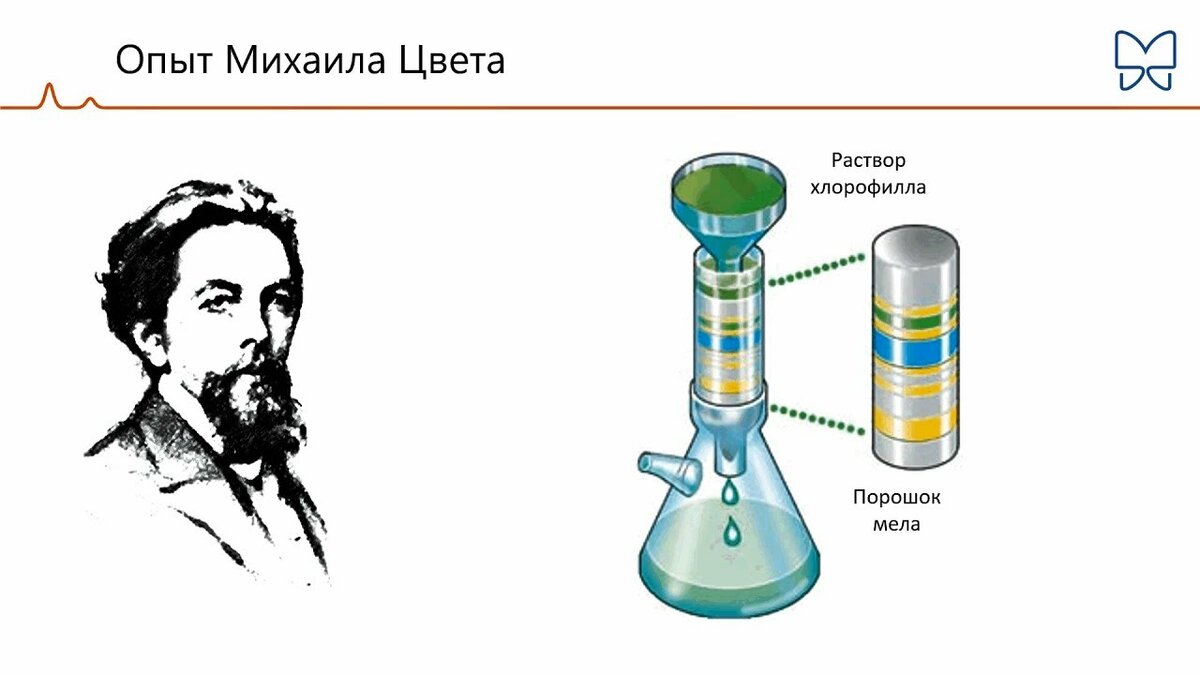
Рисунок 1- Опыт М.С.Цвета
Классификация хроматографических методов анализа
· По агрегатному состоянию фаз хроматографические методы анализа делятся на:
-газожидкостные. Подвижной фазой служит поток инертного газа, который проходит через жидкий сорбент.
-газоадсорбционные. Проба в газообразном состоянии пропускается через твердое вещество, на поверхности которого осуществляется адсорбция.
-жидкостно‑жидкостные. В качестве элюента и неподвижной фазы используются жидкие среды.
-жидкостно‑адсорбционные. Реагент подается вместе с растворителем и проходит через твердый пористый материал.
-жидкостно‑гелевые. В этом методе неподвижная фаза представлена гелеобразным веществом.
· По конструкции хроматографического оборудования.
-колоночная хроматография- адсорбция осуществляется в колонках, заполненных неподвижной фазой.
-плоскостная хроматография, в которой используется тонкий срез сорбента или специальная бумага.
-капиллярная хроматография- разделение происходит в пленке жидкости
- хроматография в полях, требующая для проведения анализа создания дополнительных магнитных, центробежных или иных сил.
|
|
|
· По механизмам разделения хроматография делится на:
-адсорбционную — основывается на разнице в адсорбируемости компонентов пробы;
-распределительную — протекает за счет различной растворимости веществ в фазах;
-ионообменную — осуществляется благодаря достижению констант ионообменного равновесия;
-проникающую — строится на разнице в формах и размерах молекул;
-осадочную — происходит благодаря осаждению нерастворимых соединений;
-адсорбционно‑комплексообразовательную — выполняется за счет образования на поверхности неподвижной фазы координационных соединений разной прочности.
· по способам перемещения поглощаемых компонентов вдоль адсорбционного слоя:
-проявительный (или элюентный) метод.
-фронтальный и вытеснительный метод.
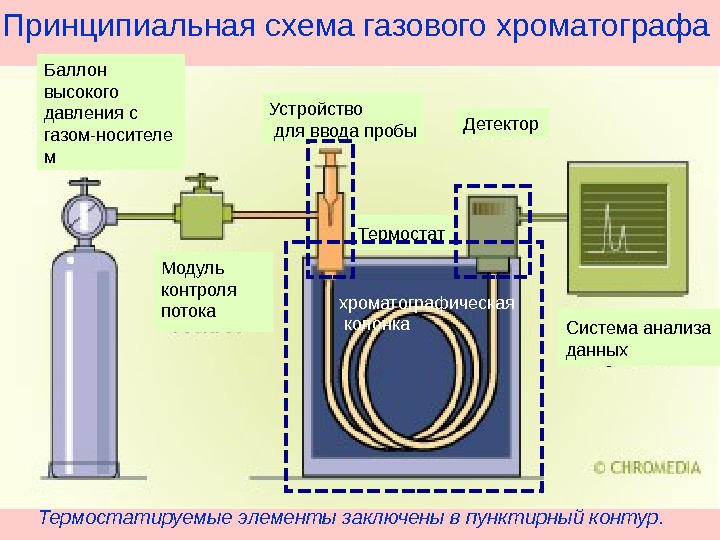

Рисунок 2-хроматограф
Большинство методов хроматографии выполняется на сложных приборах-хроматографах.
Рассмотрим один из методов
1. Ионообменная хроматография.
Метод ионообменной хроматографии основан на использовании явления ионного обмена между неподвижной твердой фазой ‒ ионообменником (сорбентом) и подвижной жидкой фазой ‒ раствором, содержащим ионы, обмениваемые с ионами сорбента.
Ионный обмен ‒ это гетерогенный процесс, при котором сорбент и находящийся с ним в контакте раствор обратимо и стехиометрически обменивается одноименно (одного и того же знака) заряженными ионами.
В качестве сорбентов используют ионообменники ‒ иониты, представляющие собой обычно нерастворимые в воде твердые фазы. Иониты состоят из матрицы, в которой распределены ионогенные группы, включающие фиксированные, прочно связанные в матрице, ионы, и менее прочно связанные противоионы (т. е. ионы противоположного знака), способные к отщеплению от ионита и к переходу в раствор. Эти противоионы могут обмениваться с одноименными (катионы ‒ с катионами, анионы ‒ с анионами) ионами раствора.
Иониты, обменивающиеся катионами раствора, называются катионитами (катионообменниками), а иониты, обменивающиеся анионами раствора, ‒ анионитами (анионообменниками).
Известны также амфотерные иониты (амфолиты), способные обмениваться с раствором как катионами, так и анионами.
По химическому составу иониты бывают неорганические (например, алюмосиликаты, силикаты, Al(OH)3 и органические (продукты химической переработки угля или лигнина*, а также полученные синтетическим путем ионообменные смолы).
По происхождению иониты разделяют также на естественные и искусственные. В практике чаще применяют искусственные иониты, к которым и принадлежат сульфированные угли (сульфоуголь) и ионообменные смолы.
Катиониты - сорбенты, способные к обмену катионами. Содержат в своем составе
Ионогенные группы, раличной кислотности, например, группу – SO3H, карбоксильную группу –СООН, ион водорода которых способен к катионному обмену.
Химическую формулу катионитов схематично изображают
RSO 3 H или [ R ] H
RSO 3 Na или [ R ] Na ,
где R (матрица) -сложный органический радикал
Наиболее часто применяют сильнокислотные катиониты марок КУ-1,КУ-2,СДВ-2
КУ-2 –сульфированный сополимер стирола и дивинилбензола
Схема катионного обмена:
[ R ] H + Ме+ = [ R ] Ме + Н+
Например:
RSO 3 H + К NO 3 = RSO 3 К + Н+
Аниониты - сорбенты, способные к обмену анионами
Содержат в своем составе
Основные ионогенные группы, например, аминогруппы различной степени замещения:
-NH2, =NH, -NH2OH, и др.
Химическую формулу анионитов схематично изображают
R NH 3 OH или [ R ] OH
RNH 3 Cl или [ R ] Cl
Схема анионного обмена:
[ R ] OH + А+ = [ R ]А + OH -
Применяют аниониты марок АВ-17, АН-1, ЭДЭ-10 и др.
Кроме ионитов, обладающих кислотно-основными свойствами, известны также сорбенты, проявляющие окислительно-восстановительные и комплексообразующие свойства.
В ионообменной хроматографии ионный обмен проводят в хроматографических колонках.
Хроматографи́ческая коло́нка — устройство для хроматографии, используемое как для работы ручным методом, так и в составе специального агрегата, хроматографа.
Для работы ручным методом колонки представляют собой стеклянные трубки с краном в нижней части (иногда ‒ это обычные стеклянные бюретки). Колонки заполняют заранее приготовленным ионитом в той или иной форме и заливают дистиллированной водой (или раствором) так, чтобы верхний уровень жидкости всегда находился на 1‒1,5 см выше уровня ионита. В нижнюю часть колонки перед ее заполнением ионитом помещают стеклянную вату.


Хроматографические колонки
Перед анализом ионообменную колонку регенерируют, т.е. переводят ионит в определенную ионообменную форму.
Зарядка катионита Н+ ионами, а анионита ОН- ионами проводят путем пропускания через колонку определенного количества кислоты или основания. Затем ионит отмывают водой от избытка кислоты или щелочи (по индикатору) и пропускают через него с определенной скоростью анализируемый раствор.
Колонку промывают водой или другим элюентом, собирая элюат целиком или по фракциям.
Определение содержания анализируемого компонента завершают различными методами: титриметрическим, потенциометрическим, спектровотометрическим и другими
· Качественный и количественный анализ
Хроматографические методы анализа устанавливают качественный и количественный состав вещества.
При качественных испытаниях на хроматографах пробу идентифицируют по ее хроматограмме, сравнивая полученные параметры с эталонными значениями, хранящимися в библиотеке данных.
Количественный метод анализа строится на измерении пиков, формирующихся в зависимости от концентрации примесей. Лаборант изучает хроматограмму одним из следующих методов:
-метод абсолютной градуировки. Зависимость параметров пика от концентрации разных веществ определяется экспериментально. Затем составляются графики и таблицы, с которыми в последующем и сравнивается хроматограмма. Благодаря простоте и высокой точности, метод является основным для выявления микропримесей.
-метод внутренней нормализации. Сумма выбранных пиковых параметров (например, их высота или площадь) принимается за 100%. Далее рассчитывается отношение высоты отдельного изучаемого пика к суммарному значению, благодаря чему определяется массовая доля конкретного компонента в пробе.
-метод внутреннего стандарта. В смесь вводится стандартное вещество, для которого заранее известен калибровочный график. Затем пики изучаемых компонентов сравниваются с пиками «стандарта». Метод применяют в случае исследования составов с переменным, но известным количеством анализируемых компонентов.
Дата добавления: 2020-11-29; просмотров: 628; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
