Защита неметаллическими плёнками.
КОРРОЗИЯ МЕТАЛЛОВ. СПОСОБЫ БОРЬБЫ С НЕЙ

Коррозией называется разрушение металла вследствие химического или электрохимического воздействия на него внешней среды.
Коррозия – это неотвратимая потеря металлов, это большие убытки, поэтому борьба с коррозией – важнейшая задача для промышленности и вообще техники.
Коррозия чёрных металлов называется ржавлением, ежегодно до 10 % выработанного железа расходуется на замену проржавевшего.
В зависимости от воздействия среды различают:
Атмосферную коррозию.

жидкостную коррозию.


газовую коррозию.

По месту распределения коррозия бывает:
равномерная,
местная
межкристаллитная.

Теория коррозии
Коррозия начинается с поверхности на границе двух фаз – «металл»-«внешняя среда» и с течением времени распространяется вглубь.
По характеру физико-химических процессов, происходящих между металлом и внешней средой, различают два вида коррозии: химическую и электрохимическую.
Химическая коррозия
возникает в результате химического воздействия внешней среды на поверхность металла, например, образование слоя окислов (окалина) на металле в печах при высоких температурах, например, при отпуске.

При разных температурах образуется на поверхности металла тонкая плёнка окисла, толщина которой увеличивается с ростом температуры.
От толщины плёнки окисла и, значит, от ее оптических свойств зависит её цвет:
|
|
|
при 220 оС – жёлтый,
255 оС – коричневый,
300 оС – тёмно-синий,
330 оС – серый,
это так называемые «цвета побежалости», по ним определяют температуру отпуска.
Электрохимическая коррозия – возникает при действии на металл электролитов. Это наиболее распространённый вид коррозии.


Большинство металлических конструкций находится в соприкосновении с воздухом, водой и землёй – мосты, крыши зданий, механизмы (подъёмные краны), кабели, трубопроводы и так далее.
В воздухе и земле всегда есть влага – роса, дождь, водяные пары, грунтовые воды и так далее.
На конструкциях всегда есть грязь, в воздухе – SO2, SO3, NO2, NO3, СО, которые растворяясь в воде, диссоциируют на положительные и отрицательные ионы – а это электролит, который и вызывает электрохимическую коррозию (ЭХК).
Коррозия металлов и сплавов в электролите аналогична работе гальванического элемента.
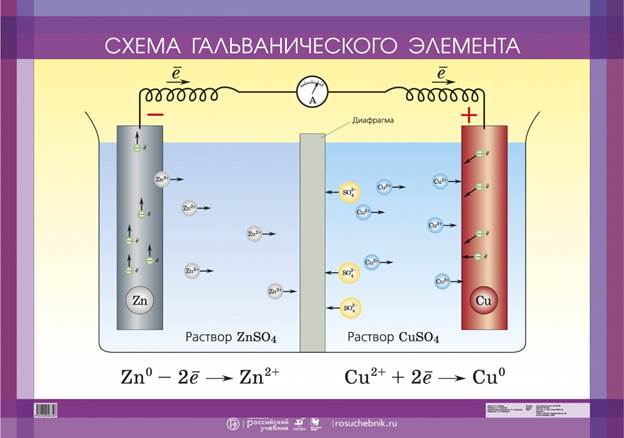
Металлы и сплавы по химическому составу неоднородны и различаются также по структуре составляющих их частей: твёрдый раствор, химическое соединение, механическая смесь.
Эти структурные составляющие имеют различные электродные потенциалы, обусловленные их химической и физической природой.
|
|
|
Когда сплав находится в электролите, одни участки, имеющие низкий электродный потенциал, становятся анодами (что значит «подъём») и разрушаются, так как их ионы переходят в раствор электролита и становятся солями при высыхании воды.
Другие участки, обладающие более высоким электродным потенциалом, становятся – катодами (это значит «путь вниз») и сохраняются неизменными, так как на них ионы Н+ нейтрализуются и образуется Н2.
Так как анодных и катодных участков в сплаве очень много, то сплав можно рассматривать состоящим из большого числа электродов, то есть как многоэлектродный микроэлемент. Когда два микроэлемента находятся в контакте (болтовое соединение (например, чугунный фланец и стальной болт), склёпанные листы и др.), то образуется макроэлемент.
Методы защиты от коррозии
1. Защита легированием –

при легировании стали хромом или хромом и никелем (более эффективно) сталь способна сопротивляться коррозии, так как её электродный потенциал становится высоким и она является отрицательно заряженным катодом.
Дорогостоящий никель частично заменяют более дешевым марганцем.
Хрома должно быть не менее 12 %, иначе сталь становится положительно заряженным анодом (на нержавеющей посуде стоит знак «18/10», это значит, в металле 10 % Ni и 18 % Cr).
|
|
|

Защита неметаллическими плёнками.
Это окисные плёнки, получаемые оксидированием и фосфатные плёнки, получаемые фосфатированием.

Детали обрабатывают либо сильным окислителем (едким натром NаОН), либо смесями фосфорной кислоты и её солей, в результате детали покрываются окисной плёнкой чёрно-синего цвета (воронение), либо фосфатной плёнкой.


3. Защита металлическими покрытиями.
На поверхность детали наносится тонкий слой другого металла, в зависимости от того, какой металл наносится, процесс называется:
– Zn – цинкование,
Al – алитирование,
Sn – лужение,
Pb – свинцевание,
Cr – хромирование,
Cd – кадмирование,
Ni – никелирование,
Cu – меднение,
также покрывают металл латунью и бронзой.
Способы нанесения металла на деталь:
· погружением детали в расплавленный металл, применяется для нанесения пленок из плавящихся при низких температурах металлов (цинка, олова, свинца) – используется в случае деталей сравнительно небольшого размера;

· путём распыления расплавленного металла (цинка, кадмия) сжатым воздухом с набрызгиванием его на деталь – для крупных деталей;
|
|
|


· диффузионным методом – алитирование, хромирование (см. выше, ХТО).

· гальваническим путём – электролиз водных растворов солей того металла, который является покрытием. Преимущества метода: управляемость процессом, экономное расходование металла, отсутствие нагрева. Различают анодное и катодное покрытие.
– анодное (цинком) – у цинка электродный потенциал ниже, чем у железа, поэтому он защищает и механически, и электрохимически, так как он является анодом (+) и разрушается;
– катодное (оловом) – электродный потенциал олова выше, чем у железа, то защищает только механически, а в случае повреждения плёнки электрохимическим путём разрушается железо.
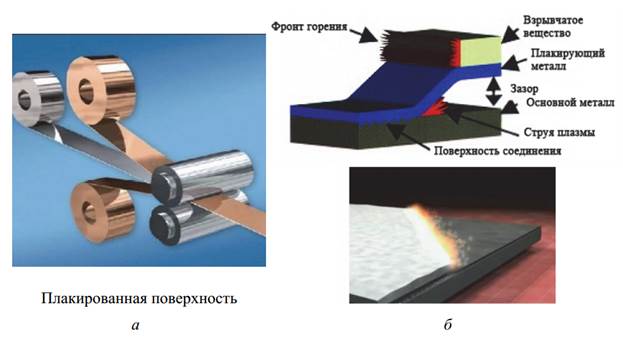
· методом плакирования – термин происходит от французского слова «плаке», что значит накладывать, покрывать – горячей прокаткой или прессованием покрывают один металл тонким слоем другого металла – например, сталь латунью, дюралюмин – алюминием.
4. Защита протекторами – от латинского защищающий – к детали, находящейся в электролите (в почве всегда есть вода) присоединяют металл с меньшим электродным потенциалом (обычно цинк), который, являясь анодом, и разрушается. Деталь является катодом и не корродирует.
5. Защита неметаллическими покрытиями. Это краски, лаки – они дешёвы, экономят цветные металлы, защищают любые конструкции. Недостаток – трескаются и пропускают воду. Применяются краски масляные и эмалевые.
6. Защита обработкой коррозионной среды.
Есть вещества, замедляющие химические реакции и даже прекращающие их (их называют ингибиторами).
Когда такой ингибитор вводят в коррозионную среду (например, в воду радиаторов двигателей внутреннего сгорания, теплообменников, компрессоров), то коррозия практически прекращается.
Достоинство – ингибитора требуется обычно мало, так как он, сдерживая реакцию, сам в ней не участвует (как и катализатор, который ускоряет химическую реакцию, также не участвуя в ней).
Задание для самостоятельной работы:
Проработать вышеизложенный материал и подготовить ответы на контрольные вопросы:
Дата добавления: 2020-11-29; просмотров: 191; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
