Мыла – натриевые или калиевые соли высших карбоновых кислот. Натриевые соли высших карбоновых кислот имеют твердое агрегатное состояние, а калиевые – жидкое (жидкое мыло).
ПКД-11 Химия
Тема. Жиры. Соли карбоновых кислот. Мыла.
Для тех, кто пожелал участвовать в олимпиадах по химии и биологии, нужно поторопиться! Пройти олимпиаду в разделе «Школьные инфоконкурсы» можно только до 23.10.2020
Тема урока
Сложные эфиры — это вещества, которые образуются в результате взаимодействия органических или кислородсодержащих неорганических кислот со спиртами (реакции этерификации).
Общая формула сложных эфиров одноатомных спиртов и одноосновных карбоновых кислот:

Сложные эфиры в природе.
Запись в тетради.
Сложные эфиры – функциональные производные карбоновых кислот, в молекулах которых гидроксильная группа (-ОН) замещена на остаток спирта (-OR)
Сложные эфиры карбоновых кислот – соединения с общей формулой
R–COOR', где R и R' – углеводородные радикалы.
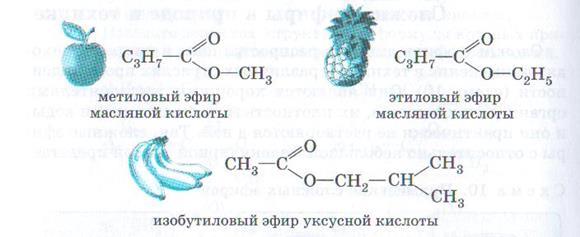
Сложные эфиры – жидкости, обладающие приятными фруктовыми запахами. В воде они растворяются очень мало, но хорошо растворимы в спиртах. Сложные эфиры очень распространены в природе. Их наличием обусловлены приятные запахи цветов и фруктов. Они даже могут находиться в коре некоторых деревьев.

Эфиры высших одноосновных кислот и высших одноатомных спиртов – основа природных восков. Воски не растворяются в воде. Их можно формовать в нагретом состоянии. Примерами животных восков могут служить пчелиный воск, а также ворвань (спермацет), содержащийся в черепной коробке кашалота (кашалотовый воск). Пчелиный воск содержит сложный эфир пальмитиновой кислоты и мирицилового спирта (мирицилпальмитат): CH3(CH2)14–CO–O–(CH2)29CH3.
Физические свойства сложных эфиров.
Запись в тетради.
Физические свойства сложных эфиров:
· Летучие, бесцветные жидкости
· Плохо растворимы в воде
· Чаще с приятным запахом
· Легче воды
Название сложных эфиров.
Краткие названия сложных эфиров строятся по названию радикала (R') в остатке спирта и названию группы RCOO- в остатке кислоты.
Например, этиловый эфир уксусной кислоты CH3COOC2H5 называется этилацетат.
Получение сложных эфиров.
Cложные эфиры могут быть получены при взаимодействии карбоновых кислот со спиртами (реакция этерификации). Катализаторами являются минеральные кислоты.
Реакция этерификации.

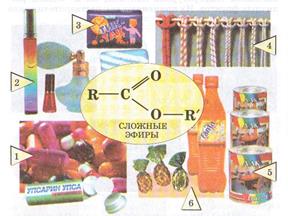
6. Применение сложных эфиров:
1) лекарственные средства; 2,3)парфюмерия и косметика; 4) синтетические и искусственные волокна; 5) лаки; 6) производство напитков и кондитерских изделий.
ЖИРЫ
1. Важнейшими представителями природных сложных эфиров являются жиры.



2.Классификация жиров:
1) твердые – это жиры, в состав которых входят предельные карбоновые кислоты. Это жиры животного происхождения (говяжий, свиной, бараний и т.д.), исключение составляет рыбий жир;
2) жидкие – это жиры, в состав которых входят непредельные карбоновые кислоты. Это жиры растительного происхождения, или масла (подсолнечное масло, соевое масло, рапсовое масло и т.д.), исключение составляет пальмовое масло.
3.. Химические свойства жиров:
А). Жиры нерастворимы в воде, но хорошо растворимы в органических растворителях – бензоле, гексане;
Б). Гидрированием жидких жиров получают твердые сложные эфиры. Именно эта реакция лежит в основе получения из растительного масла твердого жира – маргарин.

В). Жиры подвергаются гидролизу.
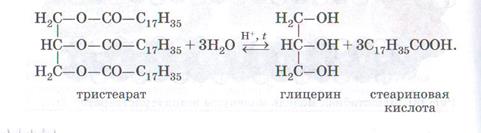
Г). Если проводить гидролиз жиров в щелочной среде, то произойдет омыление жиров.
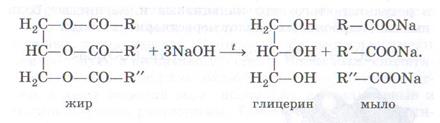
Что такое мыла?
Мыла – натриевые или калиевые соли высших карбоновых кислот. Натриевые соли высших карбоновых кислот имеют твердое агрегатное состояние, а калиевые – жидкое (жидкое мыло).
При изготовлении мыла в него добавляют душистые вещества, глицерин, красители, антисептики, растительные экстракты.
Исходным сырьем для получения мыла служат растительные масла (подсолнечное, хлопковое и др.), животные жиры, а также гидроксид натрия или кальцинированная сода. Растительные масла предварительно подвергаются гидрогенизации, т. е. их превращают в твердые жиры. Применяются также заменители жиров — синтетические карбоновые жирные кислоты с большей молекулярной массой.»
· Почему мыло теряет свою моющую способность в жесткой воде?
Если мы используем для мытья и стирки жесткую воду, а такая вода содержит ионы Са 2+ и Mg2+,то мыло теряет свою моющую способность.
· Как вы думаете почему?
Это происходит в результате того, что кальциевые и магниевые соли высших карбоновых кислот нерастворимы в воде. Запишем уравнение реакции:
2С17Н35СООNa + СаСI2 = (C17 H35COO)2Ca ↓ + 2NaCI
· Почему после мытья волос твердым мылом в жесткой воде нужно прополоскать их раствором уксуса?
Чтобы удалить нерастворимые соли кальция и жирных кислот.
· Как используя мыльный раствор отличить родниковую воду от снеговой? (В родниковой выпадет осадок).
Домашнее задание: устно ответьте на вопросы- что такое жиры? Чем отличаются по строению жидкие жиры от твердых, Что такое мыла? Как их получают? Чем отличаются натриевые мыла от калиевых?
Тестирование
1 - В результате гидролиза жидкого жира образуются:
1) твердые жиры и глицерин; 3) глицерин и непредельные кислоты;
2) глицерин и предельные кислоты; 4) твердые жиры и смесь кислот.
Дата добавления: 2020-11-23; просмотров: 131; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
