В т о р о е о с н о в а н и е всего 64 трип-
Лекция 2. Молекулярные и цитологические основы наследственности. Клетка как элементарная единица наследственности. Генетический код.
Место генетики человека в системе биологических и медицинских знаний фармацевта определяется 2 главными обстоятельствами.
1. Теоретическое значение. Без знания алфавита невозможно читать.
2. Практическое значение. Современный уровень понимания механизмов действия многих лекарственных препаратов связан с влиянием на генетический материал и систему его реализации.
Биология - наука (слово) о жизни.
Жизнь- сложная открытая саморегулирующаяся, самовоспроизводящаяся система, постоянно обменивающаяся с окружающей средой веществом и энергией.
Разделами биологии можно считать все науки, которые имеют отношение к живым организмам. Это: физиология, ботаника, патология, микробиология, биохимия, молекулярная биология, фармакология, фармакотерапия...
Принципиальные отличия живого от неживого давно пытаются понять. Одно из важных отличий связывают с отношением живых и неживых систем ко второму закону термодинамики. Только живые системы и системы, созданные разумными существами, могут не подчиняться важнейшему аспекту этого универсального закона физики. Второй закон термодинамики - закон увеличения хаоса. Все неорганические системы стремятся к минимальному содержанию энергии и к максимуму энтропии, как меры неупорядоченности (степени хаоса). Во вселенной все известные неживые системы теряют энергию и упрощаются. Наоборот, живые системы усложняются и увеличивают энергию системы, что снижает энтропию. Так, например, из желудя вырастает дуб, а одна клетка - зигота становится человеком, состоящим из сотни триллионов клеток. Когда организм теряет жизнь, второй закон термодинамики начинает действовать в полном объеме. Разлагающиеся трупы теряют энергию и упрощаются вплоть до органических молекул.
|
|
|
Признаки жизни
1. Питание - получение материала для строительства тела.
Пища состоит из белков, липидов, углеводов, витаминов, минеральных веществ, которые используются, для построения человеческого тела.
2. Дыхание - получение окислителя.
Люди и большинство других живых существ используют для этого кислород.
3. Выделение - удаление отработанных продуктов метаболизма.
Выведение из организма конечных продуктов белкового обмена (мочевина, мочевая кислота) при работе почек.
4. Раздражимость - способность реагировать на изменения в среде обитания.
Рефлекторное одергивание руки при контакте с горячим предметом (утюгом, угольком).
|
|
|
5. Подвижность- движение организма в среде обитания и целенаправленное перемещение веществ по организму.
Транспорт глюкозы из листьев в стебель и корни растений.
6. Рост - увеличение размеров и самообновление живой системы.
Масса ребенка в течение первых 15 лет жизни увеличиваются от 3,5 до 80 кг: а рост от 50 до 180 см. Обновление кожи и других органов у взрослых людей не прекращается до смерти.
7. Размножение - способность воспроизводить себе подобные живые системы (характерно для вида в целом, а не для каждой особи).
В пчелиной семье трутни и матка производят на свет новых пчел, а рабочие пчелы, хотя и живые организмы, не участвуют в размножении.
Уровни организации живого.
Практически на всех этих уровнях можно обнаружить элементы современных генетических знаний.
1. Атомный (элементарный) уровень - это уровень, на котором рассматривают роль отдельных химических элементов в живом организме (Fe, F, I, Se, Na ...).
2. Молекулярный уровень. На этом уровне рассматривают молекулярные компоненты живых организмов (белки, липиды, углеводы, ДНК, РНК...).
3. Субклеточный уровень (органоидов). На этом уровне рассматривают органоиды клетки (миофибриллы, митохондрии, ядра, лизосомы...).
|
|
|
4. Клеточный уровень. На этом уровне рассматривают строение и функции отдельных клеток (бактерий, гепатоцитов, лейкоцитов...).
Элементарной единицей наследственности у даже у самых простых самодостаточных организмов является клетка. Клеточная теория (Шванн, Шлейден)- одно из важных биологических обобщений. Согласно этой теории все организмы имеют клеточное строение. Клетки, имеющие ядро - эукариоты (лейкоцит человека, амеба дизентерийная). Клетки, не имеющие ядра - прокариоты (стафилококки, кишечные палочки).
5. Тканевый уровень. На этом уровне рассматривают ткани организмов (эпителиальную, соединительную, нервную, мышечную).
6. Органный уровень. На этом уровне рассматривают отдельные органы (печень, кожа, почки, сердце...).
7. Системноорганный уровень. На этом уровне рассматривают системы органов (выделительную, пищеварительную, дыхательную...).
8. Организменный уровень. На этом уровне рассматривают целые организмы (человек, морская свинка, лягушка, гельминт, бактерия...)
9. Популяционно-видовой уровень. На этом уровне рассматривают группы особей одного вида (штамм стафилококков, колонию грызунов, человечество...).
|
|
|
10. Биогеоценотический уровень. На этом уровне рассматривают взаимодействие разных видов животных в среде обитания (биогеоценозах леса, озера, луга, тундры, пустыни...).
Относительно простых живых организмов (бактерии, некоторые водоросли, простейшие) организменный и клеточный уровни совпадают, а тканевый, органный, системно-органный отсутствуют.
Атомный или элементарный уровень организации живого. Основные химические элементы живого и примеры их роли в живых системах.
1. Макроэлементы: О, C, H, N, P, S, Na, K, Ca, Fe, Mg и др.
2. Микроэлементы: Cu, I, F, Co, Mo, Mn, Ni, Zn и др.
3. Ультрамикроэлементы:U, Au, Be, Hg, Cz, Se, Li и др.
Деление химических элементов на группы достаточно условно. Их значение для живого организма непропорционально их количеству. У одних элементов могут быть множественные функции, а роль других не слишком ясна.
Углерод, кислород, азот, водород - это базовые химические элементы органических молекул и воды, а кислород еще и главный окислитель для большинства живых организмов.
Фосфор можно отнести к базовым элементам. Фосфор - компонент ДНК, РНК, АТФ. Без фосфора нет ДНК, а без ДНК нет жизни.
Сера - компонент некоторых аминокислот, а без аминокислот нет белков.
Натрий и калий обеспечивают электрические процессы в мембранах живых клеток.
Кальций - активный участник сокращения мышц. Железо - компонент гемоглобина крови.
Магний входит в состав хлорофилла, без которого растения не усваивают солнечную энергию.
Медь входит в состав окислительных ферментов. Йод компонент гормонов щитовидной железы.
Фтор обеспечивает нормальную функцию эмали зубов. Кобальт входит в состав витамина B12.
В организме человека селен усиливает защиту клеточных мембран от свободнорадикального перекисного окисления, а обнаружение избытка лития в организме связывают с проявлением у людей психических расстройств.
Молекулярный уровень организации живого (белки).
Роль воды в организме. Самая распространенная молекула в организме
- это молекула воды (Н2О). Вода единственный универсальный растворитель и среда для химических реакций обмена веществ. Она принимает активное участие во многих биохимических реакциях (в т. ч. при метаболизме лекарственных веществ).
Основные группы органических молекул живых организмов: белки, нуклеиновые кислоты, липиды, углеводы.
Белки (протеины)- биологические гетерополимеры, мономерами которых являются аминокислоты.
Известно более 100 аминокислот, но только 20 их них кодируются триплетным кодом в ДНК всех живых организмов. Аминокислоты делят на
«заменимые» и «незаменимые» для людей.
Общая формула аминокислот H2N-HCR-COOH, где R-радикал, по которому они отличаются друг от друга. Аминокислоты амфотерные соединения, связывающиеся в молекулы белка пептидными связями. При образовании дипептида происходит реакция:
H2N-HCR1-COOH + H2N-HCR2-COOH = H2N-HCR1-OC-NH-HCR2-COOH
+ H2O
 |
С точки зрения химического строения белков (протеинов) выделяется:
- первичная структура - последовательная цепочка аминокислот, соединенная пептидными связями;
- вторичная структура - цепочка сворачивается в спираль;
- третичная структура - спираль скручивается в глобулу (шарик, глыбку);
- четвертичная структура - несколько глобул образуют крупный
конгломерат.
Функции белков.
1. Структурная (строительная). Белки входят в состав или являются частью клеточных мембран, ферментов, пищевых продуктов, рецепторов, гемоглобина, антител, микрофиламентов мышечных клеток, гормонов, нуклеопротеидов ДНК...
2. Ферментативная. Белки - катализаторы биохимических реакций. Ферменты не только ускоряют реакции. Без ферментов скорость большего числа биохимических реакций была бы нулевой.
Названия ферментов часто имеют окончание "-аза", которое добавлено к корню слова, обозначающего субстрат реакции. Например, фермент лактаза расщепляет молочный сахар лактозу.
3. Энергетическая. При полном окислении 1 г белков выделяется энергия = 4,1 ккал или 17,2 кДж.
4. Сигнальная. Белки входят в состав гликопротеидов многих видов рецепторов. Например, рецепторов постсинаптических мембран мышечных клеток.
5. Транспортная. Белки - переносчики веществ в организме. Так, белок гемоглобин переносит кислород, а для переноса с кровью липидов используются их соединения с белками- липопротеидные комплексы.
6. Защитная. Белки защищают организм от чужеродных объектов. Например, иммуноглобулины-антитела защищают людей от бактерий и собственных мутантных клеток.
7. Двигательная (сократительная). Белки актин и миозин входят в состав сократительных элементов мышечных клеток.
8. Регуляторная. Некоторые биологически активные вещества гормоны являются белками (соматотропный гормон, инсулин).
9. Репродуктивная. Белки принимают участие в хранении и реализации генетической информации (гистоны ДНК, белки-репрессоры).
Нуклеиновые кислоты - это биологические гетерополимеры нуклеотидов. Они имеют сложную первичную (цепочка нуклеотидов), вторичную (первичная спираль) и третичную структуру (вторичную спираль, кольцо, глобулу). Первичная структура нуклеиновых кислот представляет собой цепочку из нуклеотидов.
Выделяют 8 разновидностей нуклеотидов. Четыре разновидности нуклеотидов для дезоксирибонуклеиновой кислоты (ДНК)-и четыре для рибонуклеиновой кислоты (РНК).
Каждый нуклеотид этих гетерополимеров состоит из 3 компонентов: азотистого основания, пятиуглеродного сахара (пентозы) и остатка фосфорной кислоты.
 O H
O H

 O P O H
O P O H

O H
1. Фосфорная кислота (Ф) одинакова у ДНК и РНК.
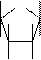
2. Пентоза - это пятиуглеродный моносахарид.
H2

 H O C O H O
H O C O H O
H H
H H
H2
 H O C O H O
H O C O H O
H H
H H
O H O H
O H H
Пентоза РНК - рибоза. Пентоза ДНК- дезоксирибоза
3. Азотистых оснований нуклеиновых кислот пять видов. Их разделяют на большие- производные пурина (два гетероциклических кольца) и маленькие- производные пиримидина (один гетероцикл).
пурин пиримидин

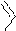
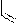
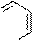 N N N
N N N
|
N H
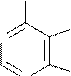
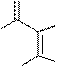
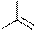
Пуриновых азотистых оснований два - аденин и гуанин (А и Г).
аденин гуанин
 NH2
NH2
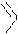 N N
N N
|
O
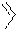
 HN N
HN N
|
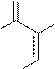
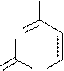
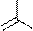
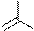
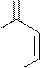
Пиримидиновых азотистых оснований три- тимин, цитозин и урацил (Т, Ц и У).
 O
O
 HN CH3 N
HN CH3 N
NH2 O
 HN
HN
O N O N O N
H H H
тимин цитозин урацил
Название нуклеотида определяется его азотистым основанием и часто сокращается до одной буквы.
В молекуле ДНК 4 вида нуклеотидов: А, Г, Т, Ц.
Аденин (аденин + фосфорная кислота + рибоза или АФД) = А. Гуанин (ГФД)- Г. Тимин (ТФД) = У. Цитозин (ЦФД) = Ц.
В молекуле РНК тоже 4 вида нуклеотидов. А, Г, У, Ц.
Аденин (аденин + фосфорная кислота + рибоза или АФР) = А. Гуанин (ГФР)- Г. Урацил (ТФР) = У. Цитозин (ЦФР) = Ц.
Пример нуклеотида РНК - АФР. Пример нуклеотида ДНК -
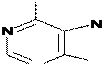
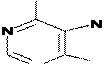 NH2 NH2
NH2 NH2



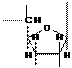 O H N H N
O H N H N


 O P O O H
O P O O H
O H N H N




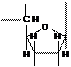 O P O O H
O P O O H
АФД
O H O H
H O H
Таким образом, на этом уровне ДНК и РНК отличаются по виду остатка сахара (рибоза и дезоксирибоза) и по одному виду азотистого основания. В ДНК это тимин, в РНК урацил.
Молекулы нуклеиновых кислот представляют собой цепочки, соединенные посредством прочных ковалентных связей между фосфорной кислотой одного нуклеотида и пентозой следующего нуклеотида.
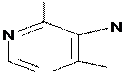
Пример соединения аденина и цитозина в одной цепочке молекулы ДНК:
 NH2
NH2
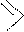 |
O H N H N



 O P O O H
O P O O H
NH2
 O H O N
O H O N

 H2
H2



 O P O C
O P O C
 O
O
H H
O H
H H
O H H
Вторичная структура ДНК имеет форму скрученной лестницы или двойной спирали. Две отдельные цепочки молекулы ДНК соединяются друг с другом посредством относительно слабых водородных связей между азотистыми основаниями нуклеотидов. Такие связи лежат в основе принципа комплементарного спаривания нуклеотидов. При комплементарном спаривании нуклеотидов соблюдаются строгие правила.
Большие (пуриновые) азотистые основания спариваются только с маленькими (пиримидиновыми).
Гуанин в любой молекуле (ДНК и РНК) может спариваться только с цитозином, образуя три водородные связи.
Аденин в молекуле может спариваться с тимином или с урацилом, образуя по две водородные связи. Если аденин спаривается с тимином, то синтезируется или работает молекула ДНК. Если аденин спаривается с урацилом, то синтезируется или работает молекула РНК.
 Другие варианты спаривания нуклеотидов невозможны. Кратко принцип
Другие варианты спаривания нуклеотидов невозможны. Кратко принцип

 А Т(У)
А Т(У)

 Пуриновые Г Ц Пиримидиновые
Пуриновые Г Ц Пиримидиновые
комплементарного спаривания азотистых оснований нуклеотидов записывают так:
Пример соединения двух пар нуклеотидов в молекуле ДНК
ТИМИН
 H3C O
H3C O


 H2N
H2N
АДЕНИН
 O O H
O O H
 H2 N
H2 N
NH O
H O P O C
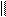 O
O
O
 O
O
O
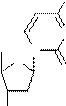 ЦИТОЗИН
ЦИТОЗИН
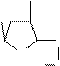 NH2 N
NH2 N
N
|
C H2
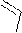
 O P O H
O P O H

O

 H O P O O
H O P O O
C H2 N
 O
O
O
HN


 H2N
H2N
 N H2
N H2
|
 O
O

 H O P O
H O P O
O P O H
 O
O

Этот принцип является не только способом связи параллельных цепочек ДНК. Он основа для репликации ДНК и реализации генетической информации (транскрипция при биосинтезе белка). Для понимания последнего процесса используется понятие о генетическом коде.
Таблица 1. Универсальный генетический код. Последовательности азотистых оснований в триплетах и кодируемые ими аминокислоты для и-РНК. Свойства генетического кода.
в т о р о е о с н о в а н и е всего 64 трип-
┌────────┬────────┬────────┬────────┐ лета генети-
│ У │ Ц │ А │ Г │ ческого кода
┌─┼────────┼────────┼────────┼────────┼─┐
│У│УУУ Фен │УЦУ Сер │УАУ Тир │УГУ Цис │У│ 61 триплет ко- п│ │УУЦ Фен │УЦЦ Сер │УАЦ Тир │УГЦ Цис │Ц│т дирует все 20 е│ │УУА Лей │УЦА Сер │УАА стоп│УГА стоп│А│р аминокислот, р│ │УУГ Лей │УЦГ Сер │УАГ стоп│УГГ Трп │Г│е если 1 амино- в├─┼────────┼────────┼────────┼────────┼─┤т кислоту коди- о│Ц│ЦУУ Лей │ЦЦУ Про │ЦАУ Гис │ЦГУ Арг │У│ь рует не 1 три- е│ │ЦУЦ Лей │ЦЦЦ Про │ЦАЦ Гис │ЦГЦ Арг │Ц│е плет, а более,
│ │ЦУА Лей │ЦЦА Про │ЦАА Глн │ЦГА Арг │А│ то такой код о│ │ЦУГ Лей │ЦЦГ Про │ЦАГ Глн │ЦГГ Арг │Г│о называют вы- с├─┼────────┼────────┼────────┼────────┤─┤с рожденным н│А│АУУ Иле │АЦУ Тре │ААУ Асн │АГУ Сер │У│н
о│ │АУЦ Иле │АЦЦ Тре │ААЦ Асн │АГЦ Сер │Ц│о 1 триплет мо- в│ │АУА Иле │АЦА Тре │ААА Лиз │АГА Арг │А│в жет кодировать а│ │АУГ Мет │АЦГ Тре │ААГ Лиз │АГГ Арг │Г│а только 1 ами- н├─┼────────┼────────┼────────┼────────┼─┤н нокислоту и│Г│ГУУ Вал │ГЦУ Ала │ГАУ Асп │ГГУ Гли │У│и
е│ │ГУЦ Вал │ГЦЦ Ала │ГАЦ Асп │ГГЦ Гли │Ц│е 3 триплета ко-
│ │ГУА Вал │ГЦА Ала │ГАА Глу │ГГА Гли │А│ дируют оконча-
│ │ГУГ Вал │ГЦГ Ала │ГАГ Глу │ГГГ Гли │Г│ ние синтеза -
└─┴────────┴────────┴────────┴────────┴─┘ - это термини-
Рующие кодоны
Сокращения:
стоп - кодон окончания синтеза
1. Ала - L-Аланин 11. Тре - L-Треонин У-урацил
2. Вал - L-Валин 12. Цис - L-Цистеин Ц-цитозин
3. Лей - L-Лейцин 13. Тир - L-Тирозин А-аденин
4. Иле - L-Изолейцин 14. Асн - L-Аспаргин Г-гуанин
5. Мет - L-Метионин 15. Глн - L-Глутамин
6. Про - L-Пролин 16. Асп - L-Аспаргиновая кислота
7. Фен - L-Фенилаланин 17. Глу - L-Глутаминовая кислота
8. Трп - L-Триптофан 18. Лиз - L-Лизин
9. Гли - L-Глицин 19. Арг - L-Аргинин
10. Сер - L-Серин . 20. Гис - L-Гистидин
У некоторых вирусов двухцепочечной может быть РНК.
Связи между параллельными цепочками слабые (водородные), но многочисленные, что делает систему достаточно надежной.
Конкретная последовательность нуклеотидов в цепочках нуклеиновых кислот не случайная. Она передается из поколения в поколение по наследству и определяет генетический код.
Функции ДНК - хранение и реализация генетической информации.
ДНК хранит информацию и о молекулах небелковой природы (нуклеотиды, фосфолипиды, углеводы, пигменты и т.д.). Чтобы инициировать любую биохимическую реакцию надо обеспечить ее ферментативным аппаратом. Чтобы получить небелковое соединение
(например, пигмент), надо сделать белок-фермент-катализатор для его синтеза. И в этом случае ключевым молекулярным механизмом является принцип комплементарного спаривания азотистых оснований нуклеотидов.
РНК делят на 3 группы.
1. Матричная РНК (м-РНК) и близкая к ней информационная (и-РНК)- это комплементарная копия участка одной из цепочек ДНК. Она получена по принципу комплементарного спаривания азотистых оснований и представляет собой одну полинуклеотидную цепочку из разного количества нуклеотидов (от нескольких десятков до нескольких тысяч).
Функция и-РНК - перенос информации от хранилища (ДНК) к месту реализации, например, на рибосомы для сборки белка. Функционально и- РНК можно разделить на триплетные кодоны (тройки нуклеотидов, кодирующих аминокислоты).
2. Рибосомальные р-РНК, образуют большую и малую субъединицу рибосом. Их функция связана с ролью рибосом, как мест сборки белка.
3. Транспортные т-РНК, имеют сложную пространственную конфигурацию, но на плоскости изображаются в форме клеверного листа. По их главной части - триплетному антикодону - можно различить более 60 разновидностей т-РНК.
Функция т-РНК: перенос аминокислот к рибосомам на встречу с и-РНК.
Т. о., с помощью генетического кода ДНК можно записать любую последовательность аминокислот и синтезировать не только белки, но и любую другую группу органических веществ.
Всего в геноме человека насчитывается более 3 миллиардов нуклеотидных пар.
Дата добавления: 2020-11-15; просмотров: 107; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
