Адсорбция ионов на кристалле. Электрокинетические явления
Образование и строение ДЭС. Электрокинетический потенциал. Правила написания мицелл
Адсорбция электролитов сводится к адсорбции ионов, т.е. переходу ионов из одной фазы в другую. Это явление приводит к образованию двойного электрического слоя (ДЭС). Переход ионов обусловлен различием значения величины химического потенциала компонентов (ионов) в граничащих фазах. Ионы переходят из фазы с большим значением в фазу с меньшим значением. В результате на границе раздела фаз образуется скачок потенциала, который приостанавливает дальнейший переход ионов. В зависимости от значения ионы переходят из раствора на поверхность или наоборот. В обоих случаях поверхность приобретает избыточный заряд, который компенсируется ионами противоположного знака. Таким образом, на поверхности раздела фаз возникает двойной электрический слой (ДЭС).
Пути образования ДЭС:
1-й путь – адсорбционный;
2-й путь - поверхностная диссоциация.
Рассмотрим 1-й путь. Пусть происходит реакция
AgNO 3 + KCl ® AgCl + KNO 3
Примем, что в избытке KCl. Образующиеся кристаллы AgCl находятся в ионном растворе, содержащем ионы К+, Сl-, NO3-, при условии ж(Cl-) >т(Сl-). Ионы Cl переходят из раствора в твердую фазу, т.е. адсорбируются на твердой поверхности кристалла, на границе раздела фаз не возникает необходимость для равновесия скачка потенциала. Поверхность кристалла при этом приобретает отрицательный заряд. Поскольку согласно правилу Фаянса - Панета – Пескова на кристалле адсорбируются ионы общей природы с ионами кристалла или изоморфные им, т.е. способные достраивать кристаллическую решетку.
|
|
|

В нашем случае адсорбция ионов Cl- происходит за счет химических сил, приводящих к прочному присоединению их к кристаллу. Оставшиеся в растворе ионы К+ электростатически притягиваются к поверхности и восстанавливают нарушения электронейтральности системы. Однако прочно к поверхности они не присоединяются, а так как их концентрация около поверхности больше, чем в растворе, то они диффундируют в сторону меньшей концентрации, т.е. от поверхности в раствор. На поверхности кристалла возникает двойной электрический слой (ДЭС), имеющий следующее строение:
ДЭС состоит из внутренней обкладки или адсорбционного слоя (ионы Cl-) и наружной обкладки или слоя противоионов (ионы К+). Часть противоионов связано с поверхностью относительно прочно и входит в плотный слой. Остальные противоионы, совершающие тепловое движение около поверхности, составляют диффузионную часть двойного электрического слоя (ДЭС). Распределение противоионов плотной и диффузной частей определяется соотношением между электростатическими притяжением ионов к поверхности и их диффузии в растворе. Последнее определяется тепловым движением ионов и зависит от разности концентрации в двойном электрическом слое (ДЭС) и объеме раствора. Если для реакции взять избыток AgNO3, то внутренняя обкладка двойного электрического слоя (ДЭС) будет состоять из ионов Ag, а противоположными будет NO3. Примером двойного электрического слоя (ДЭС), образованного путем поверхностной диссоциации, является двойной электрический слой (ДЭС), возникающий на поверхности стекла в H2O за счет катионов К, Na и т.п. Таким образом, поверхность стекла в H2O заряжается отрицательно. Растворение материала поверхности и возникновение на ней двойного электрического слоя (ДЭС) можно вызвать добавлением веществ, реагирующих с поверхностью. Например, амфотерный Al(OH)3 в присутствии кислоты заряжается положительно, а в щелочи отрицательно.
|
|
|
 Al(OH)3 . . Al(OH)2Cl . Al(OH)2+ Cl-
Al(OH)3 . . Al(OH)2Cl . Al(OH)2+ Cl-
Al(OH)3 . +HCl . Al(OH)2Cl . Al(OH)2+ Cl-

 Al(OH)3 . . Al(OH)2Cl . Al(OH)2+ Cl-
Al(OH)3 . . Al(OH)2Cl . Al(OH)2+ Cl-
Al(OH)3 . . Al(OH)2Cl . Al(OH)2+ Cl-
Al(OH)3 . . Al(OH)2Cl . Al(OH)2+ Cl-
|
|
|

В пределах двойного электрического слоя (ДЭС) действует электрическое поле, интенсивность которого характеризуется значением потенциала. На рис. 2.5.1.1 показано изменение потенциала двойного электрического слоя (ДЭС) на кристалле AgCl с увеличением расстояния от поверхности. Потенциал на поверхности частицы называется термодинамическим потенциалом. Он характеризует скачок потенциала на границе раздела между фазами. Ионы в слое противоионов (плотного слоя) приближаются к поверхности на расстояние, определяемое собственными размерами. Воображаемая поверхность, проведенная через их центры, называется плоскостью максимального приближения и расположена на расстоянии порядка молекулярных размеров, а потенциал плоскости равен . Смещение фаз в дисперсной системе относительно друг друга вызванное внешними силами (электрическое поле) происходит по поверхности скольжения, которая не всегда совпадает с плоскостью максимального приближения и обычно расположена на бόльшем расстоянии от поверхности. Потенциал на поверхности скольжения называется электрокинетическим потенциалом или z потенциалом. Его можно рассчитать из электрокинетических экспериментов. Его значение зависит от числа не скомпенсированных на поверхности скольжения зарядов адсорбционного слоя, т.е. числа ионов в диффузионном слое. Падение потенциалов в плотной части двойного электрического слоя (ДЭС) имеет линейный характер. В диффузной части двойного электрического слоя (ДЭС) для слабо заряженных поверхностей изменение потенциалов с расстоянием подчиняется экспоненциальной зависимости
|
|
|

где j 0- потенциал поверхности;
c- параметр Дебая;
r - характеристическая величина атмосферы, расстояние, на котором действуют адсорбционные силы;
х - расстояние от поверхности, толщина двойного электрического слоя (ДЭС).
 ,
,
где z – заряд.
Существует несколько правил для составления мицелл:
1. Основа мицеллы – агрегат, нерастворимый в данной дисперсионной среде, состоящий из множества (m) молекул (атомов) простого вещества (осадка).

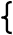 mAg3AsO3 × nAsO33- × 3(n-x)Na+ -3x×3xNa+
mAg3AsO3 × nAsO33- × 3(n-x)Na+ -3x×3xNa+
Агрегат Потенциал- Противо- Ионы
определяю- ионы диффузионного
 щие ионы адсорбции- слоя
щие ионы адсорбции- слоя
онного слоя

 Ядро мицеллы
Ядро мицеллы
Адсорбционный слой Диффузион-
 ный слой
ный слой
Коллоидная частица
Здесь m , n , x – натуральные числа;
m – число молекул в агрегате;
n – число потенциалопределяющих ионов;
(n – x) – число противоионов адсорбционного слоя;
x – число противоионов диффузного слоя.
Численный коэффициент 3 перед (n – x) и х поставлен ввиду трехос-новности аниона AsO33-.
2. Согласно правилу Пескова-Фаянса-Панета, на поверхности агрегата адсорбируются ионы электролита-стабилизатора, входящие в состав агрегата, либо имеющие общую природу с ним, либо специфически взаимодействующие с ним и находящиеся в избытке. Ионы, сообщающие агрегату поверхностный заряд, называются потенциалопределяющими. Агрегат + потенциалопределяющие ионы = ядро мицеллы.
3. Заряд ядра компенсируется эквивалентным количеством противоположно заряженных ионов электролита-стабилизатора – противоионов. Часть противоионов, прочно связанных с ядром, входит в адсорбционный слой. Агрегат + адсорбционный слой = коллоидная частица (имеет заряд).
4. Остальная часть противоионов образует диффузионный слой.
5. Суммы электрических зарядов коллоидной частицы и диффузионного слоя равны друг другу по абсолютной величине и противоположны по знаку.
6. Электрический заряд коллоидной частицы равен алгебраической сумме электрических зарядов потенциалопределяющих ионов и противоионов адсорбционного слоя.
7. Мицелла гидрофобного золя является электронейтральной, т.е. алгебраическая сумма электрических зарядов ионов всех слоев равна нулю
Для любого типа реакции одно из исходных веществ берут в избытке по сравнению со стехиометрически необходимым соотношением:
Na3AsO3 + 3AgNO3 → ↓Ag3AsO3 + 3NaNO3
избыток осадок
Электролитическая диссоциация электролита, взятого в избытке:
Na3AsO3 « 3Na+ + AsO33-
Заряд коллоидной частицы определяется так (правило 6):
n(-3) + 3(n – x)(+1) = -3x
Для проверки правильности записи формулы мицеллы подсчитывают алгебраическую сумму зарядов всех ионов (правило 7):
n(-3) + 3(n – x)(+1) + 3х(+1) = 0
Коллоидная частица имеет отрицательный заряд, мицелла в целом электронейтральна.
Дата добавления: 2019-11-25; просмотров: 478; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
