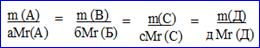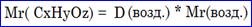РЕШЕНИЕ ЗАДАЧ НА ОПРЕДЕЛЕНИЕ МОЛЕКУЛЯРНОЙ ФОРМУЛЫ»
Цель: Научиться решать задачи на нахождение молекулярной формулы веществ по известным данным о продуктах реакции и составе вещества.
ТЕОРИТИЧЕСКАЯ ЧАСТЬ
Реакция: аА + бВ® сС + дД
Используя данные пропорции можно рассчитать любую величину:
Формулы для расчёта:
| ¾  По водороду ( Mr(H2)= 2):
¾ По водороду ( Mr(H2)= 2):
¾  По хлору( Mr(CL2)= 71):
¾ По воздуху ( Mr(воздуху)= 29): По хлору( Mr(CL2)= 71):
¾ По воздуху ( Mr(воздуху)= 29):
¾ По кислороду ( Mr(О2)= 32):
| ||||||||||||||||||||||||||||||
ПРАКТИЧЕСКАЯ ЧАСТЬ
| ЗАДАЧА №1 Установите молекулярную формулу углеводорода, если плотность его равна 4,107г/л.(н.у.), а массовая доля углерода -91,31%. Дано: Р (СхНу)=4,107г/л W%(С)=91,31%. W%(Н)=100-91,31=8,69%. Найти: СxHy, где Х -число атомов «С», Y- атомов «Н» Решение: 1. Найдем молекулярную массу углеводорода: М(СхНу)= Р (СхНу) * Vm=4.107* 22.4=92г/ моль 2. Определим количество атомов «С» в веществе: -92г/моль - 100% - m (С) г. - 91,31 m(С) =92 * 91.31 / 100% = 84 г., Х= m(С) / Аr(C) = 84 / 12 = 7 3. Определим количество атомов «Н» в веществе: -92г/моль - 100% - m (Н) г. - 8,69% m(Н) =92 * 8,69 /100% = 8 г. Y= m(Н) / Аr(C) = 8 / 1 = 8 4. Сделаем проверку: Мr (С7Н8) =7*12+8*1=92 Ответ: С7Н8 | Хлоропроизводное углеводорода имеет плотность по воздуху 8,07. Определите формулу соединения, если его состав входят:89,1%хлора и 10,9%углерода. Дано: …………………………………………………………………… …………………………………………………………………… Найти:…………………………………………………………… Решение: …………………………………………………………………… …………………………………………………………………… …………………………………………………………………… …………………………………………………………………… …………………………………………………………………… …………………………………………………………………… …………………………………………………………………… …………………………………………………………………… …………………………………………………………………… …………………………………………………………………… |
| ЗАДАЧА №2 При сжигании 25г .органического вещества получили 70,2 г. газа СО2 и 14.36г. воды. Определите формулу вещества , если его плотность по отношению к кислороду равна 2,937. Дано: m(CxHyOz) =25г. m (СО2)=70,2г. m (Н2О)=14,36г. Д о2(СхНуОz)=2,937 Найти: СхНуОz Решение: При горении cоединения образовался СО2 и Н2О, предположим, что формула его СхНуОz. a) Найдем молекулярную массу вещества М(СхНуОz)=М(О2)* Dо2(СхНуОz)=32×2,937=94г/моль. b) Составим уравнение горения 2СхНуОz+вО2® 2хСО2 +уН2О Составим пропорцию: m (СхНуО z ) = m ( C О2) = m (Н2О) 2М(СхНуОz) 2хМ(СО2) уМ(Н2О) Выразим из пропорции Х m (СхНуО z = m ( C О2) 2М(СхНуОz) 2хМ(СО2) Х= m ( C О2) *2*М(СхНуО z ) = 70,2*2*94 =6 m (СхНуОz)*2*М(СО2) 25*2*44 Выразим из пропорции У : m (СхНуО z ) = m (Н2О) 2М(СхНуОz) уМ(Н2О) У= m (Н2О) × 2М(СхНуО z ) = 14,36*2*94 =6 m (СхНуОz)×М(Н2О) 25*18 Выразим z Z=М(СхНуО z )-хА r (С)-уА r ( H) = 94-6*12-6*1 = 1 Ar(O) 16 Ответ : С 6Н6О. | При сжигании 3г. неизвестного органического соединения получили 4,63 л. углекислого газа и 4,69г. воды. Определите формулу соединения, если известно , что 2,5л. его весят 6,47г.(н.у.) Дано: …………………………………………………………………… …………………………………………………………………… Найти:…………………………………………………………… Решение: …………………………………………………………………… …………………………………………………………………… …………………………………………………………………… …………………………………………………………………… …………………………………………………………………… …………………………………………………………………… …………………………………………………………………… …………………………………………………………………… …………………………………………………………………… …………………………………………………………………… …………………………………………………………………… …………………………………………………………………… …………………………………………………………………… …………………………………………………………………… …………………………………………………………………… …………………………………………………………………… …………………………………………………………………… |
САМОСТОЯТЕЛЬНАЯ РАБОТА
Выполнить одно из дифференцированных заданий.
| Программа А («5») Сожгли 44 г. углеводорода и получили 17,11г. СО2 и 16,55г. Н2О. Определите его формулу, если его плотность по водороду равна 36. Необходимо учесть , что в веществе присутствовало 25 % горючего материала. Программа Б («4») Сожгли 7г. углеводорода и получили 20,53г. углекислого газа и 12,6г. воды. Определить формулу углеводорода, если его плотность при нормальных условиях равна 1,34г/л. Программа С («3») Найдите молекулярную формулу вещества содержащего 82,8% углерода и 17,2% водорода, плотность вещества при нормальных условиях 2,59г/л | …………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………… |
Вывод:
………………………………………………………………………………………………………………………………………….
………………………………………………………………………………………………………………………………………….
………………………………………………………………………………………………………………………………………….
ПРАКТИЧЕСКАЯ РАБОТА №13
"РЕШЕНИЕ ЭКСПЕРИМЕНТАЛЬНЫХ ЗАДАЧ НА ИДЕНТИФИКАЦИЮ ОРГАНИЧЕСКИХ ВЕЩСТВ.
РАСПОЗНОВАНИЕ ПЛАССТМАС И ВОЛОКОН".
Дата добавления: 2019-09-13; просмотров: 152; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!