Агонисты глутамат связывающего сайта
Из эндогенных соединений агонистом рецепторов NMDA являются не только L‑глутаминовая кислота, но и D- и L‑аспарагиновые кислоты. Эти соединения обладают приблизительно одинаковой агонистической активностью, в то время как D‑глутаминовая кислота менее активна, чем L‑изомер. Указанные соединения не обладают специфичностью, а параллельно участвуют во многих биохимических процессах. Поэтому, с целью получения селективных агонистов, конструировали их аналоги.
Удачным явилось варьирование заместителя у атома N‑аминогруппы. N‑метиласпарагиновая кислота определяет прототип рецепторов, а вот N‑этиласпарагиновая кислота обладает схожей активностью. D‑конфигурация хирального центра N‑замещенных аналогов является предпочтительной, а соответствующие L‑изомеры существенно менее активны. Дальнейшее увеличение длины алкильного заместителя приводит к резкому снижению активности.
Конструирование агонистов включает в себя синтез биоизостерических аналогов глутаминовой и аспарагиновой кислот. Например, замена карбоксильной группы на фосфоновую 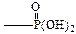 или сульфогруппу приводило к уменьшению активности полученных соединений.
или сульфогруппу приводило к уменьшению активности полученных соединений.
Другой тип структурной модификации глутаминовой кислоты заключается в ограничении конформационной подвижности функциональных групп. Этот пример является классическим в медицинской химии, так как во многих случаях позволяет зафиксировать наиболее подходящие для взаимодействия с активным центром конформации. При этом очевидно, что активность структурно жестких аналогов ГАМК (γ‑аминомасляной кислоты) должно существенным образом зависеть от стереохимии.
|
|
|
Таким образом для подавляющего большинства агонистов рецепторов NMDA характерны следующие структурные особенности:
1. Наличие одной основной и двух кислотных группировок
2. Короткая, в 1,2‑метиленовой группировке, цепочка, соединяющая терминальные кислотные группировки.
3. D‑конфигурация хирального центра.
Исключения составляют активные соединения, в структуре которых нет карбоксильной группы у β‑углеродного атома. К ним относится тетразолилглицин – один из наиболее активных агонистов рецепторов NMDA.
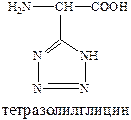
Функциональную роль карбоксила здесь выполняет гетероциклический фрагмент, в частности тетразолильный, который часто используется в медицинской химии для конструирования биоизостеров карбоксила.
Антагонисты глутамат связывающего сайта
Изначальные вариации структуры ГАМК (γ‑аминомасляной кислоты) включают в себя удлинение цепи, соединяющей терминальные карбоксильные группировки. Этот прием часто используется в медицинской химии для конструирования антагонистов. Некоторые из удлиненных аналогов глутамата, например, α‑аминопробковая кислота, проявляют умеренную антагонистическую активность по отношению к рецепторам NMDA. Биоизостерическая замена карбоксильной группировки этих аналогов на фосфоновую и сульфоновую группировки показало, что наибольшей антагонистической активностью обладает 2‑аминофосфонокарбоновые кислоты.
|
|
|
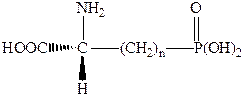
В настоящее время они и являются наиболее изученным классом конкурентных антагонистов рецепторов NMDA. Среди удлиненных фосфоновых аналогов глутаминовой кислоты наибольшей антагонистической активностью обладают нечетные члены ряда. Когда n = 3 мы имеем 2‑амино‑5‑фосфоновалериановую кислоту, при n = 5 - 2‑амино‑7‑фосфоноэнантовую кислоту. Кислоты с n = 4 и n = 6 значительно слабее. L‑изомеры всех указанных соединений менее активны.
Конструирование структурно жестких аналогов ω‑аминофосфонкарбоновой кислоты привело к созанию новых структурных типов антагонистов, например, циклобутанкарбоновые кислоты – сильные антагонисты рецепторов NMDA.
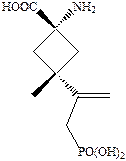
Из ароматических аналогов аминодикарбоновых кислот (более жесткий цикл) умеренной антагонистической активностью обладает 4‑карбоксифенилглицин, который является соединением лидером для многочисленных структурных модификаций.
|
|
|
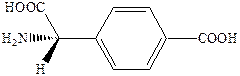
Введение карбоксильной группы в положение 3 бензольного кольца приводит к резкому повышению антагонистической активности, но одновременно расширяет спектр действия полученного соединения, которое приобретает свойство слабого агониста AMPA каинатных рецепторов.
Еще один структурный класс антагонистов рецепторов NMDA: фосфорилированные производные фенилаланина или дифенилаланина. Производные дифенила являются одними из самых сильных антагонистов описанных на сегодня.

Эффект максимальный, когда R = 2Cl.
Суммируя данные о конструировании антагонистов глутаминового сайта рецепторов NMDA можно выделить следующие закономерности:
1) Относительно длинная цепочка (3-6 метиленовых групп), соединяющая терминальные кислотные функции.
2) Предпочтительно замещение одной карбоксильной группы на фосфоновую.
3) Предпочитать D‑конфигурацию хирального центра.
Дата добавления: 2019-09-08; просмотров: 183; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
