Синтез S-заміщених похідних 2-метил-4-меркапто-8-метоксихіноліну.
S-заміщені похідні 2-метил-4-меркапто-8-метоксихіноліну були синтезовані на основі 2-метил-4-хлоро-8-метоксихінолінів (І) і 2-метил-4-меркапто-8-метоксихінолінів (П) за відомими реакціями, що наведені на схемах 1, 2 [Бражко О.А. дис... доктора біол. наук: .- К., 2005].
Будову отриманих сполук (Табл.) доведено за допомогою елементного аналізу, ІЧ- та ПМР-спектроскопії, хромато-мас-спектрометрії, а чистота – за допомогою тонкошарової хроматографії.
Для забезпечення кращої водорозчинності синтезованих похідних вони були перетворені у ряді випадків у відповідні гідрохлориди або натрієві чи калієві солі (див. сполуки 2, 5, 6, 10, 12, 14, 15, 17, 19-21, 23, 25, 26, 34, 35).
Таблиця
S-заміщені похідні 2-метил-4-меркапто-8-метоксихінолінів
| № | Сполука | № | Сполука | № | Сполука |
| 1 | 
| 13 | 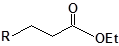
| 25 | 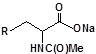
|
| 2 | 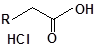
| 14 | 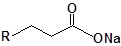
| 26 | 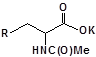
|
| 3 | 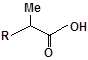
| 15 | 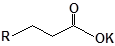
| 27 | 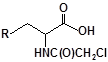
|
| 4 | 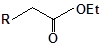
| 16 | 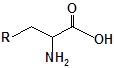
| 28 | 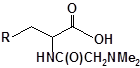
|
| 5 | 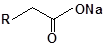
| 17 | 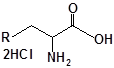
| 29 | 
|
| 6 | 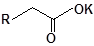
| 18 | 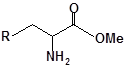
| 30 | 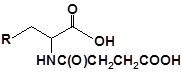
|
| 7 | 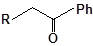
| 19 | 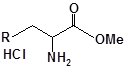
| 31 | 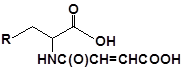
|
| 8 | 
| 20 | 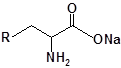
| 32 | 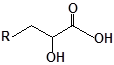
|
| 9 | 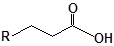
| 21 | 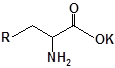
| 33 | 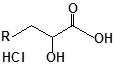
|
| 10 | 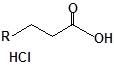
| 22 | 
| 34 | 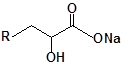
|
| 11 | 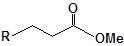
| 23 | 
| 35 | 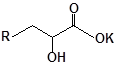
|
| 12 | 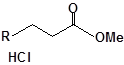
| 24 | 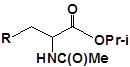
| 36 | 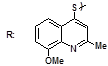
|
Зв’язок між хімічною будовою й біологічною активністю в ряду S-заміщених 2-метил-4-меркапто-8-метоксихінолінів
Гостра токсичність. За результатами дослідження гострої токсичності показано, що ЛД50 синтезованих сполук знаходиться в межах від 566 − 2000 мг/кг і залежить від їх хімічної будови. Це дозволяє віднести їх до мало- та нетоксичних сполук за класифікацією Сидорова (Сидоров К.К., 1973).
|
|
|
Подовження карбонового ланцюга на метиленову групу не впливає на ЛД50 (сполуки 1 та 9). ЛД50 знаходиться майже на рівні – 900 і 969 мг/кг відповідно.
Наявність аміногрупи в карбоновому ланцюзі збільшує токсичність (сполука 16 – в порівнянні зі сполукою 9) – 898 і 969 мг/кг відповідно.
Заміна аміногрупи на гідроксильну в α-положенні карбонового ланцюга (сполука 32 – 2-гідрокси-3-(8-метокси-2-метилхінолін-4-ілтіо)пропанова кислота) не змінює ЛД50 в порівнянні зі сполукою 16.
Наявність N–ацетильного залишку в карбоновому ланцюзі в 4-му положенні хінолінового циклу зменшує токсичність (сполука 22 – 2-ацетиламіно-3-(8-метокси-2-метилхінолін-4-ілтіо)пропанова кислота) в порівнянні зі сполукою 16. ЛД50 – 1245 мг/кг.
Етерифікація (-ОС2Н5) карбоксильної групи (сполука 4) збільшує гостру токсичність (ЛД50 – 714±56 мг/кг), а сполуки 13 – зменшує її (ЛД50 – <2000 мг/кг).
Найбільшу токсичність має гідрохлорид метилового естеру (8-метокси-2-метилхінолін-4-ілтіо)пропанової кислоти − сполука 12 (рис. 1). Його ЛД50 становить 566 мг/кг.
Рис. 1. Гостра токсичність S-заміщених 2-метил-4-меркапто-8-метоксихінолінів
Антирадикальна і антиоксидантна активність. У дослідах in vitro на моделі аутоокиснення адреналіну виявлено антирадикальну активність S-заміщених 2-метил-4-меркапто-8-метоксихінолінів. На цій моделі високу активність проявили водорозчинні форми – натрієві та калієві солі (сполуки 5, 6, 34). Подовження карбонового ланцюга на метиленову групу і наявність гідроксильної групи зменшує прояв антирадикальної активності (сполука 32) порівняно зі сполуками 5, 6 (рис. 2). Сполуки 5, 6 та 34 перевищують антирадикальну активність еталону порівняння – L-ацетилцистеїну.
|
|
|
Рис. 2. Антирадикальна активність S-заміщених похідних 2-метил-4-меркапто-8-метоксихіноліну (концентрація сполук 25 мкм)
Встановлено, що подовження на метиленову групу карбонового ланцюга в 4-му положенні хінолінового циклу (сполука 10) зменшує антирадикальну активність, наявність гідроксильної групи (сполука 32) – її підвищує. Етерифікація (-ОСН3) карбоксильної групи (сполука 12) призводить до зменшення прояву активності в порівнянні зі сполукою 10.
За результатами проведених досліджень виявлено, що синтезовані сполуки проявляють антирадикальні і антиоксидантні властивості.
Вільнорадикальне окиснення ліпідів. На моделях генерації вільнорадикального окиснення ліпідів in vitro S-заміщені похідні 2-метил-4-меркапто-8-метоксихіноліну знижують утворення вільних радикалів, виявляючи властивості “пасток” супероксиданіону у водній фазі, перехоплюють гідроксилрадикал у гетерогенній системі та є протекторами меркаптогруп протеїнів, включаючи ферменти антиоксидантного захисту (супероксиддисмутази, каталази, глутатіонпероксидази, знижують утворення малонового діальдегіду).
|
|
|
(Хінолін-4-ілтіо)карбонові кислоти (сполуки 1, 3) і гідрохлорид (сполука 2) на всіх моделях ініціації вільнорадикального окиснення ліпідів проявляють високу антиоксидантну активність (рис. 3).
Наявність метильної групи в α-положенні карбонового ланцюга S-заміщених 2-метил-4-меркапто-8-метоксихінолінів зменшує прояв антиоксидантної активності (сполука 3) (рис. 3). Калієва сіль 3-(8-метокси-2-метилхінолін-4-ілтіо)пропанової кислоти – сполука 15 – проявляє антиоксидантну активність в 3 рази меншу, ніж сполука 1. Наявність аміногрупи – сполука 17, N-ацетильного залишку − сполука 22 – в карбоновому ланцюзі S-заміщених 2-метил-4-меркапто-8-метоксихінолінів зменшує активність на даній моделі в порівнянні зі сполукою 1.
На моделі ферментативного ініціювання вільнорадикального окиснення ліпідів найменша кількість малонового діальдегіду утворилась в присутності сполук 2 та 3 (рис. 3), що проявляють найбільшу антиоксидантну активність (АОА). Наявність аміногрупи або N-ацетильного залишку в карбоновому ланцюзі S-заміщених похідних − сполуки 17, 22 − проявляють меншу АОА в порівнянні зі сполукою 2 та еталонами порівняння – метіоніном та унітіолом.
|
|
|
Найбільшу активність на моделі неферментативного ініціювання показала сполука 2, АОА якої перевищує активність дибунолу на 19 % (р<0,05), α-токоферолу – на 36 % (р<0,05). Введення СН3-групи в α-положення карбонового ланцюга − сполука 3, зменшує прояв АОА.
Для N-ацильних 2-метил-4-S-гетерилзаміщених 8-метоксипохідних хіноліну спостерігається зменшення АОА − сполуки 17 та 22. Калієва сіль 3-(8-метокси-2-метилхінолін-4-ілтіо)пропанової кислоти − сполука 15 – проявляє антиоксидантну активність, яка знаходиться на рівні з АОА еталону порівняння − α-токоферолу (23 та 24 % відповідно).
Найбільша антирадикальна активність на моделі інгібування NO-радикалу властива 3-(8-метокси-2-метилхінолін-4-ілтіо)оцтовій кислоті (сполука 1) та 2-(8-метокси-2-метилхінолін-4-ілтіо)пропановій кислоті (сполука 3) (63,5 та 40,8 % відповідно) в порівнянні з ацетилцистеїном. Гідрохлорид – сполука 2 – на цій моделі проявляє меншу активність, ніж кислота (35,0 та 63,5% відповідно). Водорозчинна форма – калієва сіль 3-(8-метокси-2-метилхінолін-4-ілтіо)пропанової кислоти – сполука 15 – проявляє значно меншу антирадикальну активність порівняно зі сполукою 1. N-ацильні S-заміщені 2-метил-4-меркапто-8-метоксипохідні хіноліну – сполуки 17 та 22 характеризуються проявом збільшення антирадикальної активності в порівнянні з калієвою сіллю та зменшення в порівнянні з кислотою (сполука 1).
Таким чином, на всіх моделях ініціювання вільнорадикального окиснення ліпідів спостерігається наступна залежність: подовження карбонового ланцюга залишку меркаптокарбонової кислоти на СН2-групу, наявність аміногрупи, N-ацетильного залишку в карбоновому ланцюзі в 4-му положенні хінолінового циклу, зменшує прояв антиоксидантної активності.
На всіх моделях ініціювання вільнорадикального окиснення ліпідів in vitro похідні S-заміщених 2-метил-4-меркапто-8-метоксихінолініу (сполуки 5, 14, 34 – натрієві солі) проявили антиоксидантну активність.
На моделі гальмування окиснення адреналіну спостерігається наступна залежність: подовження карбонового ланцюга на СН2-групу і поява в ньому ОН-групи в α-положенні впливає на збільшення прояву АОА на 10 – 32,5% (сполуки 14 та 34 відповідно) порівняно зі сполукою 5 (Р<0,05).
Для сполук 5, 14, 34 на моделі ферментативного ініціювання вільнорадикального окиснення ліпідів встановлено, що збільшення карбонового ланцюга на метиленову групу (сполука 14) збільшує АОА на 22,8% порівняно зі сполукою 5. Наявність гідроксигрупи в α-положенні карбонового ланцюга (сполука 34) зменшує прояв АОА на 12,8% порівняно зі сполукою 14. Всі досліджені сполуки в цьому випадку перевищують АОА препарату порівняння – унітіолу.
На моделі неферментативного ініціювання спостерігається аналогічна залежність між хімічною будовою і дією для сполук 5, 14, 34, як і на моделі інгібування супероксидрадикалу, тобто збільшення карбонового ланцюга на СН2-групу і поява ОН-групи в ньому збільшує прояв АОА.
На моделі інгібування NO-радикалу спостерігаємо таку закономірність: відбувається збільшення антирадикальної активності в ряду: сполука 5 − сполука 14 – сполука 34 (25,0, 40,0 та 55,0 % відповідно). Дві сполуки 14 та 34 перевищують активність еталону порівняння – ацетилцистеїну – на 10 та 15% відповідно (Р<0,05).
Антиоксидантна та мембраностабілізуюча активність in vivo. На основі даних комп’ютерного прогнозу і вивчення антиоксидантної активності in vitro досліджено мембраностабілізуючу та антиоксидантну активності в умовах цілісного організму (in vivo).
Найбільш виражений ефект на 14 добу дослідження мали сполуки 3 та 32 (рис. 4). При їх введенні спостерігалась стабілізація мембран гепатоцитів, про що свідчить суттєве зменшення показників активності амінотрансфераз – АлТ і АсТ, які є вірогідними по відношенню до контролю. Наявність гідроксигрупи в α-положенні карбонового ланцюга − сполука 32 − зменшує показники рівня АлТ та АсТ, наближаючи їх до інтактної групи тварин. Ці сполуки на фоні токсичного гепатиту наближають показники білоксинтезуючої активності до рівня інтактних тварин.
На моделі окисного стресу in vivo (ішемія головного мозку) введення нетоксичних S-заміщених 2-метил-4-меркапто-8-метоксихінолінів (натрієві солі) у дозі 1/50 ЛД50 (препарат порівняння − пірацетам) наближає до норми рівень показників вільнорадикального окиснення (рівень триєнкетонів), показники вуглеводного обміну (рис. 5); впливає на рівень антиоксидантних ферментів (супероксиддисмутази, каталази, глутатіонпероксидази, вміст α-токоферолу).
Сполуки, що досліджувались, по-різному впливали на рівень лактату. При дії сполуки 5 вміст лактату зменшився на 40,6% відносно контролю (Р<0,05). Збільшення ланцюга на СН2-групу в залишку карбонової кислоти (сполука 14) впливає на достовірне зменшення вмісту лактату на 43,7% (Р<0,05). Наявність ОН-групи в α-положенні карбонового ланцюга (сполука 34) зменшує рівень показника лактату на 50% відносно контролю. Всі досліджені сполуки перевищують дію еталона – пірацетаму.
Всі сполуки впливали на підвищення показників малату. Наявність залишку оцтової кислоти (сполука 5) впливає на достовірне збільшення рівня малату (на 110 %) відносно контролю. Збільшення карбонового ланцюга на СН2-групу (сполука 14) призводить до зростання вмісту малату на 140% (Р<0,05). Наявність ОН-групи в карбоновому ланцюзі (сполука 34) впливає на підвищення рівня малату на 180% відносно контролю і відповідає рівню малату інтактної групи тварин. Всі сполуки перевищують дію препарату порівняння – пірацетаму на 50-100% (Р<0,05) (рис. 5).
Важливим моментом досліджень є значне (по відношенню до контрольної групи) зниження рівня пошкоджень мозкової тканини – креатинфосфокінази – на 28,5 – 57,1% під дією натрієвих солей S-заміщених 2-метил-4-меркапто-8-метоксихінолінів, що свідчить про мембраностабілізуючу та нейропротекторну дію. За впливом на рівень ізоферменту КФК вони переважали пірацетам на 7,1 – 35,7%. Похідні хіноліну на цьому фоні зменшують витрати ендогенного антиоксиданту – α-токоферолу.
Встановлено, що збільшення карбонового ланцюга на метиленову групу (сполука 14) та наявність гідроксильної групи (сполука 34) впливає на збільшення показників і наближення до рівня показників інтактних тварин.
Захисна дія S-заміщених 2-метил-4-меркапто-8-метоксихінолінів реалізується на початкових етапах розвитку вільнорадикального окиснення при ішемії за рахунок гальмування утворення активних форм кисню, реактивації антиоксидантного комплексу та позитивного впливу на порушення біоенергетичних процесів. Можливо, в механізмі антиоксидантної, мембраностабілізуючої і нейропротекторної дії найбільш активних сполук – натрієвих солей S-заміщених похідних 2-метил-4-меркапто-8-метоксихіноліну – бере участь атом сірки залишку тіогліколевої кислоти, 3-меркаптопропанової кислоти, як замісники з потенційно високими антиоксидантними властивостями, а також карбоксильна, гідроксильна група та ендогенний атом азоту (метильна група в 2-му положенні хіноліну підсилює основність азоту). Це свідчить про те, що вони приймають участь у хелатоутворенні і здатні зв’язувати метали змінної валентності – прооксиданти – гальмують процеси вільнорадикального окиснення в реакціях Фентона і Габера-Вейса.
Синтез та вивчення специфічної активності натрієвої солі 2-гідрокси-3-(8-метокси-2-метилхінолін-4-ілтіо)пропанової кислоти. На основі проведених досліджень нами встановлено, що натрієва сіль 2-гідрокси-3-(8-метокси-2-метилхінолін-4-ілтіо)пропанової кислоти (сполука 34) малотоксична, проявляє високу антирадикальну і антиоксидантну активність in vitro. Тому вона була обрана для поглибленого вивчення специфічної дії in vivo.
Для доклінічного дослідження натрієву сіль 2-гідрокси-3-(8-метокси-2-метилхінолін-4-ілтіо)пропанової кислоти синтезовано нами за схемою 3.
Гостра токсичність (ЛД50) цієї сполуки становить <1000 мг/кг.
За результатами дослідження її специфічної активності встановлено, що сполука 34 знижує показники окисного стресу при гострому порушенні мозкового кровообігу, проявляє антиоксидантну активність та ефективно захищає мембрани клітин печінки, перевищуючи ефект пірацетаму.
Кількість дієнових кон’югатів у тканинах головного мозку при введенні сполуки 34 зменшувалася на 55,5%, триєнкетонів – на 61,5%, малонового діальдегіду – на 53,7% відповідно (Р<0,05), що на 27,8%, 19,2% та 22,7% перевищувало дію еталона порівняння – пірацетаму (Р<0,05).
У тканинах головного мозку активність супероксиддисмутази підвищувалася на 120,3%, що на 81,4% більше показника пірацетаму. Зростала активність глутатіонпероксидази на 85,6%, що перевищує дію пірацетаму на 61% (Р<0,05).
При введенні сполуки 34 тваринам з експериментальною ішемією головного мозку спостерігалася нормалізація рівня каталази і вмісту a-токоферолу. Рівень a-токоферолу зростав на 100% порівняно з контролем. Це перевищувало дію препарату порівняння − пірацетаму на 35,0% (Р<0,05).
Сполука 34 збільшує показники окисної продукції енергії – рівень лактату на 50,0%, пірувату на 111,1%, малату на 180,0% порівняно з контролем (Р<0,05). При цьому спостерігалося збільшення показників вуглеводного обміну порівняно з пірацетамом.
Пошкодження структурної цілісності клітинних мембран супроводжувалося збільшенням активності ВВ-ізоформи КФК. Наслідком антиоксидантного ефекту та позитивної реакції на порушення тонких ланок метаболізму була нейропротекторна дія щодо клітинних мембран мозкової тканини, про що свідчить зниження гіперферментації ВВ-КФК.
Порівнюючи антиоксидантну дію сполуки 34 з дією еталону порівняння − пірацетамом при гострому порушенні мозкового кровообігу, встановлено, що вона реалізує свій ефект як на початкових етапах вільнорадикального окиснення, так і на вільнорадикальному етапі розвитку ВРО, а також на етапі пероксидації.
Дуже важливо, що на фоні використання сполуки 34 не спостерігалося загибелі експериментальних тварин на моделі гострого порушення мозкового кровообігу.
Таким чином, натрієва сіль 2-гідрокси-3-(8-метокси-2-метилхінолін-4-ілтіо)пропанової кислоти може бути використана в медичній та ветеринарній практиці як перспективний антиоксидант і нейропротектор.
ВИСНОВКИ
1. У дисертації наведено теоретичне узагальнення і нове вирішення наукової задачі, що виявляється у пошуку ефективних біорегуляторів серед S-заміщених похідних 2-метил-4-меркапто-8-метоксихіноліну, у результаті чого знайдені сполуки з антиоксидантними, мембраностабілізуючими, нейропротекторними властивостями.
2. Комп’ютерний прогноз біологічної активності за допомогою програми “PASS” показав доцільність пошуку серед похідних хіноліну речовин з різнобічною біологічною активністю та дав можливість поповнити банк даних комп’ютерних програм новими дескрипторними центрами.
3. Синтезовано 35 нових S-заміщених похідних 2-метил-4-меркапто-8-метоксихіноліну та вивчено їх фізико-хімічні властивості й біологічну активність в модельних дослідах in vitro та in vivo.
4. Встановлено, що ЛД50 отриманих похідних знаходиться в межах 566 − 2000 мг/кг, тобто вони відносяться до мало- та нетоксичних сполук. Наявність N–ацетильних залишків в 4-му положенні хінолінового циклу або гідроксигрупи в карбоновому ланцюзі зменшує токсичність. Етерифікація карбоксильної групи залишку оцтової кислоти збільшує гостру токсичність сполук, а пропанової − зменшує її.
5. У дослідах in vitro виявлена властивість S-заміщених 2-метил-4-меркапто-8-метоксихінолінів виконувати функцію “пасток” супероксиданіона у водній фазі, “пасток” гідроксилрадикала у гетерогенних системах та захист антиоксидантних ферментів. Усі досліджені сполуки гальмують утворення активних форм оксиду азоту. Ступінь прояву антиоксидантних властивостей залежить від природи залишків карбонових кислот у 4-му положенні хінолінового циклу.
6. Встановлено, що найбільш виражена мембранозахисна дія in vivo властива 2-гідрокси-3-(8-метокси-2-метилхінолін-4-ілтіо)пропановій кислоті, наближає до норми рівень ферментативної активності та білоксинтезуючу функцію печінки.
7. Показано, що S-заміщені похідні 2-метил-4-меркапто-8-метоксихіноліну in vivo (модель двосторонньої перев’язки загальної сонної артерії) проявляють властивості ефективних біорегуляторів з антиоксидантною, нейропротекторною дією і переважають еталон порівняння – пірацетам.
8. Розроблено зручний метод синтезу та проведені доклінічні дослідження натрієвої солі 2-гідрокси-3-(8-метокси-2-метилхінолін-4-ілтіо)пропанової кислоти. Встановлено, що сполука має виражену антиоксидантну та нейропротекторну активність. Зокрема, вона знижує активність вільнорадикальних процесів, нормалізує енергетичні процеси і відновлює ферментну систему антиоксидантного захисту.
Дата добавления: 2019-07-15; просмотров: 210; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
