Практическая работа №2 «Синтез неорганического вещества»
Класс
Практическая работа №2 «Синтез неорганического вещества»
Группа 1
Получение оксида меди ( II )
Оксид меди (II) можно получить термическим разложением гидроксокарбоната меди (II):
t°
(CuOH)2CO3 → 2СuO + CO2 + H2O.
Оборудование и реактивы: штатив, 2 муфты, кольцо, лапка, латунная сетка, пробирка, пробка с газоотводной трубкой, спиртовка, спички, 2 стакана (50-100 мл), лучина, (CuOH)2CO3, известковая вода (насыщенный раствор Ca(OH)2).
Опыт. Реакцию разложения гидроксокарбоната меди (II) можно провести в приборе, изображенном на рисунке:

Последовательность выполнения операций:
1) порошкообразный гидроксокарбонат меди (II) помещают в пробирку, заполнив им примерно 1/5 ее объема;
2) закрывают пробирку пробкой с газоотводной трубкой;
3) пробирку укрепляют в штативе в наклонном положении, чтобы вода, образующаяся в реакции, могла стекать по газоотводной трубке (см. рисунок);
4) газоотводную трубку опускают в стакан;
5) нагревают пробирку в пламени спиртовки (сначала нужно прогреть ее по всей длине, потом сосредоточить нагревание в той зоне, где протекает реакция).
О течении реакции можно судить по изменению цвета вещества, нагреваемого в пробирке, образованию капель воды на ее стенках и выделению углекислого газа, который можно обнаружить, опустив в стакан горящую лучинку: она погаснет.
Об окончании реакции можно судить, опустив конец газоотводной трубки в стакан с известковой водой. Если разложение не кончилось, должен выделяться углекислый газ, который реагирует с известковой водой (образуется «муть»).
ё
Вопросы. 1) К какому классу солей принадлежит гидроксокарбонат меди (II)?
2) Напишите уравнение реакции взаимодействия углекислого газа с известковой водой.
8 класс
Практическая работа №2 «Синтез неорганического вещества»
Группа 2
Получение хлорида магния
Хлорид магния можно получить взаимодействием магния с соляной кислотой.
Оборудование и реактивы: пробирка, фарфоровая чашка, штатив, муфта, кольцо, спиртовка, спички, Mg (стружки), HCl (1:5)
Опыт. В пробирку помещают магний, затем постепенно приливают около 3 мл раствора соляной кислоты до полного растворения магния.
По окончании реакции раствор переливают в фарфоровую чашку и выпаривают (см. рисунок):

Вопросы. 1) Напишите уравнение реакции взаимодействия магния с соляной кислотой.
2) Каким еще способом разделения смесей можно было бы воспользоваться, чтобы отделить воду и хлорид магния друг от друга?
8 класс
Практическая работа №2 «Синтез неорганического вещества»
Группа 3
Получение гидроксида меди ( II )
Гидрокисид меди (II) может быть получен в результате взаимодействия хлорида меди (II) с гидроксидом натрия.
Оборудование и реактивы: стакан (100 мл), мерный цилиндр (50 мл), стеклянная палочка с резиновым наконечником, водоструйный насос, колба Бунзена, воронка Бюхнера, шланги резиновые толстостенные, фильтр бумажный, CuCl2 (тв.), NaOH (5%-ный раствор), H2O (дистиллированная).
Опыт. Последовательность выполнения операций:
1) в стакан помещают 1,78 г хлорида меди (II), растворяют его в 30 мл дистиллированной воды;
2) к полученному раствору осторожно приливают 20 мл 5%-ного раствора гидроксида натрия, тщательно перемешивают и дают жидкости отстояться;
3) осадок отфильтровывают и сушат.
Фильтрование жидкостей, смешанных со студенистым осадком или мелкокристаллическим веществом, проходит очень медленно. Его можно ускорить, если отсасывать жидкость из воронки. Для этого используется специальное лабораторное оборудование – воронка Бюхнера (фарфоровая воронка с дырчатой перегородкой), которая подсоединяется к колбе Бунзена (толстостенной колбе с боковым отводом). Из колбы Бунзена при помощи водоструйного насоса высасывается воздух, вследствие чего давление в ней становится меньше атмосферного. Следовательно, на поверхности жидкости в воронке воздух оказывает большее давление, чем снизу. Благодаря этому процесс фильтрования ускоряется. Подобный способ фильтрования называют фильтрованием под вакуумом.
Установка для фильтрования под вакуумом изображена на рисунке:

Последовательность операций при фильтровании под вакуумом:
1) положить фильтр на воронку Бюхнера, смочить его дистиллированной водой;
2) включить водоструйный насос;
3) постепенно приливать фильтруемую жидкость в воронку Бюхнера;
4) после окончания фильтрования на некоторое время оставить осадок для просушивания;
5) отсоединить шланг от колбы Бунзена;
6) выключить водоструйный насос.
Вопросы. 1) Напишите уравнение реакции получения гидроксида меди (II).
2) Можно ли высушить полученный осадок, поместив в фарфоровую чашку и нагрев в пламени спиртовки?
8 класс
Практическая работа №2 «Синтез неорганического вещества»
Группа 4
Получение кремниевой кислоты
Кремниевая кислота может быть получена в результате взаимодействия силиката натрия с соляной кислотой.
Оборудование и реактивы: стакан (100 мл), 2 мерных цилиндра (50 мл), стеклянная палочка с резиновым наконечником, водоструйный насос, колба Бунзена, воронка Бюхнера, шланги резиновые толстостенные, фильтр бумажный, Na2SiO3 (10%-ный раствор), HCl (1:5), H2O (дистиллированная).
Опыт. Последовательность выполнения операций:
1) при помощи мерных цилиндров отмеряют 25 мл раствора соляной кислоты и 50 мл раствора силиката натрия;
2) выливают в стакан раствор силиката натрия, за ним – раствор соляной кислоты и сразу же энергично размешивают стеклянной палочкой, палочку оставляют в стакане;
3) полученный гель кремниевой кислоты тщательно промывают на фильтре водой и оставляют на несколько дней сушиться на воздухе.
Фильтрование жидкостей, смешанных со студенистым осадком или мелкокристаллическим веществом, проходит очень медленно. Его можно ускорить, если отсасывать жидкость из воронки. Для этого используется специальное лабораторное оборудование – воронка Бюхнера (фарфоровая воронка с дырчатой перегородкой), которая подсоединяется к колбе Бунзена (толстостенной колбе с боковым отводом). Из колбы Бунзена при помощи водоструйного насоса высасывается воздух, вследствие чего давление в ней становится меньше атмосферного. Следовательно, на поверхности жидкости в воронке воздух оказывает большее давление, чем снизу. Благодаря этому процесс фильтрования ускоряется. Подобный способ фильтрования называют фильтрованием под вакуумом.
Установка для фильтрования под вакуумом изображена на рисунке:
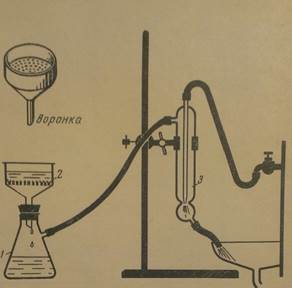
Последовательность операций при фильтровании под вакуумом:
7) положить фильтр на воронку Бюхнера, смочить его дистиллированной водой;
8) включить водоструйный насос;
9) постепенно приливать фильтруемую жидкость в воронку Бюхнера;
10) после окончания фильтрования на некоторое время оставить осадок для просушивания;
11) отсоединить шланг от колбы Бунзена;
12) выключить водоструйный насос.
После опытов с силикатом натрия всю посуду сейчас же тщательно моют, так как раствор этой соли сильно разъедает стекло!
Вопросы. 1) Напишите уравнение реакции получения кремниевой кислоты.
2) Однородной или неоднородной смесью является гель кремниевой кислоты? Какие вещества входят в состав этого геля?
При выполнении практической работы №2 класс делится на 4 группы. Каждая группа получает задание синтезировать определенное неорганическое вещество. Между членами группы распределяются роли:
1) экспериментаторы (группа 1 – 4 человека, группа 2 – 2 человека, группа 3 – 4 человека, группа 4 – 3 человека) составляют план эксперимента, договариваются между собой, в какой последовательности они будут выполнять операции с веществами и посудой, указанные в методике, отчитываются учителю, затем проводят эксперимент;
2) секретарь (по 1 человеку в каждой группе) следит за ходом эксперимента и письменно оформляет практическую работу; все остальные после того, как выполнят свои задания, переписывают работу у секретаря;
3) докладчик (по 1 человеку в каждой группе) следит за ходом эксперимента, готовит по нему устный отчет, после того, как все 4 группы закончат работу, выступает (регламент 1,5 – 3 мин.); члены групп имеют право задавать докладчику вопросы, касающиеся проведенных его командой опытов;
4) рецензент (по 1 человеку в каждой группе) следит за ходом эксперимента, отмечает положительные и отрицательные стороны работы команды, наиболее легкие и трудные в исполнении элементы практической работы, выступает после докладчика (регламент 1 – 2 мин.);
5) ответственный за соблюдение техники безопасности (по 1 человеку в каждой группе) следит за соблюдением техники эксперимента и правил безопасного обращения с реактивами и оборудованием.
Дата добавления: 2019-01-14; просмотров: 531; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
