Вопросы и задания для контроля
Лабораторная работа 2.6 «Изучение температурной зависимости электрического сопротивления электролита »
Теоретические основы
Основные понятия, определения и формулы
1. Электролиты – это вещества, которые проводят электрический ток вследствие диссоциации их молекул на ионы (это происходит в растворах и расплавах).
2. Диссоциацией называется распад нейтральных молекул вещества на положительные и отрицательные ионы.
3. Рекомбинацией называется процесс, обратный диссоциации – воссоединение ионов при их столкновении с образованием нейтральных молекул. В электролитах при фиксированной температуре устанавливается определенное динамическое равновесное состояние, при котором число ионов в единице объема можно считать неизменным.
4. Коэффициент диссоциации численно равен доле молекул вещества, распавшихся на ионы:  , где n – концентрация распавшихся молекул вещества, n0 – концентрация молекул растворенного вещества
, где n – концентрация распавшихся молекул вещества, n0 – концентрация молекул растворенного вещества
Цель работы — ознакомиться с закономерностями прохождения электрического тока через электролиты; экспериментально изучить зависимость сопротивления электролита от температуры и определить температурный коэффициент сопротивления электролита.
Вопросы для допуска к лабораторной работе
1. Сформулировать цель работы.
2. Какие вещества называются электролитами?
3. Какими носителями электрического заряда создается электрический ток в растворах или расплавах электролитов?
|
|
|
4. Как происходит процесс электролитической диссоциации молекул?
5. Что называется коэффициентом диссоциации и от чего он зависит?
6. Какой процесс называется рекомбинацией?
Методика и порядок измерений
Прохождение электрического тока через электролит сопровождается выделением веществ на электродах. Это явление получило название электролиза.
Электрический ток в электролитах представляет собой перемещение ионов обоих знаков в противоположных направлениях. Положительные ионы движутся к отрицательному электроду (катоду), отрицательные ионы — к положительному электроду (аноду).
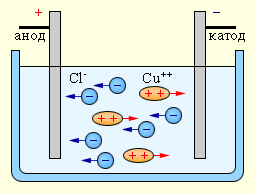
| Рисунок — Электролиз водного раствора хлорида меди |
Ионы обоих знаков появляются в водных растворах солей, кислот и щелочей в результате расщепления части нейтральных молекул. Это явление называется электролитической диссоциацией. Например, хлорид меди CuCl2 диссоциирует в водном растворе на ионы меди и хлора:  . Следует отметить, что процесс диссоциации молекул растворенного вещества происходит вследствие взаимодействия их с молекулами растворителя, т.е. он происходит и в отсутствии внешнего электрического поля. Силы межмолекулярного взаимодействия имеют электростатическую природу.
. Следует отметить, что процесс диссоциации молекул растворенного вещества происходит вследствие взаимодействия их с молекулами растворителя, т.е. он происходит и в отсутствии внешнего электрического поля. Силы межмолекулярного взаимодействия имеют электростатическую природу.
|
|
|
При подключении электродов к источнику тока ионы под действием электрического поля начинают упорядоченное движение: положительные ионы меди движутся к катоду, а отрицательно заряженные ионы хлора — к аноду (см. рис. 1).
Достигнув катода, ионы меди нейтрализуются избыточными электронами катода и превращаются в нейтральные атомы, оседающие на катоде. Ионы хлора, достигнув анода, отдают по одному электрону. После этого нейтральные атомы хлора соединяются попарно и образуют молекулы хлора Cl2. Хлор выделяется на аноде в виде пузырьков.
Наряду с диссоциацией молекул происходит и обратный процесс — воссоединение ионов при их столкновениях (рекомбинация). При каждой температуре устанавливается определенное равновесное состояние, при котором число ионов в единице объема приблизительно постоянно. Отношение концентрации распавшихся на ионы молекул (n) к концентрации молекул растворенного вещества (n0)  называется коэффициентом диссоциации; он показывает, какая доля молекул растворенного вещества распалась. Коэффициент диссоциации зависит от концентрации раствора, от рода растворителя и от температуры. С повышением температуры α увеличивается. Молекулы растворителя обволакивают ион, образуя вокруг него сольватную оболочку. Это, во-первых, затрудняет рекомбинацию ионов, во-вторых, затрудняет движение ионов — фактически в растворе движется сольват — шарик, состоящий из иона и сольватной оболочки вокруг него.
называется коэффициентом диссоциации; он показывает, какая доля молекул растворенного вещества распалась. Коэффициент диссоциации зависит от концентрации раствора, от рода растворителя и от температуры. С повышением температуры α увеличивается. Молекулы растворителя обволакивают ион, образуя вокруг него сольватную оболочку. Это, во-первых, затрудняет рекомбинацию ионов, во-вторых, затрудняет движение ионов — фактически в растворе движется сольват — шарик, состоящий из иона и сольватной оболочки вокруг него.
|
|
|
При наличии внешнего электрического поля плотность тока в электролите определяется выражением: j=q+n+u++q  n
n  u
u  , где q+, q
, где q+, q  — величина зарядов положительных и отрицательных ионов, n+, n
— величина зарядов положительных и отрицательных ионов, n+, n  — их концентрация, u+, u
— их концентрация, u+, u  — их скорости направленного движения. Заряд иона кратен элементарному заряду (e=1,6
— их скорости направленного движения. Заряд иона кратен элементарному заряду (e=1,6  Кл): q=ez, где z – валентность иона. Из закона сохранения электрического заряда следует q+n+= q
Кл): q=ez, где z – валентность иона. Из закона сохранения электрического заряда следует q+n+= q  n
n  =qn,последнее выражение определяет суммарный заряд ионов одного знака в единице объема. Тогда плотность тока j=qn
=qn,последнее выражение определяет суммарный заряд ионов одного знака в единице объема. Тогда плотность тока j=qn  .
.
Скорость упорядоченного движения сольвата можно найти из следующих соображений. В электрическом поле на сольват вдоль направления движения действуют электрическая сила  и сила внутреннего трения жидкости
и сила внутреннего трения жидкости  , где
, где  — радиус сольвата,
— радиус сольвата, 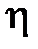 — коэффициент вязкости жидкости. При установившемся движении
— коэффициент вязкости жидкости. При установившемся движении 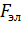 =
=  , откуда
, откуда  =bE, где
=bE, где  — подвижность иона, т.е. подвижность иона численно равна скорости направленного движения соответствующего иона при напряженности электрического поля, равной единице. В общем случае подвижности ионов противоположных знаков не одинаковы.
— подвижность иона, т.е. подвижность иона численно равна скорости направленного движения соответствующего иона при напряженности электрического поля, равной единице. В общем случае подвижности ионов противоположных знаков не одинаковы.
|
|
|
С учетом вышесказанного выражение для плотности тока принимает вид j=qn 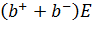 . Отсюда следует, что для электролитов также выполняется закон Ома
. Отсюда следует, что для электролитов также выполняется закон Ома  , где удельная электропроводность
, где удельная электропроводность  = qn
= qn 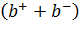 =
=  qn0
qn0 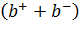 . Удельное сопротивление электролита
. Удельное сопротивление электролита  . С повышением температуры сопротивление электролита довольно быстро убывает, поскольку возрастает коэффициент диссоциации и уменьшается вязкость электролита.
. С повышением температуры сопротивление электролита довольно быстро убывает, поскольку возрастает коэффициент диссоциации и уменьшается вязкость электролита.
В небольших интервалах температур можно приближенно считать, что сопротивление электролита уменьшается линейно с ростом температуры. В этом приближении зависимость сопротивления  электролита от температуры
электролита от температуры 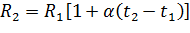 , где R1 и R2 — сопротивления электролита соответственно при температурах t1 и t2,
, где R1 и R2 — сопротивления электролита соответственно при температурах t1 и t2,  — средний температурный коэффициент сопротивления, численно равный относительному изменению сопротивления электролита, при изменении температуры электролита на 1
— средний температурный коэффициент сопротивления, численно равный относительному изменению сопротивления электролита, при изменении температуры электролита на 1  . Таким образом, измерив сопротивление электролита при двух различных температурах, можно приближенно определить его температурный коэффициент сопротивления.
. Таким образом, измерив сопротивление электролита при двух различных температурах, можно приближенно определить его температурный коэффициент сопротивления.
Измерения
Электрическая схема, общий вид лабораторной установки и порядок выполнения работы показаны в дополнении к работе, находящемся на рабочем месте. Учитывая дополнение, проделайте следующее.
1. Измерьте сопротивление электролита при его нагревании от 20  до 80
до 80  через каждые 10
через каждые 10  . Результаты измерений занесите в таблицу.
. Результаты измерений занесите в таблицу.
2. Измерьте сопротивление того же электролита при его остывании от 80  до 20
до 20  через каждые 10
через каждые 10  . Результаты измерений занесите в таблицу.
. Результаты измерений занесите в таблицу.
3. Рассчитайте среднее значение сопротивления при каждой температуре.
4. По средним значениям сопротивления вычислите 3 значения температурного коэффициента сопротивления  для различных температурных интервалов.
для различных температурных интервалов.
Таблица
| t | 20 | 30 | 40 | 50 | 60 | 70 | 80 | |
| R, Ом | нагревание | |||||||
| остывание | ||||||||
|
| ||||||||
Расчет температурного коэффициента сопротивления | ||||
t1 
| R1, Ом | t2 
| R2, Ом |  , К-1 , К-1
|
5. По экспериментальным данным постройте график зависимости Rср (t).
6. Запишите найденное значение в виде:  . Сформулируйте вывод по работе.
. Сформулируйте вывод по работе.
.
Вопросы и задания для контроля
I уровень
1. Сформулируйте определение и запишите выражение для температурного коэффициента сопротивления электролита.
2. В каких единицах измеряется температурный коэффициент сопротивления?
3. Что является носителям зарядов в электролитах?
4. В результате чего появляются в электролитах ионы?
5. Опишите процесс диссоциации в жидких электролитах.
6. Что является количественной характеристикой процесса диссоциации?
7. Что называется подвижностью иона?
8. Одинаковая ли подвижность положительных и отрицательных ионов в электролитах?
II уровень
9. Объясните полученную Вами экспериментально зависимость сопротивления электролита от температуры.
10. Выполняется ли для электролита закон Ома?
11. Получите аналитическое выражение закона Ома в дифференциальной форме для электрического тока в электролитах.
12. Воздух между плоскими электродами ионизационной камеры ионизируется рентгеновским излучением. Сила тока, текущего через камеру, равна 1,5 мкА. Площадь каждого электрода равна 300 см2 , расстояние между ними 2 см, разность потенциалов 100 В. Найти концентрацию пар ионов между пластинами, если ток далек от насыщения. Подвижность положительных ионов 1,4  и отрицательных 1,9
и отрицательных 1,9  . Заряды ионов равны элементарному заряду.
. Заряды ионов равны элементарному заряду.
Дата добавления: 2019-01-14; просмотров: 223; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!

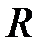 ср, Ом
ср, Ом