МАКСИМАЛЬНО СОКРАЩЕННАЯ (МАКСИМАЛЬНО УКОРОЧЕННАЯ) ДЫХАТЕЛЬНАЯ ЦЕПЬ.
Она представлена только цитохромной частью. Эксперименты показали, что здесь может быть окислен только один субстрат - аскорбиновая кислота, с участием фермента, восстановленные эквиваленты включаются в цепь на уровне цитохрома С цитохромоксидазы (цитохром аа3), но в реальных условиях такого окисления практически не происходит. Образуется вода и 1 молекула АТФ. Коэффициент Р/О=1.
Возможность такого окисления доказана в эксперименте in vitro. А в живой клетке аскорбиновая кислота обычно используется как донор водорода в системе окисления оксигеназного типа (реакции, катализируемые монооксигеназами: смотрите лекцию «Внемитохондриальное окисление»). Такие реакции с участием витамина «С» особенно важны для формирования белка коллагена, в котором за счет монооксигеназной реакции образуется гидроксипролин.
ОКИСЛИТЕЛЬНОЕ ДЕКАРБОКСИЛИРОВАНИЕ ПИРОВИНОГРАДНОЙ
И a-КЕТОГЛУТАРОВОЙ КИСЛОТ В МИТОХОНДРИЯХ
Этот вариант дыхательной цепи удлинен по сравнению с полной цепью за счет того, что первое звено катализируется не никотинамидным ферментом, а мультиферментным комплексом. Это единая надмолекулярная структура. В состав этого комплекса входят 3 фермента и 5 коферментов. Такой комплекс называется мультиферментным комплексом окислительного декарбоксилирования a -кетокислот, и он окисляетдва субстрата:
1. Пировиноградную кислоту (пируват, ПВК)
|
|
|
Окисляется с помощью ферментов пируватдегидрогеназного комплекса;
2. a-кетоглутаровую кислоту (a-КГ)
Окисляется с помощью ферментов a-кетоглутаратдегидрогеназного комплекса.
Оба комплекса ферментов работают одинаково. Они катализируют реакции окислительного декарбоксилирования соответствующей a-кетокислоты.
ОКИСЛИТЕЛЬНОЕ ДЕКАРБОКСИЛИРОВАНИЕ ПИРУВАТА
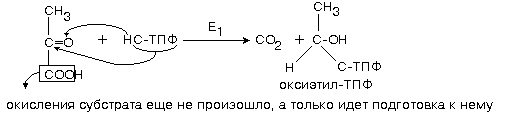
1-ю реакцию катализирует фермент ПИРУВАТДЕКАРБОКСИЛАЗА (Е1).
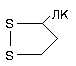
Простетической группой пируватдекарбоксилазы является тиаминдифосфат (ТПФ, тиаминпирофосфат, ТДФ) - это активная форма витамина В1. Активная часть ТПФ - тиазоловое кольцо и атом водорода в нем. Для краткости записывают: НС-ТПФ.
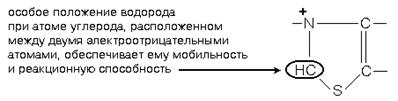
Пируватдекарбоксилаза отщепляет CO2, а оставшаяся оксиэтильная группа присоединяется к ТПФ.
|
|
2-ю и 3-ю реакцию процесса катализирует фермент АЦИЛТРАНСФЕРАЗА (Е2). Простетическая группа ацетилтрансферазы - амид липоевой кислоты. Катализирует перенос оксиэтильного остатка на свой собственный кофермент (строение ЛК знать описательно по учебнику). В ее составе есть дисульфидная связь.

На этом этапе уже произошло окисление оксиэтильного остатка до остатка уксусной кислоты, одновременно с этим началось восстановление липоевой кислоты.
|
|
|
3 этап - продолжает работать фермент ацилтрансфераза.
На этой стадии фермент переносит остаток уксусной кислоты на молекулу кофермента А (КоА). В КоА содержится остаток пантотеновой кислоты (витамин В3). Активной частью КоА является остаток тиоэтаноламина и его -SH группа.
Выяснено, что этот фермент переносит не только остатки уксусной кислоты, но и остатки других кислот (нециклических). Поэтому его еще называют коферментом ацилирования.

Второй фермент данного комплекса является не только ацетилтрансферазой, но и окислительным ферментом одновременно (дегидрогенизирующая ацетилтрансфераза).
Энергия этого окисления аккумулируется в виде макроэргической связи активной формы уксусной кислоты (ацетил-КоА).
4 этап катализируется ферментом ДИГИДРОЛИПОИЛДЕГИДРОГЕНАЗОЙ.
Кофермент этого этапа - особый ФАД с низким окислительно-восстановительным потенциалом (обозначается как ФАД'). Переносит протоны и электроны с дигидролипоата на НАД - последний кофермент в описанном комплексе.
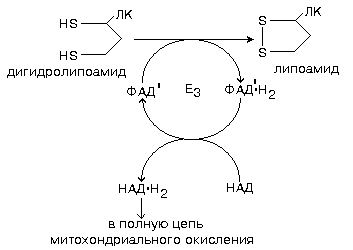
В итоге можем записать суммарное уравнение:
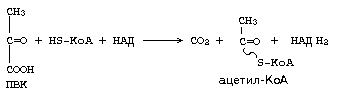
Аналогично действует ферментный комплекс для окислительного декарбоксилирования a-кетоглутарата. Но названия двух из трех ферментов другие:
|
|
|
1-й фермент - декарбоксилаза a-кетоглутаровой кислоты
2-й фермент - сукцинилтрансфераза (переносит остаток янтарной кислоты)
Суммарное уравнение для этого комплекса:


В результате действия этих двух комплексов, каждый из двух приведенных субстратов (ПВК и a-КГ) - теряют СО2, два протона и два электрона, которые передаются на кислород с образованием Н2О и параллельно происходит фосфорилирование трех молекул АТФ. Сами субстраты превращаются в итоге в активную форму соответствующей кислоты.
Макроэргическая связь в молекулах этих активных форм может легко трансформироваться в макроэргическую связь молекулы АТФ. Например, для молекулы сукцинил-КоА:
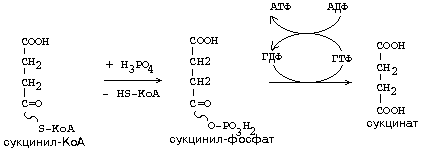
Такой способ образования АТФ, когда нет сопряжения с процессами окисления, называется СУБСТРАТНЫМ ФОСФОРИЛИРОВАНИЕМ (при этом используется макроэргическая связь в молекуле какого-нибудь субстрата). В организмах высших животных и человека этот путь получения АТФ не является главным. Благодаря такому механизму окислительное декарбоксилирование a-кетокислот может считаться энергетически более выгодной, потому что образуется вещество с макроэргической связью - ацетил-КоА. Некоторые синтетазы используют макроэргические связи из Ацетил-КоА или Сукцинил-КоА для реакций биосинтеза.
|
|
|
Например, при синтезе гема гемоглобина используется часть молекул сукцинил-КоА:
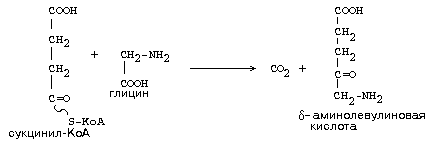
Большая часть будет все же использоваться для синтеза ГТФ.
Другой продукт окислительного декарбоксилирования (Ацетил-КоА) может расходоваться в реакциях синтеза жирных кислот, холестерина, стероидов. А самая большая часть этого вещества используется при синтезе лимонной кислоты в реакциях Цикла Трикарбоновых Кислот.
ЭНЕРГЕТИЧЕСКИЙ ИТОГ УДЛИНЕННОЙ ЦЕПИ.
Образуются 3 молекулы АТФ путем окислительного фосфорилирования. Продукты окислительного декарбоксилирования (ацетил-КоА и сукцинил-КоА) содержат макроэргическую связь. Энергия макроэргической связи сукцинил-КоА используется двумя способами.
1) Субстратное фосфорилирование в ЦТК (так расходуется большая часть этого вещества).
2) Реакции синтеза гема (меньшая часть сукцинил-КоА).
Энергия макроэргической связи Ацетил-КоА используется только в реакциях синтеза:
а) Синтез лимонной кислоты (цитрата).
б) Синтез кетоновых тел
в) Синтез жирных кислот
г) Синтез холестерина
Среди субстратов МтО почти нет веществ, которые организм получает с пищей - только глутаминовая кислота.
Субстраты МтО - в основном органические кислоты, которые образуются в организме в процессе катаболизма. В процессе катаболизма из большого количества разнообразных пищевых веществ образуется всего 2 вида общих метаболитов: Ацетил-КоА и ПВК.
ЦИКЛ ТРИКАРБОНОВЫХ КИСЛОТ
(ЦТК, лимоннокислый цикл, цикл Кребса)
ЦТК, как и реакции митохондриального окисления, протекает в митохондриях. Представляет собой серию реакций, замкнутых в цикл.

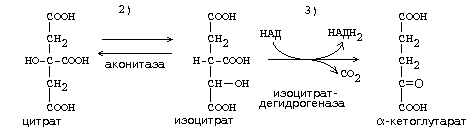
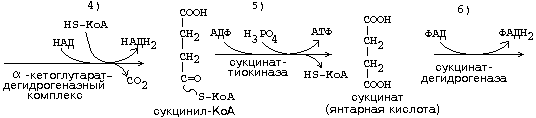
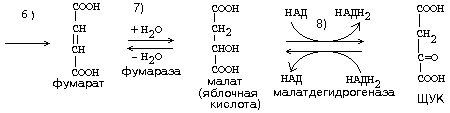
Образовавшиеся молекулы ЩУК реагируют с новой молекулой Ацетил-КоА и цикл повторяется вновь от образования цитрата до его превращения в ЩУК.
В реакциях этого цикла участвуют четыре из девяти субстратов МтО.
Происходит серия дегидрогеназных реакций. Из них 3-я, 4-я и 8-я происходят с участием НАД-зависимых дегидрогеназ, и каждая из этих реакций позволяет получить 3 молекулы АТФ. На 6-й стадии происходит ФАД-зависимая дегидрогеназная реакция, которая сопряжена с образованием 2-х молекул АТФ (Р/О = 2).
На 5-й стадии 1 молекула АТФ образуется путем субстратного фосфорилирования.
Итого за 1 оборот ЦТК образуется 12 молекул АТФ.
Смысл ЦТК заключается в том, чтобы остатки уксусной кислоты расщепились с образованием большого количества АТФ. Кроме того, из ацетатных остатков образуется СО2 и Н2О, как конечные продукты обмена веществ.
СО2 образуется в ходе ЦТК дважды:
1. на третьей стадии (окисление изоцитрата)
2. на четвертой стадии (окисление альфа-кетоглутарата).
Если прибавить еще 1 молекулу СО2, которая образуется до начала ЦТК - при превращении ПВК в Ацетил-КоА, то можно говорить о трех молекулах СО2, образующихся при распаде ПВК. Суммарно эти молекулы, образующиеся при распаде ПВК, составляют до 90% углекислоты, которая выводится из организма.
ИТОГОВОЕ УРАВНЕНИЕ ЦТК
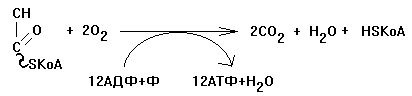
БИОЛОГИЧЕСКОЕ ЗНАЧЕНИЕ ЦТК
ГЛАВНАЯ РОЛЬ ЦТК - ОБРАЗОВАНИЕ БОЛЬШОГО КОЛИЧЕСТВА АТФ.
1. ЦТК - главный источник АТФ. Энергию для образования большого количества АТФ дает полный распад Ацетил-КоА до СО2 и Н2О.
2. ЦТК - это универсальный терминальный этап катаболизма веществ всех классов.
3. ЦТК играет важную роль в процессах анаболизма (промежуточные продукты ЦТК):
- из цитрата -------> синтез жирных кислот
- из aльфа-кетоглутарата и ЩУК ---------> синтез аминокислот
- из ЩУК ----------> синтез углеводов
- из сукцинил-КоА -----------> синтез гема гемоглобина
АВТОНОМНАЯ САМОРЕГУЛЯЦИЯ ЦТК
В ЦТК два ключевых фермента:
1) цитратсинтаза (1-я реакция)
2) изоцитратдегидрогеназа (3-я реакция)
Оба фермента аллостерически ингибируются избытком АТФ и НАДН2. Изоцитратдегидрогеназа сильно активируется АДФ. Если АДФ нет, то этот фермент неактивен. В условиях энергетического покоя концентрация АТФ увеличивается, и скорость реакций ЦТК мала - синтез АТФ уменьшается.
Изоцитратдегидрогеназа ингибируется АТФ намного сильнее, чем цитратсинтаза, поэтому в условиях энергетического покоя повышается концентрация цитрата, и он выходит в цитоплазму по градиенту концентраций путем облегченной диффузии. В цитоплазме цитрат превращается в Ацетил-КоА, который участвует в синтезе жирных кислот.
Дата добавления: 2018-11-24; просмотров: 550; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!