Алмаз как материал для изготовления инструментов
80 % добываемых природных алмазов и все синтетические алмазы используются в качестве инструментальных материалов.
Основное количество алмазов используется в виде алмазного порошка для изготовления алмазно-абразивного инструмента – шлифовальных кругов, притиров, хонов, надфилей и др., для обработки особо твердых металлов и горных пород. Большое значение имеют заточные круги для твердосплавного инструмента, это увеличивает производительность труда и срок службы инструмента. Повышение стойкости твердосплавного инструмента обеспечивается высокой чистотой (отсутствие зазубрин, мелких трещин) лезвия инструмента.
Алмазный инструмент изготовляется в виде алмазосодержащих кругов с бакелитовой или металлической связкой.
Также изготавливают алмазные резцы (для обработки корпусов часов), фильеры (для волочения проволоки из высокотвердых и драгоценных металлов) и др.

 Лекция 20
Лекция 20

Коррозионно-стойкие стали и сплавы. Жаростойкие стали и сплавы. Жаропрочные стали и сплавы
1. Коррозия электрохимическая и химическая.
2. Классификация коррозионно-стойких сталей и сплавов
3. Хромистые стали.
4. Жаростойкость, жаростойкие стали и сплавы.
5. Жаропрочность, жаропрочные стали и сплавы
6. Классификация жаропрочных сталей и сплавов
Коррозия электрохимическая и химическая.
Разрушение металла под воздействием окружающей среды называют коррозией.
|
|
|
Коррозия помимо уничтожения металла отрицательно влияет на эксплуатационные характеристики деталей, содействуя всем видам разрушения.
Коррозия в зависимости от характера окружающей среды может быть химической и электрохимической.
Электрохимическая коррозия имеет место в водных растворах, а так же в обыкновенной атмосфере, где имеется влага.
Сущность этой коррозии в том, что ионы металла на поверхности детали, имея малую связь с глубинными ионами, легко отрываются от металла молекулами воды.
Металл, потеряв часть положительно заряженных частиц, ионов, заряжается отрицательно за счет избыточного количества оставшихся электронов. Одновременно слой воды, прилегающий к металлу, за счет ионов металла приобретает положительный заряд. Разность зарядов на границе металл – вода обуславливает скачок потенциала, который в процессе коррозии изменяется, увеличиваясь от растворения металла, и уменьшаясь от осаждения ионов из раствора на металле.
Если количество ионов переходящих в раствор и осаждающихся на металле одинаково, то скорости растворения и осаждения металла равны и процесс коррозии (разрушения металла) не происходит. Этому соответствует равновесный потенциал 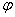 .
.
|
|
|
За нулевой потенциал принимают равновесный потенциал водородного иона в водном растворе при концентрации положительных ионов водорода, равной 1 моль ионов 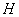 + на 1 литр.
+ на 1 литр.
Стандартные потенциалы других элементов измерены по отношению к водородному потенциалу.

Металлы, стандартный потенциал которых отрицательный – корродируют в воде, в которой растворен кислород тем активнее, чем отрицательней значение электрохимического потенциала.
Уходящие ионы металла, взаимодействуя с ионами 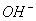 , образуют гидроксиды, нерастворимые в воде, которые называют ржавчиной, а процесс их образования – ржавлением.
, образуют гидроксиды, нерастворимые в воде, которые называют ржавчиной, а процесс их образования – ржавлением.
Схема ржавления железа:
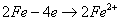 ;
;

Гидроксид железа 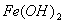 в присутствии кислорода, растворенного в воде, превращается в
в присутствии кислорода, растворенного в воде, превращается в 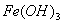 . Так как это нерастворимое соединение, то равновесный потенциал не может быть достигнут и коррозия будет продолжаться до полного разрушения.
. Так как это нерастворимое соединение, то равновесный потенциал не может быть достигнут и коррозия будет продолжаться до полного разрушения.
В зависимости от структуры коррозия имеет разное проявление: при однородном металле – коррозия происходит равномерно по всей поверхности. При неоднородном металле – коррозия избирательная и называется точечной. Это явление наиболее опасно, так как приводит к быстрой порче всего изделия. Избирательная коррозия создает очаги концентрации напряжений, что содействует разрушению.
|
|
|
Химическая коррозия может происходить за счет взаимодействия металла с газовой средой при отсутствии влаги. Продуктом коррозии являются оксиды металла. Образуется пленка на поверхности металла толщиной в 1…2 периода кристаллической решетки. Этот слой изолирует металл от кислорода и препятствует дальнейшему окислению, защищает от электрохимической коррозии в воде. При создании коррозионно-стойких сплавов – сплав должен иметь повышенное значение электрохимического потенциала и быть по возможности однофазным.
Дата добавления: 2018-11-24; просмотров: 443; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
