Оптимальные условия синтеза оксида серы ( VI )
2 SO 2 + O 2 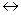 2 SO 3 ( -
2 SO 3 ( - 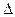 Hx . p . ):
Hx . p . ):
1) P  , to
, to  3) P
3) P 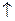 , to
, to 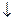
2) P 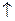 , to
, to 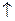 4)P
4)P 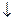 , to
, to 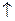
25. Математическое выражение Кр системы nA + mB 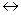 gC + pD имеет вид:
gC + pD имеет вид:
1) 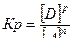 ; 3)
; 3) 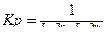 ; г г
; г г
2) 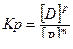 ; 4)
; 4) 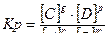 .
.
26. Равновесие химической реакции 4 HCl + O 2 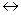 2 Cl 2 + 2 H 2 O (-
2 Cl 2 + 2 H 2 O (- 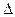 H ) смещается в сторону продуктов при г г г г
H ) смещается в сторону продуктов при г г г г
1) повышении температуры
2) повышении давления
3) наличие катализатора
4) понижении давления
27. Реакции, протекающие с выделением тепла называются …, 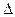 Н х.р. имеет знак ….
Н х.р. имеет знак ….
28. Химическая реакция не возможна, если ….
29. 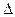 G х.р. при н.у. рассчитывают по формуле …, а при произвольных условиях: ….
G х.р. при н.у. рассчитывают по формуле …, а при произвольных условиях: ….
30. Если 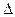 G х.р. = 0, то в системе наступает ….
G х.р. = 0, то в системе наступает ….
31. Изменение энтропии системы рассчитывают по формуле:
1) 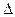 Н х.р =
Н х.р = 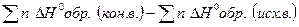 ;
;
2) 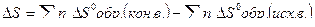 ;
;
3) 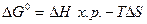 ;
;
4) 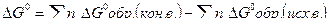 .
.
32. Если 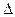 G х.р. < 0, то реакция ….
G х.р. < 0, то реакция ….
Дополните
33. Теория электролитической диссоциации:
а) В растворе сильных электролитов больше частиц - ….
б) Слабые электролиты количественно отличаются по величине …
в) рН = …
г) рН + рОН = …
д) Математическое выражение закона разбавления Оствальда …
е) [Н+] = 10-3, а [ОН-] = …
ж) [ОН-] = 10-2, рН = …
Установите соответствие
34. Класс формула
1. средняя соль а) PbOHNO3
2. двойная соль б) KH2PO4
3. кислая соль в) Fe2(SO4)3
4. комплексная соль г) KAl(SO4)2
5. кислота д) K3[Fe(CN)6]
|
|
|
6. основание е) CaOCl2
ж) H2CO3
и) Fe(OH)2
Среда раствора индикатор
1. кислая а) фенолфталеин (б/ц)
2. нейтральная б) метилоранж (оранж)
3. щелочная в) метилоранж (желт)
г) метилоранж (красн)
Диссоциация электролиты

 1. ступенчато ( ) а) FeOHCl2
1. ступенчато ( ) а) FeOHCl2
 2. в одну ступень ( ) б) Fe(OH)3
2. в одну ступень ( ) б) Fe(OH)3
 3. ступенчато ( первичная ) в) KHCO3
3. ступенчато ( первичная ) в) KHCO3
 ( вторичная ) г) ZnCl2
( вторичная ) г) ZnCl2
д) Na[Al(OH)4]
При диссоциации электролитов образуется число ионов
Электролиты число ионов
1. KAl(SO4)2 а) 3 иона
2. Fe2(SO4)3 б) 2 иона
3. CrBr3 в) 4 иона
4. AlCl3 г) 5 ионов
д) 6 ионов
Среда раствора рН
1. нейтральная а) рН = 4
2. кислая б) рН = 7
|
|
|
3. щелочная в) рН = 9
г) рН = 11
Установление правильную последовательность действий
39. При составлении ионных уравнений реакций необходимо:
1. записать схему реакции
2. определить силу электролита
3. расписать сильные электролиты на ионы
4. уравнять атомы
5. сократить одинаковые ионы
6.  записать кратное ионное уравнение
записать кратное ионное уравнение
7.  в виде молекул записать ( (осадки); (газы); слаб.эл-ты)
в виде молекул записать ( (осадки); (газы); слаб.эл-ты)
Выберите правильный вариант
 40. Краткое ионное уравнение имеет вид: 2 H + + CO 2- 3 CO 2 + H 2 O при взаимодействии:
40. Краткое ионное уравнение имеет вид: 2 H + + CO 2- 3 CO 2 + H 2 O при взаимодействии:
1.  (NH4)2CO3 + HBr
(NH4)2CO3 + HBr
2.  Li2CO3 + H2SiO3
Li2CO3 + H2SiO3
3.  CaCO3 + H2SO4
CaCO3 + H2SO4
4.  BaCO3 + HCl
BaCO3 + HCl
 41. Уравнению реакции Cu ( OH )2 + H 2 SO 4 CuSO 4 + 2 H 2 O
41. Уравнению реакции Cu ( OH )2 + H 2 SO 4 CuSO 4 + 2 H 2 O
Соответствует сокращенное ионное уравнение
 1. 2H+ + 2OH- 2H2O
1. 2H+ + 2OH- 2H2O
 2. Cu(OH)2 + 2H+ Cu2+ + 2H2O
2. Cu(OH)2 + 2H+ Cu2+ + 2H2O
 3. Cu2+ + SO42- CuSO4
3. Cu2+ + SO42- CuSO4
 4. Cu2+ + H2SO4 CuSO4 + 2H+
4. Cu2+ + H2SO4 CuSO4 + 2H+
С уменьшением концентрации соли степень диссоциации
1) возрастает 3) не изменится
2) уменьшается
Дополните:
43. В результате гидролиза соли образуется электролит ….
44. Гидролиз соли протекает по катиону, если соль образована основанием …, кислотой … и рН = ….
45. Гидролизу не подвергаются соли, образованные ….
Выберите правильный ответ:
46. Полному гидролизу подвергается:
1) AlCl3 3)KCl
|
|
|
2) ZnCl2 4) Al2S3
47. Гидролизу не подвергается:
1) Na2CO3 3) Na3PO4
2) NaBr 4) Na2SiO3
Дополните:
48. Степень окисления – это …
49. Окисление – процесс …
50. Если алгебраическая величина (С.О.) уменьшается, то протекает процесс…
51. Восстановитель в ходе окислительно-восстановительной реакции …
52. Сложное вещество, содержащее элемент в высшей степени окисления играет роль …
53. Ме – простые вещества являются …
54. Чем меньше величина 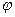 о, тем сильнее выражены свойства …
о, тем сильнее выражены свойства …
55. ЭДС рассчитывают по формуле …; ЭДС > 0, то …
Установите соответствие:
Дата добавления: 2018-11-24; просмотров: 390; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
