Основними називають оксиди, гідрати яких є основами
Хімічні властивості основних оксидів
1 Взаємодія з водою з утворенням розчинних у воді основ (лугів) (лише для активних металів):
К2O + H2O = 2КOH.
2 Взаємодія з кислотами з утворенням солей та води:
ВaO + 2HNO3 = Ba(NO3)2 + H2O.
3 Взаємодія з амфотерними оксидами з утворенням солей:
MgO + ZnO = MgZnO2,
Na2O + Cr2O3 = 2NaCrO2.
У наведених реакціях амфотерні оксиди ZnO та Cr2O3 проявляють кислотні властивості.
Кислотними називають оксиди, гідратами яких є кислоти.
Хімічні властивості кислотних оксидів
1 Взаємодія з водою з утворенням розчинних у воді кислот:
SO2 + H2O = H2SO3
2 Взаємодія з основами з утворенням солі та води:
N2O5 + 2NaOH = 2NaNO3 + H2O
3 Взаємодія з основними та амфотерними оксидами з утворенням солі:
CO2 + CaO = CaCO3
SrO + Al2O3 = Sr(AlO2)2
Амфотерними називають оксиди, які залежно від умов проявляють властивості кислотних та основних оксидів.
Хімічні властивості амфотерних оксидів
1 Не реагують з водою через нерозчинність відповідних гідроксидів.
2 Взаємодія з кислотами з утворенням солей:
ZnO + H2SO4 = ZnSO4 + H2O.
3 Взаємодія з основами з утворенням солі та води:
BeO + 2NaOH = Na2BeO2 + H2O.
4 Взаємодія з основними оксидами з утворенням солі:
PbO + MgO + = MgPbO2.
До гідратів оксидів відносять основи та кислоти.
Основами називаються складні сполуки, які складаються з атомів металу та гідроксогруп. Кількість гідроксогруп вказує на кислотність основи та визначається ступенем окиснення металу.
|
|
|
З точки зору теорії електролітичної дисоціації основами називають електроліти, при дисоціації яких утворюються у вигляді аніонів лише гідроксид-йони.
Основи класифікують:
- за розчинністю на розчинні, або луги та нерозчинні;
- за кількістю гідроксогруп на однокислотні, двокислотні та багатокислотні.
Кислотами називають складні речовини, до складу яких входять атоми Гідрогену, здатні заміщуватися на атоми металу. З точки зору теорії електролітичної дисоціації кислотами називають електроліти, при дисоціації яких у вигляді катіонів утворюються лише H+-катіони.
Кислоти класифікують:
- за основністю (аналогічно основам).
- за здатністю до дисоціації на сильні (добрі електроліти) та слабкі (погані електроліти).
- за окиснювальною здатністю на кислоти окисники (окиснюють елементом-кислотоутворювачем) та кислоти-неокисники (окиснюють катіонами Гідрогену).
- за наявністю Оксигену в молекулі поділяються на безоксигенові та оксигеновмісні.
Хімічні властивості гідратів оксидів
а) хімічні властивості основ:
1 Взаємодія з кислотами та амфотерними гідроксидами:
3LiOH + H3PO4 = Li3PO4 + 3H2O,
2NaOH + Zn(OH)2 = Na2ZnO2 + 2H2O.
|
|
|
2 Взаємодія з кислотними оксидами:
Sr(OH)2 + SO3 = SrSO4 + H2O.
3 Взаємодія з амфотерними оксидами:
2RbOH + BeO = Rb2BeO2 + H2O.
4 Розклад при нагріванні (крім KOH, NaOH, RbOH, CsOH):
Zn(OH)2 = ZnO + H2O.
б) хімічні властивості кислот:
1 Взаємодія з основами та амфотерними гідроксидами:
HBO2 + NaOH = NaBO2 + H2O
3H2SO4 + Cr(OH)3 = Cr2(SO4)3 + 3H2O
2 Взаємодія з основними та амфотерними оксидами:
2HClO2 + CaO = Ca(ClO2)2 + H2O
6HNO3 + Fe2O3 = 2Fe(NO3)3 + 3H2O
Зразок картки контролю знань
1 Назвіть оксиди та їх гідрати: Bi2О3, Tl2О, НСlO4, Al(OH)3.
2 Напишіть хімічні формули таких сполук: сульфатна кислота, ферум (II) гідроксид, берилій оксид, молібден (VI) оксид.
3 Закінчіть рівняння тих реакцій, які проходять:
Р2O5 + RbOH → CaO + Cl2O7 →
Ва(ОН)2 + CO2 → HMnO4 + NaOH →
Завдання для самостійної роботи
Завдання І
Назвіть сполуки і визначіть ступені окиснення елементів:
| В | Формули оксидів | В | Формули оксидів |
| 1 | CaO; WO3; Cl2О | 9 | CdO; Sb2O3; TeO3 |
| 2 | Na2O; Ga2O3; SeO3 | 10 | NiO; Hg2O; Fe2O3 |
| 3 | BaO; CO2; Bi2O5 | 11 | ZnO; In2O3; SO2 |
| 4 | MgO; In2O3; As2O5 | 12 | BeO; SnO; SO3 |
| 5 | Cr2O3; SnO2; CO | 13 | Al2O3; VO2; CrO3 |
| 6 | K2O; GeO; P2O5 | 14 | CoO; SnO2; TeO3 |
| 7 | Ag2O; PbO2; Cl2O7 | 15 | PbО; FeO; SiO2 |
| 8 | SrO; TiO2; V2O5 |
| |
Завдання ІІ
Напишіть хімічні формули таких сполук:
|
|
|
| В | Назви оксидів | В | Назви оксидів |
| 1 | натрій оксид ферум(ІІ) оксид хлор(І) оксид | 9 | алюміній оксид сульфур(ІV) оксид манган(VII) оксид |
| 2 | магній оксид титан(ІV) оксид фосфор(ІІІ) оксид | 10 | калій оксид силіцій(ІV) оксид ферум(ІІІ) оксид |
| 3 | цинк оксид хром(VІ) оксид карбон(ІІ) оксид | 11 | купрум(І) оксид стибій(ІІІ) оксид манган(ІV) оксид |
| 4 | рубідій оксид ванадій(V) оксид хлор(VІІ) оксид | 12 | стронцій оксид осмій(VІІІ) оксид арсен(ІІІ) оксид |
| 5 | літій оксид плюмбум(ІІ) оксид фосфор(V) оксид | 13 | берилій оксид телур(VІ) оксид індій(ІІІ) оксид |
| 6 | барій оксид нітроген(І) оксид селен(VІ) оксид | 14 | бор оксид карбон(ІV) оксид хром(VІ) оксид |
| 7 | кадмій оксид германій(ІІ) оксид сульфур(ІV) оксид | 15 | купрум(ІІ) оксид нітроген(ІІІ) оксид талій(І) оксид |
| 8 | радій оксид ванадій(ІV) оксид бісмут(V) оксид |
| |
Завдання ІII
Назвіть сполуки.
| В | Формули сполук | В | Формули сполук | В | Формули сполук |
| 1 | Ca(OH)2 H2S HClO4 | 6 | KOH HF H2CrO4 | 11 | Cu(OH)2 H2B4O7 H2SO4 |
| 2 | Zn(OH)2 H2Se HClO2 | 7 | Mn(OH)2 H2CO3 H2ZnO2 | 12 | NaOH HNO3 H4SiO4 |
| 3 | Al(OH)3 HІ H2SO3 | 8 | Fe(OH)3 HNO2 HVO3 | 13 | Mn(OH)3 H2PbO2 HPO3 |
| 4 | Ba(OH)2 H2Te HAlO2 | 9 | Ni(OH)2 HAsO3 H2SeO4 | 14 | Co(OH)2 H2SnO3 HBO2 |
| 5 | Fe(OH)2 HBr H3PO4 | 10 | TlOH H2TeO3 HMnO4 | 15 | Sr(OH)2 H3BO3 HAlO2 |
Завдання IV
|
|
|
Напишіть хімічні формули таких сполук:
| В | Назви сполук | В | Назви сполук |
| 1 | кальцій гідроксид хлоридна кислота хроматна кислота | 9 | алюміній гідроксид метафосфатна кислота цинкатна кислота |
| 2 | ферум(ІІ) гідроксид бромідна кислота нітритна кислота | 10 | цинк гідроксид ортосилікатна кислота перхлоратна кислота |
| 3 | талій(І) гідроксид сульфатна кислота метаборатна кислота | 11 | манган(ІІІ) гідроксид телуритна кислота метафосфатна кислота |
| 4 | ферум(ІІІ) гідроксид сульфітна кислота перманганатна к-та | 12 | кобальт(ІІ) гідроксид гіпохлоритна кислота метастанатна кислота |
| 5 | лантан(ІІІ) гідроксид телуридна кислота ортофосфатна к-та | 13 | германій(ІІ) гідроксид ванадатна кислота ортосилікатна кислота |
| 6 | калій гідроксид хлоратна кислота селенідна кислота | 14 | бісмут(ІІІ) гідроксид метаарсенітна кислота хлоритна кислота |
| 7 | купрум(ІІ) гідроксид бромідна кислота карбонатна кислота | 15 | арсен(ІІІ) гідроксид метастанітна кислота ортогерманітна к-та |
| 8 | стронцій гідроксид телуратна кислота нітратна кислота |
| |
Завдання V
Закінчіть рівняння тих реакцій, які проходять:
| В | Рівняння реакції | В | Рівняння реакції |
| 1 | BeO + CO2 → V2O5 + ZnO → Mn2O3 + SO3 → CrO3+Fe(OH)2→ CaO+Sn(OH)2→ Pb(OH)2+KOH→ | 9 | B2O3 + CoO→ P2O5 + Cr2O3→ MnO + ZnO → Mn2O7+NaOH→ HІ+TlOH→ Fe(OH)3+Co(OH)2→ |
| 2 | Cl2O7 + NaOH → SnO2 + CoO → SiO2+NiO→ Cr(OH)3+MgO→ Fe(OH)2+HCl→ ZnO+NaOH→ | 10 | Mn2O7 + K2O→ V2O5 + BaO→ MgO + SiO2→ HNO3+PbO→ TiO2+CaO→ SeO2+Ba(OH)2→ |
| 3 | P2O5 + MnO→ ZnO + Tl2O→ BaO + BeO → CaO+Be(OH)2→ Mg(OH)2+Ga2O3→ H2SiO3+VO→ | 11 | VO2 + MgO→ BeO + NiO → CaO + SiO2 → SeO2+Fe(OH)3→ Zn(OH)2+Mg(OH)2→ H2CrO4+BaO→ |
| 4 | Fe2O3 + NiO→ Na2O + SeO2→ Ag2O + N2O5→ Mn(OH)3+H2SO4→ SO2+Ba(OH)2→ MgO+Al(OH)3→ | 12 | Fe2O3 + SiO2→ P2O5 + ZnO→ SnO + MgO→ PbO+H3PO4→ HBO2+CdO→ NaOH+CO2→ |
| 5 | TeO3 + K2O → Al2O3 + BaO→ Cl2O + CoO→ NaOH+N2O5→ Cr(OH)3+SrO→ Tl2O+Zn(OH)2→ | 13 | CrO + SO3 → V2O5 + K2O → MgO + N2O3→ NaOH+CuO→ Ca(OH)2 + Mn2O7→ Ba(OH)2+Cl2O7→ |
| 6 | Be(OH)2 + Ni(OH)2→ TeO2 + SrO→ MgO + SiO2→ HVO3+MgO→ Cr2O3+HNO3→ B2O3+MgO→ | 14 | As2O5 + MgO→ Mn2O3 + SiO2→ Cl2O7 + CaO→ Al(OH)3+N2O5→ H2TeO4+Mg(OH)2→ Ca(OH)2+HClO→ |
| 7 | SO3 + CoO→ MgO + SeO2→ Na2O + N2O5→ Sn(OH)2+HClO2→ PbO+KOH→ V2O5+Ni(OH)2→ | 15 | SeO3+ K2O → CO2 + BaO→ SnO + FeO→ Ba(OH)2+B2O3→ ZnO+H3PO4→ BeO+Ni(OH)2→ |
| 8 | NiO + ZnO → PbO + Mn2O3 → SiO2+CaO→ | Mg(OH)2+SiO2→ CaO+CO2→ Al2O3+KOH→ | |
Тест самоконтролю №1
1 Які з ряду металів утворюють тільки основні оксиди:
а) Na, Al, Zn, Ag; б) K, Pb, Fe, Hg; в) Na, Ca, Mg, Ba;
г) Ba, Mn, Zn, Al; д) Ca, Ag, Pb, Sn.
2 Який ряд елементів утворює тільки кислотні оксиди:
а) S, Ba, Si, N; б) P, Ca, Cl, Ni;
в) S, P, Cl, C; г) Cl, Mg, Si, Zn; д) Br, I, Ag, Cu.
3 Який ряд елементів утворює тільки амфотерні оксиди:
а) Zn, Pb, Sn, Al; б) Zn, S, K, Ni;
в) Pb, N, Ag,Co; г) Fe, Sn, Cl, C; д) Ba, Ni, Al, Si.
4 Вкажіть формулу вищого оксиду для елемента з порядковим номером 7:
а) R2O3; б) R2O; в) RO;
г) R2O5; д) R2O7.
5 Вкажіть оксид, в якому валентність елемента найнижча:
а) N2O5; б) FeO; в) Li2O;
г) CO2; д) Cl2O3.
6 Вкажіть оксиди, які реагують з хлоридною кислотою:
а) BaO i SiO2; б) CaO i FeO; в) NiO i CO;
г) CoO i N2O5; д) B2O3 i SO2.
7 З натрій гідроксидом взаємодіють:
а) MgO i SO2; б) N2O5 i CoO; в) Al2O3 i Li2O;
г) Cl2O3 i BaO; д) Cl2O7 i ZnO.
8 Вкажіть оксиди, які взаємодіють з перхлоратною кислотою:
а) CaO i SiO2; б) BaO i ZnO; в) CoO i N2O3;
г) FeO i SO3; д) MnO i CO2.
9 Визначте речовини А, Б, В в схемі перетворень:
AlCl3  Al2O3
Al2O3 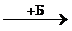 Al(NO3)3
Al(NO3)3
↓+B
NaAlO2
а) А: HCl, Б: HNO3, В: Na2O;
б) А: Cl2, Б: HNO2, В: NaCl;
в) А: HCl, Б: NO, В: Al(OH)3;
г) А: HClO, Б: N2O5, В: N2O;
д) правильної відповіді немає.
10 Визначте речовини А, Б, В в схемі перетворень:
Fe(ClO4)2  Fe2O3
Fe2O3  Fe2(SO4)3
Fe2(SO4)3
↓+B
Mg(FeO2)2
а) А: HCl, Б: SO3, В: MgO;
б) А: HClO4, Б: SO3, В: MgO;
в) А: HClO2, Б: SO2, В: MgO;
г) А: HClO4, Б: SO2, В: Mg(OH)2;
д) правильної відповіді немає.
Відповіді
1 в, 2 в, 3 а, 4 г, 5 в, 6 б, 7 г, 8 б, 9 а 10 б.
Тест самоконтролю №2
1 Вкажіть кислоту, яка належить до одноосновних:
а) нітатна; б) сульфатна; в) сульфітна;
г) телуритна; д) ортофосфатна.
2 Вкажіть кислоту, яка належить до безоксигенових:
а) ортофосфатна; б) сульфатна; в) бромідна;
г) нітритна; д) хлоратна.
3 Вкажіть назви кислот, формули яких H2B4O7, HClO3, HI:
а) метаборатна, хлоратна, йодатна;
б) тетраборатна, хлоратна, йодидна;
в) ортоборатна, хлоратна, йодидна;
г) тетраборатна, хлоратна, йодитна;
д) правильної відповіді немає.
4 Вкажіть назви кислот, формули яких HCl, H2S, H3AsO4:
а) хлоридна, сульфатна, ортоарсенатна;
б) хлоритна, сульфідна, ортоарсенатна;
в) хлоридна, сульфідна, ортоарсенатна;
г) хлоритна, сульфідна, метаарсенатна;
д) правильної відповіді немає.
5 Вкажіть назви кислот, формули яких H2Te, H3PO4, HNO2:
а) телуридна, ортофосфатна, нітритна;
б) телуритна, ортофосфатна, нітритна;
в) телуратна, метафосфатна, нітритна;
г) телуратна, ортофосфатна, нітратна;
д) правильної відповіді немає.
6 З якими речовинами взаємодіє H2TeO3:
а) Ca i SiO2; б) BaO i Mg(OH)2; в) NiO i SO2;
г) S i CO; д) ZnO i CO2.
7 З якими речовинами взаємодіє H3PO4:
а) Cu i N2O3; б) FeO i P2O3; в) MgO i Fe2O3;
г) Al i Cl2O; д) CuO i Cl2O3.
8 З якими речовинами взаємодіє HClO2:
а) Al2O3 i ZnO; б) SnO i N2O3; в) CdO i HCN;
г) Ba i V2O5; д) SiO2 i SrO.
9 Визначте речовини А, Б, В в схемі перетворень:
H2S  H2SO4(к)
H2SO4(к)  BaSO4
BaSO4
↓+B
SO2
а) А: Cu, Б: BaCl2, В: Cu;
б) А: Ca, Б: BaCl2, В: Cu;
в) А: Fe, Б: SO3, В: Ni;
г) А: Cu, Б: SO2, В: Na;
д) правильної відповіді немає.
10 Визначте речовини А, Б, В в схемі перетворень та кількість молей необхідних для одержання продуктів:
NaH2PO4  H3PO4
H3PO4  Na2HPO4
Na2HPO4
↓+B
Na3PO4
а) А: 1 моль NaOH, Б: 2 моль NaOH, В: 3 моль NaOH;
б) А: 2 моль NaOH, Б: 2 моль Na, В: 3 моль NaOH;
в) А: 2 моль Na2O, Б: 2 моль Na2O, В: 3 моль Na2O;
г) А: 3 моль NaOH, Б: 2 моль NaOH, В: 1 моль NaOH;
д) правильної відповіді немає.
Відповіді
1 а, 2 в, 3 б, 4 в, 5 а, 6 б, 7 в, 8 в, 9 б, 10 а.
Хід роботи
Кислотні оксиди
1.1 Одержання та властивості сульфур (IV) оксиду
Нагрійте в залізній ложечці грудочку сірки, поки вона не займеться (зверніть увагу на колір полум’я). опустіть ложечку з сіркою, яка горить, в колбу з водою та прикрийте її скляною пластинкою. Потримайте ложечку з палаючою сіркою над водою15-20 с, після чого вміст колби збовтайте і перевірте реакцію розчину синім лакмусовим папірцем. Який газ утворюється при горінні сірки? Що утворюється при взаємодії цього газу з водою? Зробіть висновки про хімічні властивості цього газу та напишіть відповідні рівняння реакцій.
Основні оксиди
2.1 Властивості магній оксиду
В дві пробірки покладіть по крупинці магній оксиду. В одну з них прилийте 1,5-2 мл розведеної хлоридної кислоти, а в другу – таку ж кількість концентрованого розчину натрій гідроксиду. Вміст пробірки, в якій реакція при кімнатній температурі не відбувається, нагрійте. Зробіть висновок про хімічні властивості цього оксиду та напишіть відповідні рівняння реакцій.
Амфотерні оксиди
3.1 Властивості цинк оксиду
В дві пробірки покладіть по крупинці цинк оксиду. В одну з них прилийте 1,5-2 мл розведеної хлоридної кислоти, а в другу – таку ж кількість концентрованого розчину натрій гідроксиду. Вміст пробірки, в якій реакція при кімнатній температурі не відбувається, нагрійте. Зробіть висновок про хімічні властивості цього оксиду та напишіть відповідні рівняння реакцій.
Дата добавления: 2018-04-05; просмотров: 3135; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
