Примеры решения типовых задач
Пример № 1. Определите строение сложного эфира аминокислоты, если известно, что он содержит 15,73 % азота по массе.
Решение:
Сложные эфиры a- аминокислот описываются общей формулой:
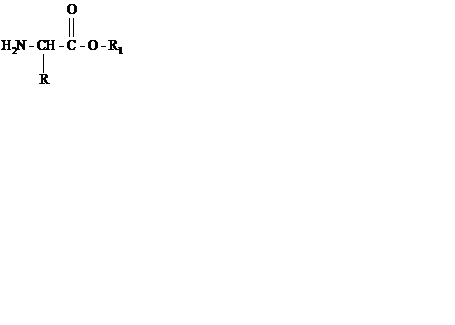
где: R – водород или углеводородный радикал;
R1 – углеводородный радикал.
В одном моле этого вещества содержится один моль азота (М = 14 г), что составляет 15,73 % от общей (молярной) массы, следовательно, молярная масса эфира равна: М(H2N – CH(R) – COOR1) = 14/0,1573 = 89 г/моль. На долю двух радикалов приходится M(R + R1) = 89 – M(H2N + CH + COO) = 16 г/моль.
Это возможно лишь в случае, если R = H; R1 = CH3. Таким образом, искомый эфир аминоуксусной кислоты: H2N – CH2 – COO – CH3.
Пример № 2. Напишите уравнения реакций образования трипептидов:
а) из аминоуксусной кислоты;
б) из аминоуксусной кислоты, аланина и цистеина.
Решение:Пептиды образуются при конденсации молекул аминокислот, при этом взаимодействует группа -NH2 одной молекулы и группа –СООНдругой.
1. При конденсации трёх молекул аминоуксусной кислоты протекает следующая реакция:
H2N – CH2 – COOH + H2N – CH2 – COOH + H2N – CH2 – COOH ®
® H2N – CH2 – CO – NH – CH2 – CO – NH – CH2 – COOH + 3H2O
2. Конденсация трёх аминокислот может произойти в различной последовательности, например в такой:

Пример № 3. С помощью каких реакций можно осуществить следующие превращения: сахароза → глюкоза → глюконовая кислота?
Решение:
Сахароза гидролизуется при нагревании в подкисленном растворе:

|
|
|
Глюкоза окисляется свежеосаждённым гидроксидом меди (II) с образованием глюконовой кислоты (С6Н12О7):

Пример № 4. Полученное из глюкозы соединение С3Н6О3 в реакции с натрием образует соединение состава C3H4Na2O3, с карбонатом кальция −С6Н10СаО6, с этанолом в присутствии серной кислоты − С5Н10О3. Назовите это соединение и напишите уравнения реакций.
Решение: При молочнокислом брожении из глюкозы получается молочная(2-гидроксипропановая) кислота: С6Н12О6 → 2СН3-СН(ОН)-СООН.
В реакции молочной кислоты с натрием участвуют и гидроксильная и карбоксильная группы:
СН3-СН(ОН)-СООН + 2Na → CH3-CH(ONa)-COONa + H2
С карбонатом кальция и с этанолом молочная кислота реагирует как обычная карбоновая кислота:

Пример № 5. Массовая доля крахмала в картофеле составляет 20 %. Рассчитайте массу глюкозы, которая может быть получена из картофеля массой 405 кг. Выход продукта равен 70 %.
Решение: Составляем уравнение реакции гидролиза крахмала, в результате которой образуется глюкоза:
(С6Н10О5) + хН2О → хС6Н12О6
Рассчитаем массу крахмала в картофеле:
m(крахмала) = ω(крахмала)∙ m(картофеля)/100 = 20 ∙ 405/100 = 81 кг
Определяем количество вещества крахмала:
n(крахмала)=m(крахмала)/M(крахмала)= 81/162x = 1/2x кмоль
Из уравнения реакции гидролиза крахмала следует
n(крахмала)/ n(глюкозы) = 1/x,
откуда получаем
n(глюкозы) = x∙n (крахмала); n(глюкозы) = x/2x = 0,5 кмоль
Вычисляем массу глюкозы, которую можно получить при количественном выходе:
m(глюкозы) = n(глюкозы)М(глюкозы); m(глюкозы) = 0,5∙180 кг = 90 кг.
Учитывая массовую долю выхода продукта, рассчитаем массу реально полученной глюкозы:
mр(глюкозы) = 90∙ 70/100 = 63 кг
|
|
|
Дата добавления: 2018-04-05; просмотров: 500; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
