Качественные (цветные) реакции на функциональные группы белков и аминокислот
| Название реакции и выявляемая группа | Исследуемый материал | Употребляемые реактивы | Наблюдаемое окрашивание | Принцип реакции |
| 1. Биуретовая реакция на наличие пептидных связей | а) яичный белок, р-р, 5 капель б) глицилглицин, 1% р-р, 5 капель в) глицин | а) биуретовый реактив, 2 капли б) -----//-------//-------- в) -----//-------//-------- | ||
| 2. Нингидриновая реакция на a - амино-кислоты | а) яичный белок, р-р, 5 капель б) β-аланин, 1% р-р, 5 капель в) a-аланин, 1% р-р, 5 капель | а) 0,5% р-р нингидрина нагреть до кипения б) -----//-------//-------- в) -----//-------//-------- | ||
| 3. Ксантопротеиновая реакция на ароматическое кольцо в аминокислоте | а) яичный белок, р-р, 5 капель б) тирозин, 1% р-р, 5 капель в) глицин, 1% р-р, 5 капель | а) конц. НNО3, 3 капли нагреть до кипения б) -----//-------//-------- в) -----//-------//-------- добавление NаОН до оранжевого окрашивания | ||
| 4. Реакция Миллона на тирозин | а)яичный белок, р-р, 5 капель б) тирозин, 0,1% р-р, 5 капель в) фенилаланин | а) реактив Миллона, 5 капель б) --//-- нагреть до 50º в) -----//-------//-------- | ||
| 5. Реакция Фоля на аминокислоты, содержащие слабосвязанную серу | а) яичный белок, р-р, 5 капель б) цистеин, 1% р-р, 5 капель в) глицин, 1% р-р, 5 капель | а) 5% р-р ацетата свинца, 10 капель, 20% р-р NаОН по каплям до растворения осадка и нагреть до кипения б) -----//-------//-------- в) -----//-------//-------- | ||
| 6. Нитропруссидная реакция на серусо-держащие аминокислоты | а) неразб. яичный белок, 5 капель б) метионин, 0,1% р-р, 5 капель в) глицин, 1% р-р, 5 капель | а) 20% р-р NаОН, 10 капель кипятить 3 минуты, охладить! 5% р-р нитропруссида натрия, 3 капли б) -----//-------//-------- в) -----//-------//-------- |
Вывод:______________________________________________________________
|
|
|
Подпись преподавателя __________________
«___»_________20____ г.
Занятие №3 Тема: Физико-химические свойства и строение белков. Диализ белков. Исследования денатурации белков. Хроматография аминокислот.
Цель:изучитьуровни структурной организации белков и связи их стабилизирующие. Выучить классификацию простых белков и характеристику отдельных их групп; физико-химические свойства белков, явление денатурации и факторы денатурации. Научиться рассчитывать Rf для каждой аминокислоты; выполнять биуретовую реакцию на пептидную группу; проводить реакцию, подтверждающую наличие низкомолекулярных соединений, проводить химические реакции, используемые для денатурации белка.
Вопросы для обсуждения.
1.Структурная организация белковых молекул.
2.Химические связи, стабилизирующие первичную, вторичную, третичную и четвертичную структуру белка.
|
|
|
3.Классификация простых белков с характеристикой их отдельных групп.
4.Физико-химические свойства белков.
5. Денатурация белков.
Выполняемая работа.
Работа №1.Хроматографический метод разделения аминокислот.
1. Зарисовать полученную хроматограмму после обработки раствором нингидринa:
2. Рассчитать значение Rf для каждой аминокислоты по формуле:
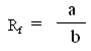 ,
,
где а - расстояние от места нанесения раствора смеси аминокислот (линия старта) до центра пятна конкретной аминокислоты; b — путь, пройденный растворителем от линии старта до его фронта после окончания хроматографии, мм.
Rf1=
Rf2=
Rf3=
Вывод:______________________________________________________________
Работа №2. Диализ белков.
Таблица 1
Принцип метода: ____________________________________________________
| Определяемые компоненты | До диализа | После диализа | ||
| Внешняя жидкость | Внутренняя жидкость | Внешняя жидкость (диализат) | Внутренняя жидкость | |
| Белок (с биуретовым реактивом, 3-5 капель) | ||||
| SО42- (с 2-3 каплями ВаСl2) | ||||
Вывод:______________________________________________________________
Работа №3 Исследование денатурации белков
Таблица 2
Принцип метода: ____________________________________________________
| Исследуемый материал | Денатурирующий фактор | Наблюдаемые изменения | Механизм денатурации белка | ||
| 1.Раствор яичного белка, 5 кап. | Конц. HNO3, 10 капель |
| |||
| 2.Раствор яичного белка, 10 капель | Трихлоруксусная кислота, 10% раствор, 2 капли | ||||
| 3.Раствор яичного белка, 10 капель | Сульфат меди, 5% раствор, 2 кап. | ||||
| 4.Раствор яичного белка, 10 капель | 100°С (кипячение) |
Вывод:______________________________________________________________
Подпись преподавателя __________________
«___»_________20____ г.
Занятие № 4 - Тема: Сложные белки и их кофакторы. Фосфопротеины. Углеводсодержащие белки. Хромопротеины. Выделение казеиногена из молока и определение фосфата в казеиногене. Определение углеводного компонента гликопротеинов. Иммуноглобулины. Химическая природа гемпротеинов.
Цель:изучитьклассификацию сложных белков;строение и свойства хромопротеинов; фосфопротеинов и углеводсодержащих белков. Научиться выполнять биуретовую реакцию на пептидную группу;ставить бензидиновую пробу на геминовую группу гемоглобина;реакцию Миллона на углеводный компонент гликопротеина яичного белка;молибденовую пробу для определения фосфорной группы казеиногена после гидролиза.
|
|
|
Вопросы для обсуждения.
1. Привести классификацию сложных белков.
2. Охарактеризуйте строение хромопротеинов, укажите простетические группы хромопротеинов.
3. Охарактеризуйте строение и функции производных бета-каротина, изоаллоксазина, порфирина, напишите их структурные формулы.
4. Фосфопротеины, особенности их строения и роль в организме.
5. Строение протеогликанов (мукопротеинов), их функции в организме, представители протеогликанов.
6. Гликопротеины, особенности строения, функции в организме, представители гликопротеинов.
7. Иммуноглобулины (антитела), особенности строения, образования и функции в организме.
Выполняемая работа
Работа №1 Химическая природа небелковых компонентов белков-протеидов
Таблица № 1
| Название сложного белка | Название определяемого компонента | Используемые материалы, реактивы и приемы | Наблюдаемые изменения | Принцип реакции |
| 1 | 2 | 3 | 4 | 5 |
| Гемпротеины | Определение гемина | 1 мл разведенной в 5000 раз крови, кипячение, охлаждение + 5 капель раствора бензидина + 5 капель раствора пероксида водорода | ||
| Определение белка | 5 капель разведенной в 5000 раз крови + 3 капли биуретового реактива | |||
| Фосфопротеины | Выделение казеиногена из молока | 1) 4мл разведенного молока; 2) 1 каплю конц. уксусной кислоты; 3) фильтрование, промывка дважды дистиллированной водой; 4) 3 капли биуретового реактива + часть осадка (казеиногена) | ||
| Гидролиз казеиногена | 1) остаток казеиногена 2) 4мл 10% р-ра NaOH 3) кипячение 10-15 мин. | |||
| Определение белка | 1) 5 капель гидролизата 2) 3 капли биуретового реактива | |||
| Определение фосфата | 1) 5 капель фильтрата 2) 20 капель молибденового реактива 3) кипячение | |||
| Гликопротеины | Определение углеводов (гексозы) | 10 кап. раствора яичного белка + 3 к. раствора альфа-нафола 1% + 20 кап. серной кислоты (к.) | ||
| Определение белка в растворе яичного белка | 1) 5 капель раствора яичного белка 2) 3 капли биуретового реактива |
Вывод: _______________________
Подпись преподавателя __________________
«___»_________20____ г.
Дата добавления: 2018-02-15; просмотров: 2132; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
