Опыт 2 Взаимодействие серной кислоты с металлами.
Лабораторная работа №2
Тема: Приготовление суспензии карбоната кальция в воде. Получение эмульсии моторного масла. Ознакомление со свойствами дисперсных систем.
Цели работы : изучить способы приготовления эмульсий и суспензий ; научиться отличать коллоидный раствор от истинного; отработать навыки экспериментальной работы, соблюдая правила техники безопасности при работе в кабинете химии.
Приборы и реактивы ;ступка с пестиком, ложка-шпатель, стакан, стеклянная палочка, фонарик, пробирка;вода, карбонат кальция (кусочек мела), масло, ПАВ, мука, раствор крахмала, раствор сахара .
Ход работы:
1 Инструктаж по ТБ
Меры безопасности:
Осторожно использовать стеклянную посуду.
Правила первой помощи:
При ранении стеклом удалите осколки из раны, смажьте края раны раствором йода и перевяжите бинтом. При необходимости обратиться к врачу.
Опыт № 1. Приготовление суспензии карбоната кальция в воде
В стеклянную пробирку влить 4-5мл воды и всыпать 1-2 ложечки карбоната кальция. Пробирку закрыть резиновой пробкой и встряхнуть пробирку несколько раз.
Наблюдали:
Внешний вид и видимость частиц:
.....................................................................................................................................................
Способность осаждаться и способность к коагуляции .........................................................................................................................................................................
Полученная смесь похожа ………………………………………………………………………………
Опыт № 2. Получение эмульсии моторного масла
В стеклянную пробирку влить 4-5мл воды и 1-2 мл масла, закрыть резиновой пробкой и встряхнуть пробирку несколько раз.
Наблюдали:
Внешний вид и видимость частиц:
.....................................................................................................................................................
Способность осаждаться и способность к коагуляции .........................................................................................................................................................................
Добавьте каплю ПАВ (эмульгатора) и перемешайте ещё раз.
Наблюдали:
Внешний вид и видимость частиц:
.....................................................................................................................................................
Способность осаждаться и способность к коагуляции .........................................................................................................................................................................
Вывод: …………………………………………………………………………………………………………………
Опыт № 3. Приготовление коллоидного раствора и изучение его свойств
В стеклянный стакан с горячей водой внести 1-2 ложечки муки(или желатина), тщательно перемешать Наблюдали:
Внешний вид и видимость частиц:
.....................................................................................................................................................
Способность осаждаться и способность к коагуляции .........................................................................................................................................................................
Пропустить через раствор луч света фонарика на фоне темной бумаги. Наблюдается ли эффект Тиндаля?
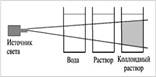
Вывод:
Лабораторная работа №3
Тема: «Приготовление раствора заданной концентрации.»
Цель: Познакомиться с понятиями раствор, концентрация, растворитель, растворенные вещества. Усовершенствование умений рассчитывать массовую долю, процентную , молярную концентрации , а также готовить растворы на основании данных расчетов.
Оборудование: Химические стаканы (или конусообразные колбы), стеклянные шпатели, мерные цилиндры, технохимические весы с разновесами, дистиллированная вода, кристаллические соли
Ход работы
1 Инструктаж по ТБ
Меры безопасности:
Осторожно использовать стеклянную посуду.
Правила первой помощи:
При ранении стеклом удалите осколки из раны, смажьте края раны раствором йода и перевяжите бинтом. При необходимости обратиться к врачу.
Задание.
Приготовить три раствора заданной концентрации
1 Приготовление раствора соли с определенной массовой долей растворенного вещества,путем растворения соли в воде.
1 Определите массу соли и воды , необходимых для приготовления раствора. Спомощью весов отмерьте рассчитанную массу твердого вещества и поместите в стакан. Зная, что плотность воды равна 1 г\мл , отмерьте объем воды мерным цилиндром и перелейте его к навеске. Перемешайте содержимое стеклянной палочкой.
2 Опишите ход выполненияопыта и наблюдения
________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
____________________________________________________________________________________________
2 Приготовление раствора №2
Рассчитайте массу воды, которую необходимо добавить к раствору№1 , чтобы получить раствор №2 меньшей концентрации. Переведите вычисленную массу воды в объём, отмерьте его и добавьте в раствор №1. Сколько грамм раствора №2 Получилось?
2 Опишите ход выполнения опыта и наблюдения
___________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
_______________________________________________________________________________________
2 Приготовление раствора №3
Рассчитайте массу твердого вещества, которую необходимо добавить для приготовления раствора №3. На весах отмерьте необходимую навеску и добавьте в раствор №2 . Сколько грамм раствора получено?
2 Опишите ход выполнения опыта и наблюдения
_______________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Лабораторная работа №4
Тема: Реакции ионного обмена в растворах электролитов .
Цель: Провести реакции ионного обмена в растворах электролитов.
Оборудование: Штатив для пробирок, пробирки , растворы KOH ,FeSO4 ,ZnSO4 ,HCl, K2CO3
Ход работы:
1 Методические указания
Реакции ионного обмена — реакции, протекающие между ионами в растворе электролитов.
Для составления уравнений реакций ионного обмена необходимо помнить следующее:
Диссоциации не подвергаются: оксиды, газообразные вещества, вода, нерастворимые в воде соединения
Реакция ионного обмена идёт до конца если образуется: газ, осадок, вода
2Инструктаж по ТБ
1 Физиологическое действие используемых реактивов :
- Кислоты и щелочи вызывают ожоги на коже .
2 Меры безопасности :
Не допускать попадания кислоты и щелочи на руки или одежду
Осторожно использовать стеклянную посуду
3 Правила первой помощи
Пораженное кислотой место промыть большим количеством воды , или 2% раствором соды .
Пораженное щелочами место промыть большим количеством воды , или 1% раствором уксусной кислоты .
При необходимости обращаться к врачу
3 Выполнение работы:
Выполните следующие опыты, запишите результаты наблюдений , составьте уравнения реакций в молекулярном и ионном виде .
Опыт №1 Налейте в одну пробирку 1 мл раствораFeSO4 , а во вторую- такое же количество ZnSO4 добавьте в каждую раствор КОН.
В первой пробирке наблюдаете ___________________________________________
Уравнения реакций в молекулярном и ионном виде
---------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------
Во второй пробирке наблюдаете ___________________________________________
Уравнения реакций в молекулярном и ионном виде
---------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------
Опыт № 2
К полученным в предыдущем опыте осадкам добавьте раствор HCl.
Наблюдаете ___________________________________________________________________________
Уравнения реакций в молекулярном и ионном виде
---------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------
Во второй пробирке наблюдаете _______________________________________________________
Уравнения реакций в молекулярном и ионном виде
---------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------
Опыт №3
В пробирку налейте 1 мл раствора K2CO3 и добавьте 1-2 мл раствора HCl.
В пробирке наблюдаете _______________________________________________________________
Уравнения реакций в молекулярном и ионном виде
---------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------
Лабораторная работа 5
Тема : Химические свойства кислот на примере H2SO4
Цель: Изучить химические свойства кислот на примере серной кислоты
Оборудование: пробирки, штатив для пробирок.
Реактивы: железо, растворы серной кислоты, гидроксида калия, хлорида бария, сульфата меди (ІІ) , карбоната натрия, метилового оранжевого, фенолфталеина.
Ход работы:
2 Инструктаж по ТБ
1 Физиологическое действие используемых реактивов :
- Кислоты и щелочи вызывают ожоги на коже .
2 Меры безопасности :
Не допускать попадания кислоты и щелочи на руки или одежду. Осторожно использовать стеклянную посуду
3 Правила первой помощи
Пораженное кислотой место промыть большим количеством воды , или 2% раствором соды .
Пораженное щелочами место промыть большим количеством воды , или 1% раствором уксусной кислоты .
При необходимости обращаться к врачу
Выполнение работы
Опыт 1Действие кислоты на индикаторы.
К раствору серной кислоты добавьте раствор метилового оранжевого.
В пробирке наблюдаете _______________________________________________________________
Опыт 2 Взаимодействие серной кислоты с металлами.
К раствору серной кислоты добавьте железо .
В пробирке наблюдаете _______________________________________________________________
Уравнения реакций в молекулярном и ионном виде
---------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------
Опыт 3 Взаимодействие серной кислоты с основаниями.
А) растворимыми в воде.
К раствору гидроксида калия добавьте несколько капель фенолфталеина.
В пробирке наблюдаете _______________________________________________________________
Добавьте немного серной кислоты.
В пробирке наблюдаете _______________________________________________________________
Уравнения реакций в молекулярном и ионном виде
---------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------
б) нерастворимыми в воде.
К раствору сульфата меди (ІІ ) добавьте раствор гидроксида калия .
В пробирке наблюдаете _______________________________________________________________
Уравнения реакций в молекулярном и ионном виде
---------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------
Затем добавьте немного раствора серной кислоты.
В пробирке наблюдаете _______________________________________________________________
Уравнения реакций в молекулярном и ионном виде
---------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------
Дата добавления: 2020-04-25; просмотров: 157; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
