Роль структури речовин у патогенезі тривоги
З літератури відомо про вплив арілпіперазінової частини молекули і довжини метиленовогоспейсера на прояв аналогами буспіронуанксіолітичної активності і афінітету до 5-НТ1А рецепторам [26], однак,
роль циклічного іміду вивчена недостатньо. У роботах деяких авторів показано, що ліпофільний характер імідної частини молекули, похідних буспірону, відіграє важливу роль для прояву сполуками високого афінітету до 5-НТ1А рецепторів [27]. Інші дослідники припускають, що найбільш значний внесок у підвищенні афінітету до 5-НТ1А рецепторів носить стеричний фактор імідного фрагменту [28]. Вказується, що присутність термінального амідного фрагменту, відіграє важливу роль в стабілізації
5-НТ1Арецепторно-лігандного комплексу, і що ця взаємодія може
носити ліпофільний, електронний або стеричний [29 - 31] характер. Є дані про те, що з активним центром 5-НТ1А- рецептору здатні зв'язуватися такі об'ємні замісники у молекулі, розмір яких досягає 60 Ǻ, як наприклад, гідантоїн в молекулі арілпіперазіну [31]. Існує й інша гіпотеза, яка
припускає, що імідна функція не потрібна для зв'язування лігандів з
5-НТ1А- рецепторами [32].
Проводяться дослідження серед агоністів/антагоністів серотонінових5НТ1А- рецепторів й препаратів, що оказують неоднозначну дію (неповні агоністи5НТ1А- і антагоністи 5НТ2-рецепторів). У майбутньомуанксіолітична терапія, можливо буде пов'язана також з пошуком нових препаратів серед антагоністів збуджуючих амінокислот. Передатчиками збудження в специфічних закінченнях є глутамат і аспартат, до 40% збуджуючих синапсів мозку використовують їх як медіаторів. Відомі в даний час антагоністи цього класу рецепторів мають небажані побічні ефекти, найнеприємнішими з яких є психотоміметичний і амнестичний Також проводиться пошук анксіолітиків серед неповних рецепторних антагоністів збуджуючих амінокислот і аллостеричних модуляторів їх активності. Крім перелічених напрямів пошукові розробки ведуться серед аналогів нейроактивних пептидів: кортікотропінрілізінг-фактора, АКТГ, холецистокініну та інших, що приймають участь на різних етапах
у формуванні розгорнутої тривожної реакції. Пошук анксіолітиків проводиться серед речовин, що приймають участь у пригніченні тривоги
на різних етапах у формуванні розгорнутої тривожної реакції. Перспективний пошук нових препаратів, що мають мінімальну кількість побічних ефектів, які властиві бенздіазепіновим похідним, серед речовин,
що впливають на активність серотонінергічних процесів. Буспірон зв'язується з 5НТ1А-підтипомсеротонінових рецепторів, і є не повним його агоністом [22], не володіє гіпнотивними, міорелаксантними властивостями
і практично відсутня у нього седативна дія [23]; здатний надавати модулюючу дію на дофамінергичну передачу. Припускають, що в звичайних умовах серотонін знижує вивільнення дофаміну [24]. Вважається, що порушення дофаминергичної передачі, яке є супутнім у неспроможностісеротонінових процесів може лежати в основі формування обсесивно-компульсивних розладів. Аналіз літератури чітко показує, що вивчення буспіроноподібних сполук є перспективним і важливим напрямом психофармакології.
|
|
|
|
|
|
ЕКСПЕРИМЕНТАЛЬНА ЧАСТИНА
Матеріали та методи
У роботі використовувалися 90 білих безпородних щурів самців масою 180-200 г. Тварин тримали в звичайних умовах віварію на стандартному харчовому раціоні. В роботі були досліджені нові похідні нафталімідо(алкіл)піперазіну властивості сполуки1 - 3 (таблиця 1). Анксіолітичні вивчали на моделях "Конфліктнасітуація" [24] і "Відкрите поле" [25]. Досліджувані речовини йбуспірон вводили в дозі 10 мг/кг внутрішньоочеревно за 30 хвилин до початку експерименту..
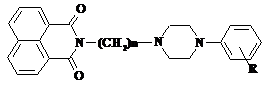
Таблиця 1.
Нові похідні нафталімідо(алкіл)піперазину
| № сполуки | n | R |
| 1 | 4 | H |
| 2 | 4 | о - Cl |
| 3 | 5 | п - Cl |
|
|
|
Синтез досліджених сполук був проведений в ПНДЛ №5 Одеського національного університету ім. І.І. Мечникова к.х.н., с.н.с., доцентом
С.Г. Соболєвої. Експериментально-дослідницька робота проведена у відділі медичної хімії у Фізико-хімічному інституті ім. О.В. Богатського НАН України, під безпосереднім керівництвом к.б.н. Замкової А.В. В якості еталону для порівняння отриманих результатів використовували буспірон (буспар, "LaboratoriesBristol", Франція). Статистичну обробку даних (обчилення середніх величин, помилок середніх величин, коефіцієнтукореляції, критерію Стьюдента) проводили з використанням програми "Microsoft Excel" для Windows-2000.
2.1.1. Методика “Конфликтної ситуації”
Методика заснована на зіткненні питного і оборонного рефлексів в момент споживання води з поїлки. Критерієм оцінки анксіолітичного ефекту було збільшення числа актів споживання води тваринами незважаючи на "наказуючу" стимуляцію - ноцицептивне (електробольове) роздратування.
Кількість тварин у кожній групі становило 10 [24].
2.1.2. Методика “Відкритого поля”
Методика "Відкритого поля" для оцінки орієнтовно - дослідницької поведенки. Під час перебування тварин у відкритому полі (3 хв.) Реєстрували число вставань на задні лапи (вертикальна рухова активність), число переходів з квадрата в квадрат (горизонтальна рухова активність), число заглядань в отвори.
|
|
|
Кількість тварин у кожній групі становило 10. [25].
Статистична обробка
Статистичну обробку даних (обчислення середніх величин, помилок середніх величин, коефіцієнта кореляції, критерію Стьюдента) проводили з використанням програми "Microsoft Excel" для Windows-2000.
3. ВСТАНОВЛЕННЯ ВПЛИВУ СТРУКТУРИ НА
АНКСІОЛІТИЧНУ АКТИВНІСТЬ НОВИХ ПОХІДНИХ НАФТАЛІМІДО(АЛКИЛ)ПІПЕРАЗИНУ ПРИ ВНУТРИШНЬООЧЕРЕВНОМУ ВВЕДЕННІ
3.1. Встановлення анксіолітичної активності в ряду нових похідних нафталімідо(алкіл)піперазіну на моделі "Конфліктної ситуації"
У даній роботі ми проаналізували зв'язок структура - анксіолітична активність в ряду нових похідних арілпіперазинів (1 - 3), в яких (рис. 1) імідна частина (частина А) була заміщена на нафлалімідний фрагмент, а арілпіперазінова частина (частина Б) містила атом хлору в різних положеннях фенілу, довжина вуглеводневого алкільного ланцюга варіювала - n = 4-5. Отримані нами дані свідчать про те, що наявність тамісцеположення атома хлору впливає на анксіолітичну активність досліджуваних сполук (рис. 1), а також від довжини вуглеводневого лінкеру.
З літератури відомо, що зменшення довжини метиленово ланцюга (n <3, 4) призводить до втрати анксіолітичної активності у похідних арілпіперазінів [33]. У наших дослідженнях, показано, що найбільш високу анксіолітичну активність, на рівні препарату порівняння буспірону, в тесті "Конфліктна сітуація", проявило похідне нафталімідо(алкіл)піперазіну, сполука 2 з довжиною метиленового ланцюжка n = 4.
Що стосується іншх вивчених похіднихарил піперазину, сполук (2та3)з кількістю метиленових атомів n = 4 та 5, відповідно,то було встановлено, що вони також володіють анксиолітичними властивостями, алеїхактивність яких декілька нижче ніж у препарату порівняння буспірону(рис. 2) однак це значення вище, ніж у контрольної групи тварин. У літературі зазначено, що пара- заміщені арилпіперазини, похідні буспірону, виявляють найменший анксіолітичну активність та афінітет до 5-НТ1А- рецепторів, що також підтверджено й отриманими нами результатами [35].
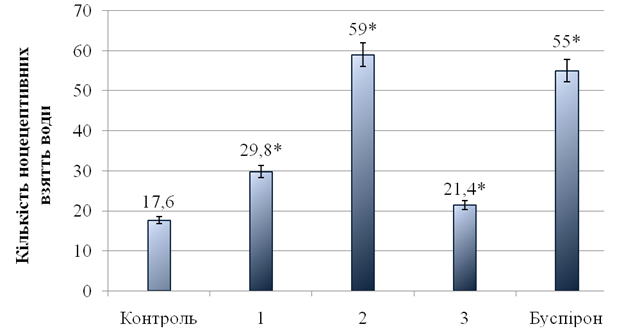
Рисунок 2. Анксіолітична активність нових похідних нафталімідо(алкил)піперазину (1 - 3) за методом “Конфліктної ситуації” в дослідах на щурах n = 3; при *при Р ≤ 0,05 по відношенню до контролю.
Таким чином, проведені нами дослідження дозволили виявити нафталімідо(алкіл)піперазини, які володіють анксіолітичними властивостями. Показано, что сполука 2 в тесті "Конфліктна ситуація" проявляє виразний анксіолітічній ефект та кількість покараних узять води тваринами повністю не відрізняється від препарату порівняння буспірону (рис. 2).
3.2. Вивчення анксіолітичних ефектів, похідних нафталімідо (алкіл) піперазину на моделі "Відкрите поле"
Буспірон та сполука 2: практичніше не знижують в тесті «Відкрите поле», загальну рухову активність щурів по відношенню до контролю, що узгоджується з даними літератури [36]. Сполука3, поряд знаявністю у неїанксіолітичноїактивністі, не змінює загальну рухову активність тварин в даному тесті, що свідчить про відсутність у неїо седативного ефекту (табл. 2).
Поява атому хлору у орто-положенніарилпіперазинової частини молекули сполуки 2 демонструє незначне зниження загальної рухової активност,і у порівнянні з контрольною групою тварин, до показників препарату порівняння буспірону.
Вітусністьбудь-якого замісника у арилпіперазиновій частині молекули сполуки 1, призводить до різкого зниження загальної рухової активності щодо буспірону та контрольної групи тварин, що свідчить про потужний седативний ефект(табл. 2).
Таблиця 2
Загальна рухова активність _____---__--__---
| Сполука № | “Відкрите поле” (загальна рухова активність) |
| Контроль | 26,5 ± 3,1 |
| 1 | 1,6 ± 0,5* |
| 2 | 17,4 ± 1,6* |
| 3 | 21,4 ± 1,9 |
| Буспірон | 19,6 ± 1,1* |
(* при Р ≤ 0,05)
Таким чином, нами було виявлено сполуки які як не проявляють седативний ефект, так й володіють виразною седативною дією, що може бути дуже корисним при використанні у медичній практиці.
Було вивчено 3 нових синтезованих сполуки, які належать до нових похідних нафталімідо(алкіл)піперазину.
На основі аналізу впливу структури на анксіолітичну активність, встановлено, що похідне нафталімідо(алкіл)піперазину 2 проявляє виразні анксіолітичні властивості на рівні препарату порівняння буспірону (59,0 покараних узять води).
Вивчені сполуки (1 -3) є перспективними для пошуку нових ефективних анксіолітичних засобів, які можуть знайти застосування в медичній практиці.
ВИСНОВКИ
Таким чином, на підставі отриманих експериментальних даних по вивченню впливу структури наанксіолітичні властивості у ряді нових похідних нафталімідо(алкіл)піперазину можна зробити наступні висновки.
1. Встановлено, що у ряді похідних нафталімідо(алкіл)піперазинуанксіолітична активність залежить від наявності замісника у арилпіперазиновій частині молекули та довжини вуглеводневого лінкеру. Найбільш оптимальна довжина вуглеводневого лінкеру, для вивчених нафталімідо(алкіл)піперазинів, складає n = 4.
2. Показано, що наявність таположення атома хлору молекулі впливає на анксіолітичну активність похідних нафталімідо(алкіл)піперазіну. Сполука, що містять атом хлору в орто-положенні з довжиною метиленовоголінкера n = 4 (сполука 2)проявлє найбільш виражену анксіолітичну активність на рівні препарату порівняння буспірону.
3. Виявлено, що атом хлору у арилпіперазиновій частинінафталімідний фрагмент (у якості імідної частини)у молекули можуть бути використані, для отримання сполук з високою анксиолітичною активністю.
7. СПИСОК ЦИТОВАНОЇЛИТЕРАТУРИ.
1. Лекарственные средства. МашковскийМ.Д., // Т. 1, Медицина, Москва, (1997), с. 83.--17
2. Механизмы действия анксиолитических противосудорожных иснотворных средств // АндронатиС.А., А.С. Яворский, В.М. Чепелев и др. – Киев: Наук.думка, 1985. – C. 256.--31
3. Модели тревоги на мышах: оценка в эксперименте и критика методики. Лапин И.П. // Эксперимент.и клин. Фармакол., 1993; т.63, №3, с. 58-62.-10
4. Новыеподходы к лечениютревоги.Жердев В.П., Воронина Т.А., Экономов А.Л., Мартынова Л.А. //Фармакол. и токсикол. – 1985. - №6. – C. 67-70.--28
5. Фармакологиеский скрининг веществ с буспироноподобным действием.ЛоуренсД.Р., БениттП.Н. // Клиническая фармакология, Т. 2, Медицина, Москва,(1993) сс. 346 – 347.--18
6. Феназепам.АндронатиС.А., АвруцкийГ.Я., БогатскийА.В. и др // 1982 – Киев: Наук.думка,. – C.142.--9
7. Характеристика фармакологических свойств феназепама. Воронина Т.А., Вихляев Ю.И., НеробковаЛ.Н. и др. // В. кн. Феназепам, Наук.думка Киев (1982), сс. 146 – 150.--19
8. Хвостатеядро. АрушанянЭ.Б., ОтеллинВ.А. //Л.: Наука, 1976.--7
9. Яп. заявка 3232864, (1991), РЖХим.СугихараХ., НисикаваК., 1993 17 о 41 п.--16
10. 5-(Piperidin-2-yl)- and 5(Homopiperidin-2-yl)-l,4-benzodiazepines, High-Affinity, Basic Ligands for the Cholecystokinm-B-Receptor. Castro J.L., Broughton H.B., RusselM.G.N. et al. // J. Med. Chem. - 1997, v. 40. - P. 2491-2501--30
11. 5-HT1ARecetors Agonists. Pierson M., Comstock J.M., Simmons R.D. et al. // J. Med. Chem. - 2000, v. 43. -P. 2350-2355--6
12. Analysis of Variation and Complexity in L-365,260. Competition Curves Radioligand Binding Assays. Harper E.A. Roberts S.P., ShankleyN.P. et al. // Br. J. Pharmacol. - 1996, Vol. 39. P. 5236-5245.--33
13. Antianxiety drugs in the aged.Petrie W. M, Ban T. A. // Ed. by Burrows G. D., Norman T. R., B. Davies Drugs in psychiatry vol.2 Antianxiety agents, 2004.- 143, Р. 57.--3
14. Cohtralled Modification of Aciditi in Cholecystokinin - B Receptor Antagonists: N – (1,4-Benzodiazepin-3-yl)-N’-[3-(tetrazol-5-ylano)phenil]ureas.Jose L. Richard G. Ball, Howard B. Broughton et al. // J.Med.Chem.1996,49,p.842-849.--12
15. Dose-depenpendent influence of buspirone in forced swimming test.Redrobe J.P. // Psycopharmacol., 1998.- 138, P. 219 – 198.--11
16. Essentialpsychopharmacology: Neuroscibasis a clinicalapplication.Stahl А., Stephen M. // CambridgeUniv. Press, 1996.- Р. 379.--26
17. Glennon R.A., NaimanN.A A New Potent Inhibitors of 5-HT1A Receptor // J. Med. Chem. - Vol. 31, № 10, p. 1968 – 1971.--13
18. MethodsforDrugDiscovery; ofPotent, SelectiveEffective, SerotoninAntagonists. HibertM. F., GittosM., MiddlemissD., et al. J. Med. Chem., 31, pp. 1087 – 1093 (1988). --21
19. Newantagonists 5-HT1ARecetors. Valverde0., Maldonado R., Foumie-Zaluski M.C. et al. // J. Phannacol. Exp. Ther. - 1994, v. 270. - P. 77-88 --8
20. New aspects in serotonin receptors research.NatorojanP.N., ChewS.T. // CanadianJournalofPharm. Sci., 8, (2), pp. 61 - 63 (1973).--15
21. Newderivativeswithanxiolyticproperties.Simon K, ArtmannG.H. //Neuropharmacology, 2010.- 12: 379, Р. 207.--27
22. Pharmacodynamics of buspirone.Lamberg T.S. Bock et al. // Еur. J. Clin. Pharmacol., 1998.- 54, P. 761 – 766.--32
23. PharmacologicalProfileof(R)-l-[2,3-Dihydro-1-(2-methylphenacyl)-2-oxo-5-phcnyl-1H-l,4-bcnzodiazepin-3-yl]-3-(3-methylphenyl)urea, a new Potent and Selective Serotonin 5-HT Receptor Antagonist in vitro and in vivo.Nishida A., Miyata К., Tsutsumil R. et al. // J. Pharmacol. Exp. Ther. - 1994, Vol. 269. - P. 725-731.--1
24. Potent Inhibitors of 5-HT1A Receptor.Glasser W. et al. // Drag. Future - 1988.- Vol. 13, №. 5.- P. 429 – 439.--14
25. Potent Inhibitors of Anxiety A Proposal on the Nature of the Binding Interaction between the Asp-Carboxylate of RGDXMimeticsStarke K, Altmann KP. // Neuropharmacol. - Vol. 12, p.1973, Р. 47.--5
26. Serotoninandpsychiatricdisorders. A keytonewtherapeuticapproaches.Costall B, NaylorRJ. //ArzneimForsh, 1991.- 42 (2A): 246, Р. 9.--22
27. Structure – affinity relationships studies on 5-HT1A receptors. SteenB.J., etal. // J. Med. Chem... – 1993. - 36;. – P. 2751-2760.--29
28. Thecombineduseofclinicalanxiolyticdrugs.GolitzD.F.,RohlR. // Drugs, 41, pp 11 – 18 (1991).--20
29. The face of emotion. Izard CE. // Appleton-Century-Crofts, 1971.- New-York.--2
30. Theneurochemistryofanxiety.Fail S. Drugsinpsychiatryvol.2Antianxietyagents,1984.- 13, Р. 33.--23
Дата добавления: 2018-06-27; просмотров: 196; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
