Невозможен вечный двигатель второго рода.
Энтропия.
Энтропия-функция состояния системы.
В термодинамикеприращение энтропии равно суммарному приведенному количеству теплоты, полученной системой:
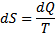

Отсюда следует, если система получает теплоту, то S возрастает, если система отдает теплоту, то S убывает.
Используя I закон термодинамики можно получить расчетные формулы для энтропии.
В статистической физике Больцман установил статистический, вероятностный смысл энтропии.
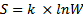
где k-постоянная Больцмана;
W- термодинамическая вероятность, равная числу способов, которыми может быть реализовано данное состояние системы.
Чем выше вероятность состояния системы, тем выше значение энтропии.
Равновесное состояние системы наиболее вероятное.
При переходе системы из неравновесного состояния в равновесное значение энтропии возрастает, достигая в равновесном состоянии максимального значения.
Установлено, что энтропия - мера хаоса, беспорядка в системе. Чем выше беспорябо, хаос в системе, тем больше значение энтропии.
В изолированной системе процессы протекают в направлении перехода системы в равновесное состояние (когда молекулы, энергия равномерно, хаотически распределены по системе). При этом энтропия системы возрастает.
Примеры с явлениями переноса.
Статистическая формулировка II закона термодинамики:
В изолированной системе все процессы протекают в направлении неубывания энтропии, т.е.
|
|
|

Третье начло термодинамики (теорема Нернста)
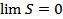
при Т→0
Тепловая «смерть» Вселенной.
Противоречие II закона термодинамики и закона эволюции живой материи.
Открытие Ильи Пригожина.
Дата добавления: 2018-05-12; просмотров: 180; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
