КИСЛОРОДОСОДЕРЖАЩИЕ ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
СПИРТЫ
СПИРТЫ – производные углеводородов, в которых один или несколько атомов водорода замещены на гидроксильную группу (ОН).
В зависимости от числа гидроксильных групп, спирты подразделяют на одно-, двух- и трёхатомные.
Одноатомные спирты
Общая формула гомологического ряда предельных одноатомных спиртов CnH2n+1OH.
В зависимости от того, при каком углеродном атоме находится гидроксильная группа, различают спирты
Первичные – R-CH2-OH
Вторичные – R2-CH-OH

Третичные – R3-C-OH

Номенклатура
Название спиртов образуют, добавляя окончание -ол к названию углеводорода с самой длинной углеродной цепью, включающей гидроксильную группу. Нумерацию цепи начинают с того края, ближе к которому расположена гидроксильная группа.
Например:


Изомерия одноатомных спиртов связана:
1) со строением углеродного скелета

2) с положением гидроксильной группы

Получение
1. Гидратация алкенов

Реакция идёт при пропускании алкена с парами воды над фосфорнокислым катализатором и протекает по правилу Марковникова.
2. Гидролиз алкилгалогенидов под действием водных растворов щелочей


3. Брожение сахаров (получение этанола)

4. Гидрирование оксида углерода

5. Восстановление карбонильных соединений:
а) при восстановлении альдегидов и сложных эфиров образуются первичные спирты

б) при восстановлении кетонов образуются вторичные спирты
|
|
|

Химические свойства спиртов
Различают два основных типа реакций спиртов с участием функциональной группы ОН.
I. Реакции с разрывом О–Н связи
1. Взаимодействие спиртов со щёлочными и щёлочноземельными металлами

Кислотные свойства спиртов выражены слабо. Спирты реагируют с металлами, но не взаимодействуют со щелочами.
2. При действии на спирты органических кислот (в присутствии минеральных кислот) образуются сложные эфиры

3. Спирты окисляются под действием окислителей (дихромата или перманганата калия) до карбонильных соединений:
а) первичные спирты окисляются до альдегидов, которые в свою очередь могут окисляться до карбоновых кислот

б) вторичные спирты окисляются до кетонов

в) третичные спирты окисляются только с разрывом С – С связи

II. Реакции с разрывом С−О связи.
1. Реакция дегидратации:
а) при сильном нагревании ( >150 оС)

б) при более слабом нагревании (<150 оС)

2. Обратимо реагируют с галогеноводородными кислотами (проявляют слабые основные свойства)

Многоатомные спирты
Двухатомные спирты (гликоли) содержат в молекуле две гидроксильные группы при разных углеродных атомах.
|
|
|
Первый представитель – этиленгликоль
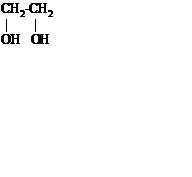
Трёхатомные спирты содержат три гидроксильные группы. Основной представитель – глицерин.

Получение
1. Гидролиз дигалогеналканов

2. Этиленгликоль образуется при окислении этилена водным раствором перманганата калия

3. Гидролизом жиров получают глицерин

Химические свойства
Для двух- и трёхатомных спиртов характерны основные реакции одноатомных спиртов. Взаимное влияние гидроксильных групп проявляется в том, что они более сильные кислоты, чем одноатомные спирты.
Соли двухатомных спиртов называются гликолятами, а соли трёхатомных спиртов – глицератами.
Качественной реакцией на многоатомные спирты, в которых гидроксильные группы находятся при соседних атомах углерода, является ярко-синее окрашивание при взаимодействии их с гидроокисью меди за счет образования комплексного соединения

При нитровании глицерина получается тринитроглицерин

Дата добавления: 2018-04-05; просмотров: 415; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
