Биосинтез глюкозы из аминокислот
Глюконеогенез – синтез глюкозы из неуглеводных продуктов. Такими продуктами или метаболитами являются в первую очередь молочная и пи-ровиноградная кислоты, так называемые гликогенные аминокислоты, гли-церол и ряд других соединений. Иными словами, предшественниками глюкозы в глюконеогенезе может быть пируват или любое соединение, превращающееся в процессе катаболизма в пируват или один из промежуточных продуктов цикла трикарбоновых кислот.
У позвоночных наиболее интенсивно глюконеогенез протекает в клетках печени и почек (в корковом веществе).
Большинство стадий глюконеогенеза представляет собой обращение реакции гликолиза. Только 3 реакции гликолиза (гексокиназная, фосфо-фруктокиназная и пируваткиназная) необратимы, поэтому в процесс глю-конеогенеза на 3 этапах используются другие ферменты. Рассмотрим путь синтеза глюкозы из пирувата.
Регуляция глюконеогенеза. Важным моментом в регуляции глюконеоге-неза является реакция, катализируемая пируваткарбоксилазой. Роль положительного аллостерического модулятора этого фермента выполняет ацетил-КоА. В отсутствие ацетил-КоА фермент почти полностью лишен активности. Когда в клетке накапливается митохондриальный ацетил-КоА, биосинтез глюкозы из пирувата усиливается. Известно, что ацетил-КоА одновременно является отрицательным модулятором пируватдегидроге-назного комплекса (см. далее). Следовательно, накопление ацетил-КоА замедляет окислительное декарбоксилирование пирувата, что также способствует превращению последнего в глюкозу.
|
|
|
Другой важный момент в регуляции глюконеогенеза – реакция, катализируемая фруктозо-1,6-бисфосфатазой – ферментом, который ингибиру-ется АМФ. Противоположное действие АМФ оказывает на фосфофруктокиназу, т. е. для этого фермента он является аллостерическим активатором. При низкой концентрации АМФ и высоком уровне АТФ происходит стимуляция глюконеогенеза. Напротив, когда величина отношения АТФ/АМФ мала, в клетке наблюдается расщепление глюкозы.
В 1980 г. группой бельгийских исследователей (Г. Херс и др.) в ткани печени был открыт фруктозо-2,6-бисфосфат, который является мощным регулятором активности двух перечисленных ферментов:
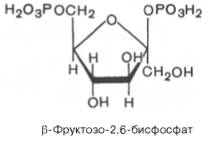
Фруктозо-2,6-бисфосфат активирует фосфофруктокиназу и ингибирует фруктозо-1,6-бисфосфатазу. Повышение в клетке уровня фруктозо-2,6-бис-фосфата способствует усилению гликолиза и уменьшению скорости глю-конеогенеза. При снижении концентрации фруктозо-2,6-бисфосфата отмечается обратная картина.
Установлено, что биосинтез фруктозо-2,6-бисфосфата происходит из фруктозо-6-фосфата при участии АТФ, а распадается он на фруктозо-6-фосфат и неорганический фосфат. Биосинтез и распад фруктозо-2,6-бис-фосфата катализируется одним и тем же ферментом, т.е. данный фермент бифункционален, он обладает и фосфокиназной, и фосфатазной активностью:
|
|
|
Показано также, что бифункциональный фермент в свою очередь регулируется путем цАМФ-зависимого фосфорилирования. Фосфорилирова-ние приводит к увеличению фосфатазной активности и снижению фосфо-киназной активности бифункционального фермента. Этот механизм объясняет быстрое воздействие гормонов, в частности глюкагона, на уровень фруктозо-2,6-бисфосфата в клетке (см. главу 16).
Активность бифункционального фермента регулируется также некоторыми метаболитами, среди которых наибольшее значение имеет гли-церол-3-фосфат. Действие глицерол-3-фосфата на фермент по своей направленности аналогично эффекту, который наблюдается при его фосфори-лировании с помощью цАМФ-зависимых протеинкиназ.
В настоящее время фруктозо-2,6-бисфосфат, помимо печени, обнаружен и в других органах и тканях животных, а также у растений и микроорганизмов.
Показано, что глюконеогенез может регулироваться и непрямым путем, т.е. через изменение активности фермента, непосредственно не участвующего в синтезе глюкозы. Так, установлено, что фермент гликолиза пиру-ваткиназа существует в 2 формах – L и М. Форма L (от англ. liver – печень) преобладает в тканях, способных к глюконеогенезу. Эта форма ингиби-руется избытком АТФ и некоторыми аминокислотами, в частности ала-нином. М-форма (от англ. muscle – мышцы) такой регуляции не подвержена. В условиях достаточного обеспечения клетки энергией происходит инги-бирование L-формы пируваткиназы. Как следствие ингибирования замедляется гликолиз и создаются условия, благоприятствующие глюконеоге-незу.
|
|
|
Наконец, интересно отметить, что между гликолизом, интенсивно протекающим в мышечной ткани при ее активной деятельности, и глюко-неогенезом, особенно характерным для печеночной ткани, существует тесная взаимосвязь. При максимальной активности мышц в результате усиления гликолиза образуется избыток молочной кислоты, диффундирующей в кровь, в печени значительная ее часть превращается в глюкозу (глюконеогенез). Такая глюкоза затем может быть использована как энергетический субстрат, необходимый для деятельности мышечной ткани. Взаимосвязь между процессами гликолиза в мышечной ткани и глю-конеогенезом в печени может быть представлена в виде схемы:
|
|
|
Показано также, что бифункциональный фермент в свою очередь регулируется путем цАМФ-зависимого фосфорилирования. Фосфорилирова-ние приводит к увеличению фосфатазной активности и снижению фосфо-киназной активности бифункционального фермента. Этот механизм объясняет быстрое воздействие гормонов, в частности глюкагона, на уровень фруктозо-2,6-бисфосфата в клетке (см. главу 16).
Активность бифункционального фермента регулируется также некоторыми метаболитами, среди которых наибольшее значение имеет гли-церол-3-фосфат. Действие глицерол-3-фосфата на фермент по своей направленности аналогично эффекту, который наблюдается при его фосфори-лировании с помощью цАМФ-зависимых протеинкиназ.
В настоящее время фруктозо-2,6-бисфосфат, помимо печени, обнаружен и в других органах и тканях животных, а также у растений и микроорганизмов.
Показано, что глюконеогенез может регулироваться и непрямым путем, т.е. через изменение активности фермента, непосредственно не участвующего в синтезе глюкозы. Так, установлено, что фермент гликолиза пиру-ваткиназа существует в 2 формах – L и М. Форма L (от англ. liver – печень) преобладает в тканях, способных к глюконеогенезу. Эта форма ингиби-руется избытком АТФ и некоторыми аминокислотами, в частности ала-нином. М-форма (от англ. muscle – мышцы) такой регуляции не подвержена. В условиях достаточного обеспечения клетки энергией происходит инги-бирование L-формы пируваткиназы. Как следствие ингибирования замедляется гликолиз и создаются условия, благоприятствующие глюконеоге-незу.
Наконец, интересно отметить, что между гликолизом, интенсивно протекающим в мышечной ткани при ее активной деятельности, и глюко-неогенезом, особенно характерным для печеночной ткани, существует тесная взаимосвязь. При максимальной активности мышц в результате усиления гликолиза образуется избыток молочной кислоты, диффундирующей в кровь, в печени значительная ее часть превращается в глюкозу (глюконеогенез). Такая глюкоза затем может быть использована как энергетический субстрат, необходимый для деятельности мышечной ткани. Взаимосвязь между процессами гликолиза в мышечной ткани и глю-конеогенезом в печени может быть представлена в виде схемы:
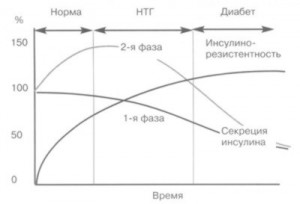
Аминокислоты и глицерин используются для синтеза глюкозы главным образом при голодании или при низком содержании углеводов в рационе (углеводное голодание). В этих условиях глюконеогенез служит для обеспечения глюкозой мозга, в то время как другие органы обеспечиваются энергией за счет окисления жирных кислот.Физиологическая роль глюконеогенеза из лактата существенно иная. Молочная кислота не является конечным продуктом обмена, но ее образование — это тупиковый путь метаболизма: единственный способ использования молочной кислоты связан с ее превращением вновь в пируват при участии той же лактатдегидро-геназы:Из клеток, в которых происходит гликолиз, образующаяся молочная кислота поступает в кровь и улавливается в основном печенью, где и превращается в пируват. Пируват в печени частично окисляется, частично превращается в глюкозу — цикл Кори, или глюкозо-лактатный цикл (рис. 9.24). Часть пирувата в мышцах путем трансаминирования превращается в аланин, который транспортируется в печень, и здесь снова образует пируват — глюкозо-аланиновый цикл.
Гликоген
ГЛИКОГЕН (от греч. glykys-сладкий и греч. -genes-рождающий, рожденный) (С6Н10О5)„, разветвленный полисахарид, молекулы к-рого построены из остатков-D-глюкопиранозы со связями 1 -> 4 в линейных участках и 1->6 в разветвлениях (ф-лу участка молекулы гликогена см. в ст. Гликозилтрансферазы). Точки ветвления во внутр. участках молекулы расположены через 3-4 остатка моносахарида, хотя в среднем одно разветвление приходится на 10-12 глюкозильных остатков.
Гликоген-аморфный продукт; мол. м. 106-109, + 196° (вода); хорошо раств. в воде (р-ры опалесцируют), из к-рой осаждается спиртом или (NH4)2SO4; раств. также в ДМСО; характеристич. вязкость 6,5-14,3 мл/г. К-тами гидролизуется, причем вначале образуются декстрины, а в конце р-ции - глюкоза. К действию конц. р-ров щелочей довольно устойчив. Водные р-ры гликогена окрашиваются иодом (410-490 нм), что используется для качеств. обнаружения полисахарида. Образует комплексы со мн. белками, напр. с альбумином и конканавалином А.
Гликоген содержится во всех тканях животных и человека и представляет собой резервное в-во (в растениях такие ф-ции выполняет крахмал), легко расщепляющееся под действием ряда ферментов до глюкозы. Обнаружен также в нек-рых бактериях, грибах и зернах растений. У человека Наиб. богаты гликогеном печень (2-6% от массы сырой ткани) и мышцы (до 2%). В тканях животных гликоген присутствует в виде частиц, наз. гликогеносомами. Наиб. крупные из них, т.н.-частицы (диам. 100-200 нм), собраны из-частиц (диам. 30-40 нм). Встречаются также еще более мелкие частицы (3-20 нм).
Биосинтез гликогена осуществляется с помощью ферментов гликозилтрансфераз. Исходным в-вом для синтеза может служить молекула олигосахарида, состоящая из остатков глюкозы, или белок, глюкозилированный в результате переноса на него остатка глюкозы с уридиндифосфатглюкозы. Гликоген расщепляется с помощью фермента фосфорилазы, переносящей остаток глюкозы на фосфорную к-ту с образованием -D-глюкозо-!-фосфата, и разл. гидролаз (напр.,-глюкозидазы), катализирующих гидролиз связей 1 -> 4 и 1 -> 6. Распад и синтез гликогена регулируется гормонами надпочечников и поджелудочной железы, напр. инсулином и адреналином.
Гликоген экстрагируют из тканей 60%-ным кипящим водным р-ром КОН, холодным р-ром трихлоруксусной к-ты или смесью фенола и воды с послед. осаждением этанолом; при этом гликоген частично разлагается. Нативный гликоген выделяют экстракцией водой на холоду в присут. солей Hg.
Нарушение обмена гликогена приводит к заболеваниям (гликогенозам), связанным с накоплением его в больших кол-вах в организме (гл. обр. в печени и сердце) или образованием молекул с отклонениями в строении.
===
Исп. литература для статьи «ГЛИКОГЕН»: Степаненко Б.Н., Боброва Л.Н., "Успехи биол. химии", 1976, т. 15, с. 195-207; Розенфельд Е. Л., Попова И. А., Гликогеновая болезнь, М., 1979; Geddes R., Harvey G. D., Wills P. R., "Biochem. J.", 1977, v. 163, № 2, p. 201-09. M.E. Преображенская.
О-ГЛИКОЗИД-ГИДРОЛАЗЫ (гликозидазы, карбогидразы), ферменты класса гидролаз, катализирующие гидролиз О-гликозидных связей в гликозидах, олиго- и полисахаридах, гликолипидах, гликопротеинах и др. гликоконъюгатах. О-Гликозид-гидролазы катализируют также обратные р-ции. Эти ферменты абсолютно специфичны к конфигурации как расщепляемой, так и синтезируемой гликозидной связи. Нек-рые типы О-гликозид-гидролаз катализируют перенос остатка углевода от гликозида, олиго- или полисахарида к соед., содержащему группу ОН (трансгликозилирование).
По механизму действия различают след. осн. типы О-гликозид-гидролаз: гликозидазы, или экзогликозидазы; эндогликаназы, или эндополисахаридазы; экзогликаназы, или экзополисахаридазы. Первые отщепляют от олигомерных субстратов концевые невосстанавливающие остатки моносахаридов. Для нек-рых из них доказан механизм, включающий промежут. образование соединения, в к-ром фермент и остаток углевода соединены ковалентной связью. Эндогликаназы (напр., лизоиим,-амилаза)расщепляют в полисахаридах гликозидную связь, удаленную от невосстанавливающего или восстанавливающего концов молекулы. Как гликозидазы, так и эндогликаназы расщепляют гликозидную связь с сохранением конфигурации аномерного атома углерода (C1 в циклич. форме моносахарида) и обладают трансгликозилирующей активностью. Экзогликаиазы (напр.,-амилаза) отщепляют от невосстанавливающего конца полисахарида моно- или олигосахаридные остатки с обращением их аномерной конфигурации и не обладают трансгликозилирующей активностью. Известны также эндогликозидазы, катализирующие отщепление олигосахаридных остатков от углеводных цепей гликопротеинов. Ниже представлен пример расщепления углевода под действием иамилаз (соотв. I и И):
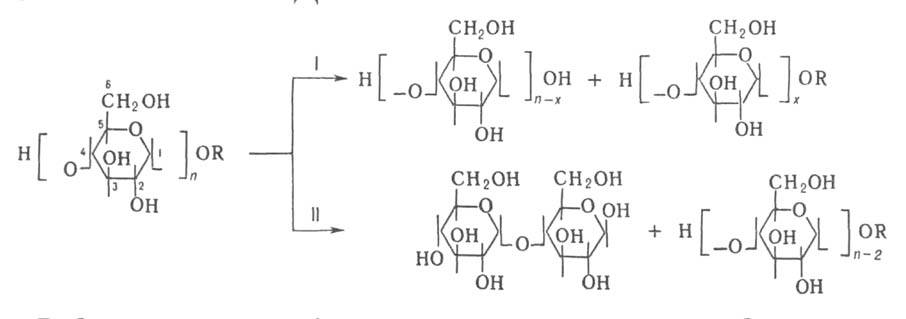
О-Гликозид-гидролазы обнаружены в вирусах и фагах, микроорганизмах, грибах, растениях, в клетках и тканях животных. Их главная ф-ция - участие в катаболизме сложных углеводов; они играют также важную роль в их биосинтезе (напр., крахмала, углеводных цепей гликопротеинов). Липидозы и др. болезни накопления обусловлены наследств. недостатком определенных О-гликозид-гидролаз.
Используют О-гликозид-гидролазы как реагенты в исследованиях сложных углеводов, как лек. ср-ва (напр., гиалуронидаза - для размягчения рубцов), в кач-ве бактерицидного ср-ва при консервировании продуктов питания (лизоцим), при облагораживании продуктов питания (напр., пектиназы), при "осахаривании" крахмала (амилазы). Представляет практич. интерес проблема переработки отходов пром-сти и с. х-ва, содержащих целлюлозу, в глюкозу с помощью ферментов целлюлазного комплекса, относящихся к О-гликозид-гидролазам.
Дата добавления: 2016-01-05; просмотров: 95; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
