Кинетика химических реакций – учение о скорости реакции и механизме ее протекания.
Скорость реакции uх.р. определяют по изменению количества (Dn) любого участника реакции за определенный отрезок времени (Dt), которое произошло в единице объема (V) системы или на единице площади поверхности (S) раздела фаз.
uгом.р-ции = ± Dn/V×Dt = ± Dc/Dt; uгет..р-ции = ± Dn/S×Dt
Влияние концентрации на uх.р. (закон действующих масс Гульдберга и Вааге 1867г.): При постоянной температуре скорость химической реакции прямо пропорциональна произведению концентраций (с) реагентов в степенях их стехиометрических коэффициентов (уравнение скорости).
В уравнение скорости входят только концентрации исходных веществ, находящихся в растворе или газообразном состоянии, так как концентрация твердой фазы и жидкости в избытке остается величиной постоянной.
| № | Уравнение реакции | Уравнение скорости реакции |
| 2А(р-р) + В(р-р) = С(р-р) | u = k с2(А) ×с(В) | |
| 2А(тв) + В(р-р) = С(газ) + Д(р-р) | u = kс(В) | |
| 2А(тв) + В(ж.изб.) = Д(р-р) | u = k |
с(А), с(В) – концентрации реагентов А и В, моль/л.
k - константа скорости реакции, не зависит от концентрации веществ; определяется для каждой реакции экспериментально.
Молекулярность реакции – число частиц (молекул или атомов), участвующих в элементарной реакции. Так реакции (1,2,3) трехмолекулярные.
Порядок реакции определяются уравнением скорости реакции, которое устанавливается экспериментально. Порядок реакции равен сумме показателей степеней при концентрациях в уравнении скорости.
|
|
|
Для элементарных гомогенных реакции порядок реакции равен ее молекулярности. Так, реакция (1) третьего порядка, реакция (2) первого порядка, реакция (3) нулевого порядка.
Влияние температуры на скорость реакции
Эмпирическое правило Вант-Гоффа: повышение температуры среды на каждые 100 увеличивает скорость большинства реакции в 2¸4 раза.
u2/u1 = gDt/10; g = k t+10/ k t = ut+10/ut = 2¸4; Dt = t2 – t1; t2 > t1
u2 и u1- скорости реакции при температурах t2 и t1.
Уравнение Аррениуса: k = А×е –Е а / RT
Где Еа – энергия активации реакции; А – постоянная для данной реакции;
е – основание натурального логарифма = 2,7183, R – газовая постоянная
Повышение t увеличивает в системе число активных частиц, обладающих энергией достаточной для акта химического взаимодействия (Е>Еа или Е=Еа).
Влияние катализатора на скорость реакции
Катализатор уменьшает энергию активации Еа реакции, тем самым увеличивает скорость процесса, но не изменяет тепловой эффект реакции (DН).
Уравнение Аррениуса: k1/k = exp (DЕа/RT) или lg (k1/k) = DЕа/2,3RT;
T = (0C + 273)K. DЕа = Еа - Еа1 R = 8,31 Дж/(моль×К)
k1 и k, Еа1 и Еа– константы скоростей реакции и энергии активации реакции в присутствии катализатора и без него.
|
|
|
7.2. Химическое равновесие химических реакций
Химическое равновесие – конечный результат любого обратимого процесса:uпрямой реакции = uобратной реакции; k прямой реакции = k обратной реакции
Концентрации веществ не изменяются, хотя реакции не прекращаются.
DG = 0. DG = DH - TDS; DH = TDS; Tравнов.= DH/DS.
Закон действующих масс в применении к равновесной системе выражается константой химического равновесия (К). В числителе ее – произведение равновесных концентрации продуктов в степенях их стехиометрических коэффициентов, а в знаменателе – произведение равновесных концентрации реагентов, также в степенях их стехиометрических коэффициентов.
Для гипотетической равновесной системы: mА(р-р) + nВ(р-р) «рС(р-р) + qД(р-р);
К=[С]p×[Д]q
К=[ А]m×[В]n
[С], [Д], [А], [В] – равновесные молярные концентрации веществ С, Д, А, В. Не включают в выражение К концентрации твердофазных веществ, а также концентрации жидкостей, взятых в избытке, их величины = const.
При К >>1 равновесие смещено вправо; uпр. >> uобр.
К <<1 равновесие смещено влево; uобр. >> uпр.
К = 1 равновероятны как прямая, так и обратная реакции.
Взаимосвязь константы равновесия К с изменением свободной энергии ГиббсаDG. DG = -2,3 RT lg K
|
|
|
При DG< 0; lg K>0; K>1
DG > 0; lg K<0; K<<1
DG = 0; lg K=0; К=1
Смещение равновесия подчиняется принципу Ле Шаталье
· с (реагентов) или ¯ с (продуктов) смещает равновесие вправо;
· Т среды смещает равновесие в сторону эндотермической реакции (DH>0); ·¯ Т среды увеличивает скорость экзотермической реакции (DH<0);
· давления смещает равновесие в сторону реакции, ведущей к уменьшению числа молекул газообразных веществ;
· введение катализатора не смещает химическое равновесие, не изменяет значение К, однако сокращает время наступления равновесия.
Вопрос №12
При растворении одновременно протекают два процесса:
· физический – диффузия растворенного вещества по всему объему растворителя и для твердых тел - разрушение структуры растворяемого вещества;
· химический – образование гидратов (гидратация) или сольватов (сольватация, если растворитель не вода), вследствие взаимодействия молекул растворителя с частицами растворенного вещества и ассоциатов, вследствие взаимодействия частиц растворенного вещества между собой.
Гидраты образуются за счет ион-дипольного взаимодействия, а также за счет водородных связей. Особенно склонны к гидратации ионы, которые за счет электростатического притяжения образуют гидратированные ионы. Образованием гидратов объясняются многие свойства растворов. Однако в некоторых случаях разрушение не происходит, и при выделении из раствора образуются кристаллы, содержащие связанную воду – кристаллогидраты. Например, CuSO4 × 5H2O(медный купорос), Na2SO4 × 10H2O (глауберова соль).
|
|
|
Таким образом,растворы – это сложные физико-химические системы, состоящие из растворителя, растворенного вещества и продуктов их взаимодействия (ассоциатов, гидратов различной прочности и состава), а процессрастворения – это сложный физико-химический процесс, сопровож-дающийся энергетическмие изменениями, вследствие свершения работы взаимодействия компонентов раствора между собой.
8.2. Факторы, влияющие на растворимость веществ
· Природа растворяемого вещества и природа растворителя.
Полярное или ионное соединение лучше растворяется в полярных растворителях (Н2О…), а неполярное вещество лучше растворяется в неполярных растворителях (С6Н6, СС14…).
· Температура среды:
t увеличивает растворимость тех твердых веществ, для которых DНр-рения>0 и уменьшает растворимость твердых веществ, если DНр-рения<0;
t уменьшает растворимость всех газообразных веществ, т.к. их DНр-рения<0;
· Давление влияет только на растворимость газа.
растворимость (S) газа при t=const прямо пропорциональна его парциальному давлению (закон Генри) S=kp
8.3. Термодинамика процесса растворения
· DG растворения всегда <0 (растворение – процесс самопроизвольный);
· DНр-рения твердого вещества может быть >0 и <0.
DНр-рения тв. в-ва = DНразрушения крист.решетки (всегда>0) +DНгидратации в-ва(всегда<0);
· DНр-рения газообразного вещества всегда <0:
· DSр-рения твердого вещества всегда >0;
· DSр-рения газообразного вещества всегда <0
8.4. Способы выражения концентрации раствора
Концентрация раствора – масса (г, кг) или количество (моль) растворенного вещества Х, содержащегося в определенном объеме (V) или массе (m) раствора.
· Массовая доля w растворенного вещества Х; безразмерная или %:
ω(X)=m(X)/m(р-ра) ω(X)%=m(X)*100%/m(р-ра)
m(р-ра)=p(р-ра)*V(р-ра)
· Молярная концентрация; моль/л или допускается М:
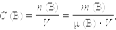
·Молярная концентрация эквивалента, ранее называли «нормальная или эквивалентная» концентрация; моль/л или допускается н:
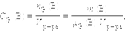
· Массовая концентрация или титр; г/мл:
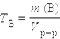
· с (fэкв (Х)) = z× с(Х) для одного и того же раствора, т.е. для одного и того же раствора молярная концентрация эквивалента или равна молярной концентрации (z=1) или больше ее в “z” раз.
* z оснований равно числу групп ОН, участвующих в реакции
Z (NaOH) = только 1; z (Са(ОН)2) м.б. = 1 и 2
z (кислот) равно числу атомов Н, участвующих в реакции
z (НС1) = только 1; z(H2SO4) м.б. = 1 и 2
z (солей) = валентность Ме × число атомов Ме.
Z (FeCI3) = 3×1 = 3; z(Na2SO4) = 1×2 = 2
ВОПРОС
Дата добавления: 2016-01-03; просмотров: 126; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
