Физическая природа электропроводности металлов.
Основные сведения о МЭТ. Материалы- это исходные вещества для производства продукции или вспомогательные вещества для проведения производственных процессов.Материалы делятся на:Сырье - это материалы, которые подлежат дальнейшей обработке (древесина, газ, руда).Полуфабрикаты - это материалы уже обработанные, но которые должны еще пройти стадии обработки для того чтобы стать готовым изделием.По общей специализации материалы делятся на: проводники, полупроводники, диэлектрики, магнитные материалы
Классификация материалов.
Материалы используемые в электронной технике, подразделяют на 1) электротехнические,
2) конструкционные, 3) специального назначения. Электротехническими называют материалы характеризуемые определенными свойствами по отношению к электромагнитному полю и применяемые в технике с учетом этих свойств. По поведению в магнитном поле электротехнические материалы подразделяют на сильномагнитные и слабомагнитные. Большинство этих материалов можно отнести к слабомагнитным. По поведению в электрическом поле материалы подразделяют на
1.Проводниковые– материалы основными свойствами которых является сильно выраженная электропроводность. 2.Полупроводниковые – материалы по удельной проводимости, являющиеся промежуточными между проводниковыми и диэлектрическими материалами отличительными свойствами которых является сильная зависимость удельной проводимости от концентрации примесей и дефектов, и их вида, а также от внешних энергетических воздействий. 3. Диэлектрические– материалы основными электрическими свойствами которых является низкая удельная электропроводность, а также способность к поляризации и в которых может существовать электростатическое поле.
|
|
|
Виды химической связи.
1.Ковалентная связь – химическая связь, образующаяся за счет обобществления электронов соседних атомов в общую электронную пару. При обобществлении электронов, происходит втягивание электронных облаков пространства между ядрами, появление состояния с повышенной плотностью электронного заряда в межъядерном пространстве и приводит к возникновению силы притяжения. Молекулы с ковалентной связью бывают полярными и неполярными. Молекулы, в которых центры полож. и отриц. совпадают называются неполярными, в которых не совпадают, называются полярными.
2.Ионная связь – это химическая связь, возникающая вследствие перехода электрона от металлического атома к металлоидному, и электростатического притяжения, разноименно заряженных ионов друг к другу. Этот вид связи реализуется в ионных кристаллах к которым относятся соли, оксиды, основания.
|
|
|
3.Металлическая связь – это химическая связь характерная для металлов, которая основывается на взаимопритяжении, положительно заряженного остова, образуемого кристаллической решеткой и электронного газа, имеющего отрицательный заряд и образуемого из свободных электронов. Притяжение между положительно заряженным остовом и электронным газом обуславливает целостность металлов. Специфика металлической связи заключается в том, что в обобществлении электронов, участвуют все атомы в кристаллах и обобществленные электроны, не локализуются около своих атомов, а свободно перемещаются вдоль всей решетки, образуя электронный газ.
4. Молекулярная связь или Ван дер Вальса –эта химическая связь образуется за счет межмолекулярного притяжения, при сопоставлении движения валентных электронов в соседних молекулах, при этом в любой момент времени, электроны должны быть максимально удалены друг от друга и максимально приближенны к положительным ядрам, тогда сила притяжения валентных электронов ядром соседней молекулы оказывается сильнее, силы взаимного отталкивания электронных оболочек этих молекул.
Особенности строения твердых тел.
|
|
|
Большинство материалов электронной техники представляют собой твердые тела, основная масса которых имеет кристаллическую решетку, обуславливающую периодическое электростатическое поле. Периодичность структуры является характерным свойством кристаллов. В периодической решетке всегда можно выделить элементарную ячейку, транслируя которую в пространстве легко получить представление о структуре всего кристалла. Кристаллические тела могут быть в виде отдельных кристаллов, монокристаллов или состоять из совокупности большого числа меньших кристалликов, зёрен. В случае поликристалла в пределах каждого зерна, атомы расположены периодически, но при переходе от одного зерна к другому, на границах раздела, регулярное расположение частиц нарушается. Кристаллов с идеальным строением не существует, происходят отклонения из-за дефектов. Их условно подразделяют на динамические или временные, и статические или постоянные. Динамические дефекты возникают при механических, тепловых или электромагнитных воздействиях на кристалл при прохождении через него потока частиц высокой энергии. Среди статических дефектов различают атомные или точечные, протяженные дефекты. Атомные могут проявляться в виде незанятых узлов решеток, называемых вакансиями в виде смещения атома из узла в междоузлие, в виде внедрения в решетку чужеродных атомов иди ионов. К протяженным дефектам относятся дислокации, то есть смещение, поры, трещины, границы зёрен и др. Некоторые твердые вещества обладают способностью образовывать не одну, а две или более кристаллические структуры, устойчивые при различных температурах, называют полиморфизмом.
|
|
|
Зонная теория твердого тела.
Зонная теория ТТ – это теория валентных электронов, движущихся в потенциальном периодическом поле в кристаллической решетке. Отдельные атомы могут иметь отдельный энергетический спектр, то есть электроны могут занимать лишь определенные энергетические уровни. Часть этих уровней, заполнена при нормальном невозбужденном состоянии атома, на других уровнях атомы могут находится лишь тогда, когда атом подвергается внешнему энергетическому воздействию, то есть когда он возбужден. Энергетическая диаграмма атома –эта диаграмма показывает энергетическое состояние валентных электронов в атоме и самого атома. (E – энергия валентных электронов, E0 – основной уровень энергии атома характеризующий минимально возможное значение атома, Ei – энергия ионизации) Возбужденное состояние атома – это такое состояние когда атом обладает энергией, большей по сравнению с минимально возможной. При сближении атомов, происходит перекрытие электронных оболочек, а это в свою очередь существенно изменяет характер движения электронов. Благодаря перекрытию оболочек, электроны могут без изменения энергии, посредством обмена, переходить от одного атома к другому. То есть перемещаться по кристаллу и становиться обобществленным, вследствие этого, дискретные энергетические уровни изолированного атома, расщепляются в энергетические зоны. Разрешенные энергетические зоны разделены запрещенными интервалами энергии, каждая из запрещенных энергетических зон, состоит из множества энергетических уровней, их количество определяется числом атомов, составляющих твердое тело, нижнюю заполненную валентными электронами зону, называют валентной, она соответствует энергетическим уровням валентных электронов. Валентную зону называют зоной проводимости, дно этой зоны соответствует энергии ионизации атомов, составляющих твердое тело. В запрещенной зоне, уровни энергии отсутствуют, характер энергетического спектра у проводников, полупроводников, диэлектриков существенно различаются. В проводниках валентная зона перекрывается зоной проводимости, в полупроводниках и диэлектриках, зоны проводимости и валентная зона разделены некоторым энергетическим зазором называемым запрещенной зоной. К полупроводникам относят вещества, у которых запрещенная зона меньше 3-ех ЭВ. С более широкой, относят к диэлектрикам. У реальных диэлектриков ширина ЗЗ может достигать 10 ЭВ.
В полупроводниках и диэлектриках при низких температурах, все электроны находятся в валентной зоне, а зона проводимости абсолютно свободна. Для проявления электропроводности, электроны необходимо перевести из валентной зоны в зону проводимости. Энергии электрического поля недостаточно, для осуществления такого перехода, требуется более сильное энергетическое воздействие. При переходе электронов из валентной зоны в зону проводимости в валентной зоне появляются энергетические вакансии, называемые дырками.
Общие свойства проводников.
К твердым проводникам относят металлы, сплавы и модификации углерода. К жидким проводникам относят расплавы металлов и электролиты. Все проводники делятся на два рода. Механизм протекания токов по металлам обусловлен движением электронов (электронная проводимость, проводники I рода). К проводникам II рода относят растворы кислот, щелочей, солей и ионные растворы (перенос заряда через ионы). Газы в обычных состояниях проводниками не являются, однако в результате ионизации в них может проявляться проводимость. Предельным случаем является плазма – сильно ионизированный газ с квазиравновесием положительных и отрицательных зарядов. Плазма очень хороший проводник – равновесная проводящая среда. В металлах проводимость электронная, электроны имеют маленькую массу (9,1 10-31 кг)и хорошую подвижность, поэтому они не только переносят энергию, но и выравнивают скорости движения атомов и молекул по объему, сравнивая температуру по образцу. Следовательно, все металлы имеют хорошую теплопроводность. При 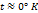 в металлах наблюдаются сложные квантовые эффекты.
в металлах наблюдаются сложные квантовые эффекты.
Физическая природа электропроводности металлов.
В основу классической электронной теории металлов положено представление об электронном газе, состоящем из свободных коллективизированных электронах. Приложение внешнего напряжения, приводит к увеличению количества электронов в направлении действующих сил поля, то есть, электроны получают некоторую добавочную скорость направленных движений, благодаря чему и возникает электрический ток. Плотность тока в проводнике равна  , е – заряд электрона, n – концентрация свободных электронов, V – средняя скорость направленного движения носителей заряда. Называемая скоростью дрейфа. Удельная проводимость равна
, е – заряд электрона, n – концентрация свободных электронов, V – средняя скорость направленного движения носителей заряда. Называемая скоростью дрейфа. Удельная проводимость равна  ,l – средняя длина свободного пробега электронов, m0 масса электрона, U – средняя плотность теплового движения. Электроны в металле переносят не только электрический заряд, но и выравнивают в нем температуру. Обеспечивая высокую теплопроводность. Молекулярная теплоемкость, кристаллической решетки любого ТТ составляет 3R, где R- универсальная газовая постоянная. Квантовая статистика базируется на принципе Паули – согласно которому в каждом энергетическом состоянии в атоме может находится только один электрон. В квантовой теории вероятность заполнения энергетических состояний электронами определяется функцией Фирни
,l – средняя длина свободного пробега электронов, m0 масса электрона, U – средняя плотность теплового движения. Электроны в металле переносят не только электрический заряд, но и выравнивают в нем температуру. Обеспечивая высокую теплопроводность. Молекулярная теплоемкость, кристаллической решетки любого ТТ составляет 3R, где R- универсальная газовая постоянная. Квантовая статистика базируется на принципе Паули – согласно которому в каждом энергетическом состоянии в атоме может находится только один электрон. В квантовой теории вероятность заполнения энергетических состояний электронами определяется функцией Фирни
 , где E – энергия уровня, вероятность заполнения которого определяется EF – энергия Фирни, k- постоянная Больцмана, T- температура. Энергия Фирни определяет максимальное значение энергии, которую может иметь электрон в металле при температуре абсолютного нуля, эту энергию называют так же уровнем Фирни. Соответствующий ей потенциал называется электрохимическим потенциалом
, где E – энергия уровня, вероятность заполнения которого определяется EF – энергия Фирни, k- постоянная Больцмана, T- температура. Энергия Фирни определяет максимальное значение энергии, которую может иметь электрон в металле при температуре абсолютного нуля, эту энергию называют так же уровнем Фирни. Соответствующий ей потенциал называется электрохимическим потенциалом
 .
.
Дата добавления: 2018-05-12; просмотров: 3528; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
