Максимуми поглинання алкалоїдів
| Речовина | Розчинник | λ |
| 1 | 2 | 3 |
| Хінін | 0,05М сульфатна кислота | 250, 316, 346 |
| Морфін | Етанол | 287 |
| 0,1М гідроксид натрію | 250 і 296 | |
| 0,05М сульфатна кислота | 284 | |
| Кодеїн | Етанол | 286 |
| Нікотин | Етанол | 260 |
| Атропін | 0,05М сульфатна кислота | 252, 258, 264 |
| Кокаїн | Етанол | 230, 274, 281 |
| 0,05М сульфатна кислота | 233, 275, (281-згин) | |
| Стрихнін | Етанол | 255 |
| 0,05М сульфатна кислота | 255 | |
| Ефедрін | 0,05М сульфатна кислота | 251, 256, 262 |
| Хінін | Етанол | 236, 278, 332 |
| 0,05М сульфатна кислота | 250, 316, 346 |
Ідентифікація за УФ-спектрами можлива тільки після ретельного очищення екстракційним методом і ТСХ- методом, або при їхньомусполученні.
Кількісне визначенняпроводиться спектральними (УФ-спектрофотометрія, фотоелектроколориметрія, екстракційна фотометрія) і хроматографічними методами (тонкошарова хроматографія - планіметричний і денситометричний методи; газо-рідинна хроматографія і рідинна хроматографія).
Тема: ХІМІКО-ТОКСИКОЛОГІЧНИЙ АНАЛІЗ СИНТЕТИЧНИХ
ЛІКАРСЬКИХ» ОТРУТ ОСНОВНОГО ХАРАКТЕРУ.
План лекції
1. Застосування, токсикологічна характеристика, методи виділення з біологічного мamepіалу і методи аналізу похідних фенотіазіну.
Застосування, токсикологічна характернстика, методи виділення з біологічного матеріалу і методи аналізу похідних фенотіазіну.

|
|
|
Похідні фенотіазіну відносяться до нейролептиків. В основі будови даної групи сполук лежить фенотиазинове кільце. Різноманіття похідних фенотіазіну зумовлено радикалами в положенні 2 і 10. З цієї групи сполук найбільше значення в хіміко-токсикологічному відношенні мають:
| Препарат | R1 | R2 |








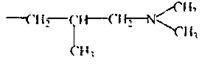
Фізико-хімічні властивості
Основний характер похідних фенотіазіну зумовлений наявністю в структурі молекули гетероциклічного атома азоту (рКа 4) і третинного атома азоту в аліфатичному радикалі (рКа 9,1 - 9,8).
При взаємодії з кислотами фенотіазіни утворюють солі - білі чи кремові порошки, розчинні у воді, спирті, хлороформі, але не розчинні в ефірі і бензолі.
Основи являють собою сиропоподібну масу, не розчинну у воді, але розчинну в спирті, ефірі, хлороформі.
Застосування
Похідні фенотіазіну (аміназин, дипразин, тизерцин) мають седативну дію, снодійний, антигистамінний ефекти. Препарати підсилюють дію наркотичних, снодійних і анальгезуючих засобів.
Похідні фенотіазіну застосовуються для лікування безсоння, психічних захворювань, алергій, дерматитів.
|
|
|
Токсична дія.
Препарати характеризуються нейротоксичним ефектом, викликають психічні збудження, порушення діяльності серцево-судинної системи, диспептичні явища, збудження гемодинаміки.
При прийомі терапевтичних доз можливі ускладнення: падіння артеріального тиску, частішання серцебиття, сухість у роті, світлобоязнь, сонливість.
При гострих отруєннях похідними фенотіазіну настає коматозний стан, що характеризується розширенням зіниць, спадом температури тіла, відбувається різке пригнічення дихального і судинорухомого центрів, з'являється тахікардія, нитковидний пульс. Смерть настає при легенево-серцевій недостатності.
Смертельна доза аміназину (для дорослих) – 5-10 г.
Поведінка в організмі.
Похідні фенотіазіну як речовини основного характеру переважно всмоктуються з кишковика, активно зв'язуються з білками, що зумовлює їхню здатність до кумуляції в організмі.
Препарати локалізуються в мозку, печінці, нирках. Виводяться нирками, в сечі виявляються в основному у вигляді метаболітів.
Метаболізм похідних фенотіазину проходить в наступних напрямках:
а) диметилирование
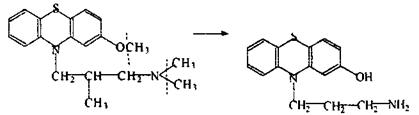
|
|
|
тизерцин 2-гідрокси-10-(3’-амінопропіл)-
фенотіазин
б) окислення гетероциклічного атома сірки в сульфоксид і сульфон
дипразин сульфоксид
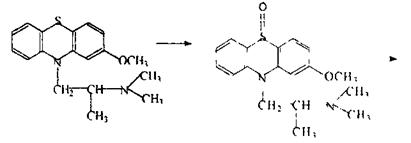
сульфон

в) ароматичне гидроксилювання в 3 і 6 положеннях з наступним кон’югуванням з глюкороновою кислотою:
|

Направлений хіміко-токсикологічний аналіз на похідні фенотіазину проводять відповідно до схеми:
Об'єкти дослідженя - мозок, печінка, нирки, шлунок з вмістом,
промивні води, легені, сеча.
Ізолюванняпрепаратів проводиться за методами К.М.Саломатіна –
модифікованим методам Cтаса-Oтто (1) і Сшедзинського (2) з
врахуванням фізико-хімічних властивостей похідних фенотіазіну і стану біологічного матеріалу.
Методи характеризуються використанням амфіфильних розчинників – етанолу (1) і ацетонітрилу (2), що допускає наявність великої кількості співекстрактивних домішок. Для руйнування зв'язку отрута - білок (рН 2-3) застосовуються кислоти - оксалатна (1) і хлористоводнева (2). При виділенні у водну фазу основи фенотіазинів утворюють солі, добре розчинні у воді, хлороформі, але погано розчинні в ефірі, що використовується для очищення витяжки від домішок. Крім екстракції ефіром домішок очищення витяжок проводять осадження білків 96 % спиртом, фільтруванням (1), а також висолюванням домішок за допомогою розчину Nа2SO4(2).
|
|
|
Враховуючи, що фенотіазіни - сильні основи, їхнє виділення з водної в ефірну фазу проводиться при рН 13, для чого водні витяжки подлужнюють розчином NaOH.

Водна фаза

Ефірна фаза
Для додаткового очищення проводиться реекстракція препаратів 0,5 % розчином Н2SO4, в який переходять солі фенотіазинів і сульфатної кислоти, домішки залишаються в ефірній фазі.
ТСХ-скринінгпроводиться в загальній системі розчинників - хлороформ диоксан - ацетон - 25 % розчин аміаку (45:47,5:5:2,5); сорбент - силікагель КСК; проявники - концентровані кислоти (Н2SO4, KNO3, HC1), а також розчини окислювачів НСlO4 і NaNO2; реактиви Марки, Манделіна.
Наявність плям рожевого і бузковго кольору в 3-їй зоні (Rf = 0,63-0,83) вказує на можливість присутності у витяжці похідних фенотіазіну.
Отруту із сорбенту силікагелю виділяють елюентом – метанол-диетиламін (9:1) з наступним проведенням підтверджуючого етапу в окремій системі розчинників - хлороформ - етанол (20:1) і циклогексан - ацетон (5:1); сорбент - основний окис алюмінію.
В якості «свідків» використовуються хлороформні розчини препаратів даної групи. Для проведення наступного етапу аналізу фенотіазіни елюють розчинниками метанол - диетиламін (9:1).
Очищення. Етап скринінга методом тонкошарової хроматографії дозволяє паралельно проводити якісне очищення від біогенних домішок, що локалізуються на хроматографічних пластинках в областях Rf <0,2 і Rf> 0,8.
Однак, в елюаті можлива присутність залишків домішок, що видаляються з використанням методів: екстракційного, гель-хроматофафії; електрофорезу; сполучення екстракційного і ТСХ-методів.
Підтверджуючі дослідження елюату включають найбільш чутливі хімічні і фізико-хімічні методи аналізу похідних фенотіазіну.
Хімічні реакції:
1. Реакції осадженняз загальноалкалоїдними осадовими реактивами (пікринова кислота; сіль Рейнеке; реактиви Драгендорфа, Марме; Майєра, Зонненшейна й ін.).
Аморфні або кристалічні осади з нехарактерною формою частинок вказують на наявність гетероциклічного атома азоту в препаратах. Реакції високочутливі, не специфічні.
2. Реакції забарвленнязасновані переважно на хімічних процесах окислювання, дегідрування, конденсації з альдегідами з використанням концентрованих кислот - Н2SO4, HNO3, НС1, НСlO4; реактиви Фреде; Манделіна; Марки; розчинів солей FeCl3, NaNO2.

Продукти реакцій забарвлені в червоно-фіолетовий, синювато-червоний кольори. Реакції забарвлення чутливі, не специфічні.
4. Мікрокристалічні реакції - більшість фенотіазінів утворюють характерні кристалічні осади із сіллю Рейнеке, однак диференціація окремих представників цієї групи за формою кристалів важка
Фізико-хімічні методи аналізу
Дата добавления: 2018-05-09; просмотров: 521; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
