II уровень. Вспомним основные положения теории
Nbsp; ФИЗИКА. 11 класс. Задание № 40 Тема: Первое начало термодинамики. Теплоемкость газа. Адиабатный процесс
I уровень. Познакомимся с параграфом
1. Первое начало термодинамики
Первое начало термодинамики – один из двух основных законов термодинамики, представляет собой закон сохранения энергии для систем, в которых существенное значение имеют тепловые процессы.
Первое начало термодинамики было сформулировано в середине XIX века в результате работ немецкого ученого Ю. Р. Майера, английского физика Дж. Джоуля и немецкого физика Г. Гельмгольца.
Согласно первому началу термодинамики термодинамическая система может совершать работу только за счет своей внутренней энергии или каких-либо внешних источников энергии.
При сообщении термодинамической системе некоторого количества теплоты  в общем случае изменяется ее внутренняя энергия на
в общем случае изменяется ее внутренняя энергия на 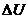 и система совершает работу
и система совершает работу  :
:  .
.
Количество теплоты, сообщенное системе, расходуется на увеличение ее внутренней энергии и на работу, совершаемую системой против внешних сил.
С учетом того, что работа внешних сил  противоположна работе системы
противоположна работе системы  (
(  ), первое начало термодинамики можно переписать в виде:
), первое начало термодинамики можно переписать в виде:  .
.
Изменение внутренней энергии системы равно сумме сообщенного ей количества теплоты и работы, произведенной над системой внешними силами.
· Вечный двигатель первого рода – устройство, которое может совершать полезную работу, превышающую затраченную, т.е. имеющее коэффициент полезного действия  .
.
|
|
|
Первый закон термодинамики утверждает, что невозможно построить такой периодически действующий двигатель, который совершил бы работу большую, чем энергия, которая подводится к двигателю извне: вечный двигатель первого рода невозможен.
Действительно, если в периодически действующем двигателе газ, пар или другое рабочее тело совершает круговой процесс, то изменения его внутренней энергии не происходит, 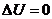 и
и  . Работа, совершаемая этим телом, не может превосходить подведенного к нему количества теплоты.
. Работа, совершаемая этим телом, не может превосходить подведенного к нему количества теплоты.
2. Применение первого начала термодинамики к различным процессам
Изохорный процесс. 
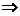
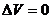 .
. 
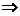
 .
.
Изменение внутренней энергии равно количеству переданной теплоты.
Количество переданной теплоты  , где
, где  – теплоемкость газа при постоянном объеме. Изменение внутренней энергии представим как
– теплоемкость газа при постоянном объеме. Изменение внутренней энергии представим как  , приравнивая, получим
, приравнивая, получим 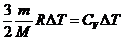
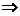
 .
.
Изобарный процесс.  ;
;  .
.
Передаваемое газу количество теплоты идет на увеличение внутренней энергии газа и совершение работы против внешних сил.
 – работа газа,
– работа газа,  – количество теплоты,
– количество теплоты,  – изменение внутренней энергии.
– изменение внутренней энергии.
|
|
|
Тогда 
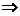
 , где
, где 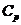 – теплоемкость газа при постоянном давлении.
– теплоемкость газа при постоянном давлении.
Изотермический процесс. 
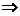
 ;
; 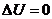
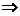
 .
.
Все переданное газу количество теплоты идет на совершение газом работы. Если газ отдает тепло, то работа газа отрицательна, а внешних сил – положительна.

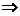
 .
.
3. Адиабатный процесс
Процесс в теплоизолированной системе называютадиабатным.Т. е. процесс осуществляется без теплообмена с внешней средой. При адиабатном процессе 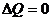 и согласно уравнению
и согласно уравнению  изменение внутренней энергии происходит только за счет совершения работы:
изменение внутренней энергии происходит только за счет совершения работы:  .
.
Нельзя окружить систему оболочкой, абсолютно не допускающей теплопередачу. Но в ряде случаев можно считать реальные процессы очень близкими к адиабатным. Для этого они должны протекать достаточно быстро, так, чтобы за время процесса не произошло заметного теплообмена между системой и окружающими телами.

Так как 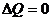 , то теплоемкость при адиабатном процессе
, то теплоемкость при адиабатном процессе 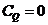 .
.
II уровень. Вспомним основные положения теории
1. Сформулируйте первое начало термодинамики и запишите его математическое выражение.
2. Примените первое начало термодинамики к изохорному процессу.
3. Примените первое начало термодинамики к изобарному процессу.
4. Примените первое начало термодинамики к изотермическому процессу.
|
|
|
5. Какой процесс изменения состояния газа называется адиабатным? Примените первое начало термодинамики к адиабатному процессу.
Дата добавления: 2018-04-15; просмотров: 290; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
