II уровень. Вспомним основные положения теории
Тема: Теплота и работа. Работа в термодинамике. Количество теплоты. Эквивалентность теплоты и работы
I уровень. Познакомимся с параграфом
1. Работа в термодинамике
 В термодинамике движение тела как целого не рассматривается. При совершении работы меняется объем тела, а его скорость остается равной нулю. Но скорости молекул меняются, поэтому меняется температура. При совершении работы в термодинамике меняется состояние макроскопических тел: их объем и температура.
В термодинамике движение тела как целого не рассматривается. При совершении работы меняется объем тела, а его скорость остается равной нулю. Но скорости молекул меняются, поэтому меняется температура. При совершении работы в термодинамике меняется состояние макроскопических тел: их объем и температура.
Для вычисления механической работы, совершаемой термодинамической системой, рассмотрим идеальный газ под поршнем в цилиндре. Пусть под действием силы давления газа  поршень поднялся на высоту
поршень поднялся на высоту  . При этом совершена работа
. При этом совершена работа 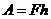 . Сила давления, действующая со стороны газа на поршень площадью поперечного сечения
. Сила давления, действующая со стороны газа на поршень площадью поперечного сечения  ,
,  , где
, где  – давление газа. Таким образом, работа газа
– давление газа. Таким образом, работа газа  . Здесь
. Здесь  – изменение объема газа в цилиндре при перемещении поршня.
– изменение объема газа в цилиндре при перемещении поршня.

 При расширении газ совершает положительную работу против внешних сил
При расширении газ совершает положительную работу против внешних сил  . При сжатии газа совершается отрицательная работа
. При сжатии газа совершается отрицательная работа  . Она совершается теми внешними телами, которые создали внешнее давление.
. Она совершается теми внешними телами, которые создали внешнее давление.
2. Геометрическая интерпретация работы
При изобарном процессе работа расширения изображается на диаграмме 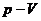 площадью заштрихованного прямоугольника.
площадью заштрихованного прямоугольника.
 В общем случае надо процесс разбить на малые части и сосчитать элементарные работы, а затем их сложить. Полная работа газа при произвольном процессе численно равна площади под всем графиком от начального состояния
В общем случае надо процесс разбить на малые части и сосчитать элементарные работы, а затем их сложить. Полная работа газа при произвольном процессе численно равна площади под всем графиком от начального состояния  до конечного состояния
до конечного состояния  .
.
|
|
|
Работа расширения, совершаемая системой, зависит от характера процесса изменения его состояния. На рисунке изображены три различных процесса, переводящих газ из состояния (1) в состояние (2). Во всех трех случаях газ совершает различную работу. Работа в термодинамике является функцией процесса и не является функцией состояния. Следовательно, работу можно вычислять указав процесс, в котором участвует термодинамическая система: изобарный, изотермический, изохорный.
3. Количество теплоты
Количество теплоты – часть внутренней энергии, переданной в процессе теплообмена от одного макроскопического тела к другому без совершения работы.
Является функцией процесса. Телу необходимо сообщать разные количества теплоты для перевода его из одного состояния в другое в зависимости от того, через какие промежуточные состояния оно при этом проходит. Например, для нагревания данной массы газа на  в изохорном процессе требуется меньшее количество теплоты, чем для такого же нагревания в изобарном процессе.
в изохорном процессе требуется меньшее количество теплоты, чем для такого же нагревания в изобарном процессе.
В Международной системе единиц (СИ) количество теплоты, как и работа, измеряется в джоулях. Для измерения количества теплоты применяется и внесистемная единица – калория:  .
.
|
|
|
4. Опыт Джоуля
 В сороковых годах ХIХ столетия английский физик Джеймс Прескотт Джоуль (1818 – 1889) провёл серию экспериментальных исследований с целью выяснить, существует ли точное количественное соотношение между теплотой и механической работой. Устройство, с помощью которого Дж. Джоуль в 1847 г. доказал, что механическая и тепловая энергия могут переходить из одной формы в другую, и измерил механический эквивалент количества теплоты, состояло из двух массивных тел, подвешенных на нитях так, что при своем движении вниз они раскручивали систему погруженных в воду легких лопастей. Сосуд с водой был теплоизолирован. Таким образом, нагревание воды можно было отнести за счет механической работы, совершенной вращающимися лопастями, которые, в свою очередь, получали кинетическую энергию вращения за счет изменения потенциальной энергии опускающихся грузов. Если признать справедливость закона сохранения энергии в любых формах, то механическая работа должна равняться количеству теплоты, затраченной на нагревание воды.
В сороковых годах ХIХ столетия английский физик Джеймс Прескотт Джоуль (1818 – 1889) провёл серию экспериментальных исследований с целью выяснить, существует ли точное количественное соотношение между теплотой и механической работой. Устройство, с помощью которого Дж. Джоуль в 1847 г. доказал, что механическая и тепловая энергия могут переходить из одной формы в другую, и измерил механический эквивалент количества теплоты, состояло из двух массивных тел, подвешенных на нитях так, что при своем движении вниз они раскручивали систему погруженных в воду легких лопастей. Сосуд с водой был теплоизолирован. Таким образом, нагревание воды можно было отнести за счет механической работы, совершенной вращающимися лопастями, которые, в свою очередь, получали кинетическую энергию вращения за счет изменения потенциальной энергии опускающихся грузов. Если признать справедливость закона сохранения энергии в любых формах, то механическая работа должна равняться количеству теплоты, затраченной на нагревание воды.
Джоуль сравнил значения 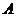 в
в  (сам Джоуль употреблял, конечно, другие единицы работы) и
(сам Джоуль употреблял, конечно, другие единицы работы) и  в калориях, которые являются устаревшими единицами измерения количества теплоты (
в калориях, которые являются устаревшими единицами измерения количества теплоты (  равна тому количеству теплоты, которое нужно, чтобы нагреть
равна тому количеству теплоты, которое нужно, чтобы нагреть  воды на
воды на  в интервале от
в интервале от  до
до  ). Полученный Джоулем результат (
). Полученный Джоулем результат (  ) несколько отличался от известного теперь. Однако следует признать, что для своего времени точность опыта Джоуля была очень высокой.
) несколько отличался от известного теперь. Однако следует признать, что для своего времени точность опыта Джоуля была очень высокой.
|
|
|
· Механический эквивалент теплоты:  .
.
· Калориметр – (от лат. calor – тепло и греч. metron – мера, metreo – измеряю), прибор для измерения количеств теплоты, выделяющейся или поглощающейся при различных физических, химических или биологических процессах. Название возникло, когда энергия, переданная от одного тела к другому в ходе теплопередачи, измерялась в калориях. Конструкция калориметра должна предусматривать уменьшение тепловых потерь во внешнюю среду.
Ученые:
· Дж. П. Джоуль
II уровень. Вспомним основные положения теории
1. По какой формуле вычисляется работа, совершенная постоянной силой давления газа при его расширении или сжатии?
2. Что называют количеством теплоты? В каких единицах измеряется количество теплоты?
3. Как геометрически можно определить работу газа с помощью графика зависимости 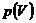 ?
?
|
|
|
4. Что называется механическим эквивалентом теплоты?
5. Какой прибор называют калориметром? Опишите устройство калориметра.
Дата добавления: 2018-04-15; просмотров: 249; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
