ЗАДАЧІ ДЛЯ САМОСТІЙНОГО РОЗВ’ЯЗУВАННЯ
2.00. В ємності V = 0,5 л міститься газ за нормальних умов. Визначити число N молекул газу, що знаходяться в колбі.
2.01. В балоні ємністю V = 5 л міститься кисень масою m = 20 г.
Визначити концентрацію n молекул у балоні.
2.02. Визначити кількість речовини водню, що знаходиться в балоні об’ємом V = 3 л, якщо концентрація молекул газу  .
.
2.03. Визначити кількість речовини 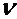 та число N молекул азоту масою m = 0,2 кг.
та число N молекул азоту масою m = 0,2 кг.
2.04. Який об’єм за нормальних умов має суміш 4 кг кисню та 2 кг азоту?
2.05. Визначити: 1) число N молекул води, що займають при температурі  об’єм
об’єм 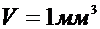 ; 2) масу цих молекули води.
; 2) масу цих молекули води.
2.06. Одна третина молекул азоту масою m = 10 г розпалась на атоми. Визначити повне число N частинок, що міститься в такому газі.
2.07. В ємності об’ємом V = 4 л знаходиться водень масою m = 1 г. Яке число молекул n містить одиниця об’єму?
2.08. В ємності знаходиться суміш кисню та водню. Маса суміші
m = 3,6 г. Маса кисню 0,6 г. Визначити кількість речовини 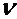 суміші, а також
суміші, а також  та
та  кожного газу окремо.
кожного газу окремо.
2.09. В балоні знаходиться газ при температурі  . До якої температури
. До якої температури  потрібно нагріти газ, щоб його тиск збільшився у 2 рази?
потрібно нагріти газ, щоб його тиск збільшився у 2 рази?
2.10. Кисень масою 12 г знаходиться в об’ємі 2 л, причому відомо, що 40% молекул дисоціювало на атоми. Знайти концентрацію частинок в одиниці об’єму а також кількість речовини  і
і  кожної компоненти.
кожної компоненти.
2.11. При нагріванні ідеального газу на  при постійному тиску об’єм його збільшився на
при постійному тиску об’єм його збільшився на  початкового об’єму. Знайти початкову температуру T газу.
початкового об’єму. Знайти початкову температуру T газу.
|
|
|
2.12. Маса m = 12г газу займає об’єм V = 4 л при температурі  . Після нагрівання газу при постійному тиску його густина стала
. Після нагрівання газу при постійному тиску його густина стала  . До якої температури нагріли газ?
. До якої температури нагріли газ?
2.13. В посудині об’ємом V = 2 л знаходиться маса 
та маса  при температурі
при температурі  . Визначити тиск суміші в посудині.
. Визначити тиск суміші в посудині.
2.14. В балонах об’ємом  знаходиться газ. Тиск у першому балоні
знаходиться газ. Тиск у першому балоні  у другому –
у другому –  Визначити загальний тиск р та парціальні тиски після з’єднання балонів, якщо температура не змінилась.
Визначити загальний тиск р та парціальні тиски після з’єднання балонів, якщо температура не змінилась.
2.15. В балоні об’ємом V = 20 л знаходиться  масою m = 500 г під тиском p = 1,3 МПа. Визначити температуру газу.
масою m = 500 г під тиском p = 1,3 МПа. Визначити температуру газу.
2.16. Газ при температурі T = 309 К і тиску р = 0,7 МПа має густину  . Визначити відносну молярну масу газу М.
. Визначити відносну молярну масу газу М.
2.17. В балоні об’ємом V = 25 л знаходиться водень при температурі Т = 290 К. Після того як частину водню використали, тиск в балоні знизився на  Визначити масу m витраченого водню.
Визначити масу m витраченого водню.
2.18. В циліндрі під поршнем знаходиться повітря під тиском  при температурі
при температурі  . Який вантаж треба покласти на поршень після нагрівання повітря до температури
. Який вантаж треба покласти на поршень після нагрівання повітря до температури  , щоб об’єм повітря в циліндрі не змінився? Площа поршня S = 30 см
, щоб об’єм повітря в циліндрі не змінився? Площа поршня S = 30 см  .
.
2.19. Яка температура Т газу, який знаходиться під тиском
р = 0,5 МПа, якщо в ємності об’ємом V = 15 л знаходиться  молекул? Газ вважати ідеальним.
молекул? Газ вважати ідеальним.
|
|
|
2.20. В балоні V = 50 л знаходиться 0,12 кмоль газу під тиском  . Визначити середню кінетичну енергію теплового руху молекул газу.
. Визначити середню кінетичну енергію теплового руху молекул газу.
2.21. Визначити середню кінетичну енергію поступального руху молекул і температуру газу, якщо під тиском  концентрація молекул газу
концентрація молекул газу  .
.
2.22. При якій абсолютній температурі середня кінетична енергія молекули одноатомного газу буде рівною  ?
?
2.23. Визначити кінетичну енергію теплового руху всіх молекул, що знаходяться в 1 кмоль водню при температурі  .
.
2.24. Розрахувати кінетичну енергію, що припадає на одну ступінь вільності молекули азоту при T = 1000 К, а також кінетичну енергію руху молекули.
2.25. Водень знаходиться при температурі Т = 300 К. Знайти середню кінетичну  енергію обертального руху однієї молекули, а також сумарну кінетичну енергію
енергію обертального руху однієї молекули, а також сумарну кінетичну енергію  усіх молекул цього газу; кількість водню
усіх молекул цього газу; кількість водню  моль.
моль.
2.26. Знайти внутрішню енергію (теплову) маси m = 1 г повітря при температурі  . Молярна маса повітря М = 0,029.
. Молярна маса повітря М = 0,029.
2.27. Енергія поступального руху молекули азоту, що знаходиться в об’ємі V = 20 л,  = 5 кДж, а середня квадратична швидкість його молекул
= 5 кДж, а середня квадратична швидкість його молекул  . Знайти масу m азоту в балоні і тиск р, під яким він знаходиться.
. Знайти масу m азоту в балоні і тиск р, під яким він знаходиться.
2.28. За нормальних умов водень займає об’єм V = 1 л. Визначити число N молекул в цьому об’ємі, що мають швидкості, менші за  .
.
|
|
|
2.29. Яка частина молекул кисню при  має швидкості від
має швидкості від  до
до  ?
?
2.30. Визначити молярну масу М двоатомного газу та його питомі теплоємності, якщо відомо, що різниця питомих теплоємностей  –
–  цього газу дорівнює
цього газу дорівнює  .
.
2.31. Знайти питомі  та
та  , а також молярні
, а також молярні  та
та  теплоємності газу
теплоємності газу  .
.
2.32. Визначити показник адіабати  ідеального газу, який при температурі Т= 350 К і тиску р = 0,4 МПа має об’єм V = 300 л і теплоємність
ідеального газу, який при температурі Т= 350 К і тиску р = 0,4 МПа має об’єм V = 300 л і теплоємність 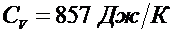 .
.
2.33. Ємність V = 6 л містить двоатомний газ за нормальних умов. Визначити теплоємність  цього газу.
цього газу.
2.34. Визначити молярні теплоємності газу, якщо його питомі теплоємності  та
та  .
.
2.35. Знайти питомі  та
та  та молярні
та молярні  та
та  теплоємності азоту та гелію.
теплоємності азоту та гелію.
2.36. Обчислити питомі теплоємності газу, якщо його молярна маса  , а відношення теплоємностей
, а відношення теплоємностей  /
/  = 1,67.
= 1,67.
2.37. Трьохатомний газ під тиском р = 240 кПа та при температурі  займає об’єм V = 10 л. Визначити теплоємність
займає об’єм V = 10 л. Визначити теплоємність  цього газу при постійному тиску.
цього газу при постійному тиску.
2.38. Одноатомний газ за нормальних умов займає об’єм V = 5 л. Обчислити теплоємність  цього газу при постійному об’ємі.
цього газу при постійному об’ємі.
2.39. За нормальних фізичних умов певний газ має питомий об’єм  . Визначити його питомі теплоємності
. Визначити його питомі теплоємності  та
та  .
.
|
|
|
2.40. При якому тиску р середня довжина вільного пробігу < l > молекул азоту дорівнює 1м, якщо температура Т газу дорівнює 700 К?
2.41. Балон ємністю V = 20 л містить водень масою m = 1 г. Визначити середню довжину пробігу молекул < l >.
2.42. Знайти середнє число зіткнень <z>, що припадає на молекулу кисню за час t = 1 с за нормальних умов.
2.43. Знайти число N усіх зіткнень, які відбуваються протягом t = 1 с між всіма молекулами водню, що займає за нормальних умов об’єм 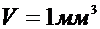 .
.
2.44. Середня довжина вільного пробігу атомів гелію за нормальних умов дорівнює 180 Нм. Визначити коефіцієнт дифузії D гелію.
2.45. Обчислити коефіцієнт дифузії D азоту: 1) за нормальних умов; 2) під тиском р =100 Па і при температурі Т = 300 К.
2.46. Знайти середню довжину вільного пробігу < l > молекул азоту за умови, що його динамічна в’язкість  .
.
2.47. Знайти динамічну в’язкість гелію  за нормальних умов, якщо коефіцієнт дифузії D за тих же умов дорівнює
за нормальних умов, якщо коефіцієнт дифузії D за тих же умов дорівнює  .
.
2.48. Визначити густину 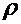 розрідженого водню, якщо середня довжина вільного пробігу < l > молекул дорівнює 1 см.
розрідженого водню, якщо середня довжина вільного пробігу < l > молекул дорівнює 1 см.
2.49. За нормальних умов середня довжина вільного пробігу < l > молекули кисню дорівнює 100 Нм. Яка середня арифметична швидкість <  > молекули кисню за цих умов?
> молекули кисню за цих умов?
2.50. Водень займає об’єм V = 10  під тиском
під тиском  . Газ нагріли при постійному об’ємі до
. Газ нагріли при постійному об’ємі до  . Визначити: 1) зміну внутрішньої енергії газу
. Визначити: 1) зміну внутрішньої енергії газу  ; 2) роботу газу A; 3) кількість теплоти Q, що передана газу.
; 2) роботу газу A; 3) кількість теплоти Q, що передана газу.
2.51. Кисень нагрівають при незмінному тиску р = 80 кПа. Його об’єм збільшується від  до
до  . Визначити: 1) зміну внутрішньої енергії кисню
. Визначити: 1) зміну внутрішньої енергії кисню  ; 2) роботу розширення газу; 3) кількість теплоти Q, що передана газу.
; 2) роботу розширення газу; 3) кількість теплоти Q, що передана газу.
2.52. Азот нагрівали при постійному тиску, причому йому було передано кількість теплоти Q = 21 кДж. Визначити роботу А, яку виконав при цьому газ, та зміну його внутрішньої енергії  .
.
2.53. Азот масою m = 200 г розширюється ізотермічно при температурі Т = 280 К, причому об’єм газу збільшується у два рази. Знайти: 1) зміну внутрішньої енергії газу  ; 2) виконану газом роботу А; 3) кількість теплоти Q, отриману газом.
; 2) виконану газом роботу А; 3) кількість теплоти Q, отриману газом.
2.54. В циліндрі під поршнем знаходиться азот масою m = 0,6 кг, що займає об’єм  при температурі Т = 560 К. В результаті нагрівання газ розширився до
при температурі Т = 560 К. В результаті нагрівання газ розширився до  при незмінній температурі. Знайти: 1) зміну внутрішньої енергії газу
при незмінній температурі. Знайти: 1) зміну внутрішньої енергії газу  ; 2) виконану газом роботу А; 3) кількість теплоти Q, передану газу.
; 2) виконану газом роботу А; 3) кількість теплоти Q, передану газу.
2.55. При ізотермічному розширенні кисню, кількість речовини якого  , а температура Т = 300 К, було передано кількість теплоти
, а температура Т = 300 К, було передано кількість теплоти
Q = 2 кДж. У скільки разів збільшився об’єм газу?
2.56. При розширенні водень виконав роботу А = 6 кДж. Визначити кількість теплоти Q, що передана газу, якщо процес проходив:
1) ізобарно; 2) ізотермічно.
2.57. При адіабатичному стисненні кисню масою m = 29 г його внутрішня енергія збільшилась на  , а температура підвищилась до
, а температура підвищилась до  . Знайти: 1) підвищення температури
. Знайти: 1) підвищення температури  ;
;
2) кінцевий тиск  газу, якщо початковий тиск
газу, якщо початковий тиск 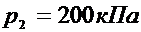 .
.
2.58. При адіабатному стисненні газу його об’єм зменшився в
n = 10 разів, а тиск збільшився в k = 21,4 рази. Визначити відношення  теплоємностей газу.
теплоємностей газу.
2.59. Кисень, що займає об’єм  під тиском
під тиском  , адіабатно розширився до
, адіабатно розширився до 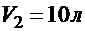 . Визначити роботу А розширення газу.
. Визначити роботу А розширення газу.
2.60. Газ, що виконує цикл Карно, віддав теплоту  . Визначити температуру
. Визначити температуру  , якщо при температурі
, якщо при температурі 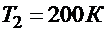 робота циклу А = 6 кДж.
робота циклу А = 6 кДж.
2.61. Газ, що виконує цикл Карно, віддав 67% отриманої теплоти. Визначити температуру  , якщо
, якщо  .
.
2.62. У скільки разів збільшиться коефіцієнт корисної дії  циклу Карно при підвищенні температури від
циклу Карно при підвищенні температури від  до
до  ? Температура
? Температура  .
.
2.63. Газ, що виконує цикл Карно, отримує теплоту Q = 84 кДж. Визначити роботу газу А, якщо температура  у три рази вища від температури
у три рази вища від температури  .
.
2.64. У циклі Карно газ отримав теплоту  і виконав роботу А = 100 Дж. Температура
і виконав роботу А = 100 Дж. Температура  . Визначити
. Визначити  .
.
2.65. Ідеальний газ, що виконує цикл Карно, 2/3 кількості теплоти  віддає теплоприймачу, температура якого
віддає теплоприймачу, температура якого  . Визначити температуру
. Визначити температуру  .
.
2.66. Газ, що виконує цикл Карно, отримав теплоту  і виконав роботу А = 2,4 кДж. Визначити температуру
і виконав роботу А = 2,4 кДж. Визначити температуру  , якщо температура теплоприймача
, якщо температура теплоприймача  .
.
2.67. Ідеальний газ виконує цикл Карно. Температура  в чотири рази більша від температури
в чотири рази більша від температури  теплоприймача. Яку частку
теплоприймача. Яку частку  кількості теплоти, отриманої за один цикл, газ віддає теплоприймачу?
кількості теплоти, отриманої за один цикл, газ віддає теплоприймачу?
2.68. Ідеальний газ, що виконує цикл Карно, отримав кількість теплоти Q = 4,2 кДж і виконав роботу А = 590 кДж. Знайти термічний к.к.д.  цього циклу. У скільки разів температура
цього циклу. У скільки разів температура  більша від температури
більша від температури  теплоприймача?
теплоприймача?
2.69. Холодильна машина, що працює за циклом Карно, підтримує в камері температуру  . За кожний цикл машина відводить від холодильної камери Q = 40 кДж енергії та передає її навколишньому середовищу, що має температуру Т = 300 К. Визначити потужність, яку споживає холодильник, якщо тривалість циклу t = 1,5 с.
. За кожний цикл машина відводить від холодильної камери Q = 40 кДж енергії та передає її навколишньому середовищу, що має температуру Т = 300 К. Визначити потужність, яку споживає холодильник, якщо тривалість циклу t = 1,5 с.
2.70. Чому дорівнює поверхневий натяг рідини, якщо маса крапель, що витікають з капілярної трубки діаметром 1,86 мм, складає 1 г.
2.71. Яку роботу А треба виконати, щоб видуваючи мильну кульку, збільшити її діаметр від  до
до  . Процес вважати ізотропним.
. Процес вважати ізотропним.
2.72. Маса 100 г крапель спирту, що витікає з капіляру, дорівнює 0,71 г. Визначити поверхневий натяг  спирту, якщо діаметр d шийки краплі в момент відриву дорівнює 1 мм.
спирту, якщо діаметр d шийки краплі в момент відриву дорівнює 1 мм.
2.73. Трубка має діаметр  . На нижньому кінці трубки висить крапля води, що має в момент відриву форму кульки. Знайти діаметр
. На нижньому кінці трубки висить крапля води, що має в момент відриву форму кульки. Знайти діаметр  цієї краплі.
цієї краплі.
2.74. Повітряна бульбашка діаметром d = 2 мкм знаходиться у воді біля самої поверхні. Визначити густину 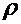 повітря в бульбашці, якщо повітря над поверхнею води знаходиться при нормальних умовах.
повітря в бульбашці, якщо повітря над поверхнею води знаходиться при нормальних умовах.
2.75. Дві краплі ртуті радіусом r =1 мм кожна злились в одну велику краплю. Яка енергія Е виділилась при цьому злитті? Вважати процес ізотермічним.
2.76. На скільки тиск повітря всередині мильної бульбашки більший від атмосферного тиску  , якщо діаметр бульбашки d = 5 мм?
, якщо діаметр бульбашки d = 5 мм?
2.77. Гліцерин піднявся в капілярній трубці на висоту h = 20 мм. Визначити поверхневий натяг  гліцерину, якщо діаметр d каналу трубки дорівнює 1 мм.
гліцерину, якщо діаметр d каналу трубки дорівнює 1 мм.
2.78. У воду опустили на дуже малу глибину скляну трубку з внутрішнім діаметром 1 мм. Знайти масу m води, що знаходиться в трубці.
2.79. Капілярна трубка діаметром d = 0,5 мм наповнена водою. На нижньому кінці трубки вода висить у вигляді краплі радіусом r = 3 мм. Знайти висоту h стовпчика води в трубці.
ДОВІДКОВІ МАТЕРІАЛИ
Таблиця 1. Основні фізичні постійні
Постійна Авогадро NA 6,02×1023 моль-1
Постійна Больцмана (k) 1,38 ×10–23 Дж/К
Універсальна газова постійна (R) 8,31 Дж/К× моль
| Таблиця 3. Властивості деяких рідин
| ||
| Речовина | Поверхневий натяг, Н/м | Густина, кг/м3 |
| Спирт Вода Гліцерин Ртуть | 0,02 0,073 0,064 0,5 | – 1,0×103 1,2×103 13,6×103 |
Дата добавления: 2018-04-05; просмотров: 1433; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
