Уравнения затухающих колебаний
Получим дифференциальное уравнение свободных затухающих колебаний на примере реального пружинного маятника, совершающего колебания в среде с сопротивлением (простейший случай - трение о воздух). Пусть масса маятника m, коэффициент упругости пружины k, сила сопротивления, действующая на маятник, F = - bv, v - скорость маятника, b - коэффициент сопротивления среды, в которой находится маятник. Так как мы рассматриваем только линейные системы, b = const, k = const. x - смещение маятника от положения равновесия.
Второй закон Ньютона в нашем случае запишется так:

Это уравнение и есть дифференциальное уравнение свободных затухающих колебаний пружинного маятника. Его, однако, принято записывать в следующем, так называемом каноническом виде:

 - коэффициент затухания,
- коэффициент затухания,  - собственная частота свободных (незатухающих) колебаний пружинного маятника, то, что раньше мы обозначали просто .
- собственная частота свободных (незатухающих) колебаний пружинного маятника, то, что раньше мы обозначали просто .
Уравнение затухающих колебаний в таком (каноническом) виде описывает затухающие колебания всех линейных систем; конкретная колебательная система отличается только выражениями для и .
2) Термодинамические параметры. Равновесное состояние системы, обратимые и необратимые процессы. Циклы.
| |||||||
| Термодинамической системой называется совокупность макроскопических тел, которые могут обмениваться между собой энергией и веществом.
Примером термодинамической системы являются: газ; жидкость и находящийся в соприкосновении с ней пар. Термодинамическая система может находиться в различных состояниях, отличающихся: температурой - Т, давлением - Р, объёмом - V, плотностью-r и т.д. Физические величины, характеризующие состояние термодинамической системы, называются параметрами состояния, или термодинамическими параметрами. Термодинамическими параметрами являются: (Т, Р, V) или (Т, r, V). Параметры состояния системы не всегда имеют определенные значения. Состояние термодинамической системы будет называться неравновесным, если хотя бы один из параметров этого состояния не имеет определенного значения. Например, если тело с одной стороны подогревать, а с другой охлаждать, то температура в разных точках тела будет разной, и телу, как целому, нельзя будет приписать определенное значение температуры. Состояние термодинамической системы будет называться равновесным, если все параметры системы имеют определенные значения, не изменяющиеся с течением времени. Термодинамическая система, не обменивающаяся с внешней средой ни энергией, ни веществом, называется замкнутой или изолированной.
Если термодинамическую систему, находящуюся в неравновесном состоянии - изолировать, то она перейдет в равновесное состояние. Термодинамическим процессом называется любое изменение в термодинамической системе, связанное с изменением хотя бы одного из её параметров, или термодинамический процесс - это переход системы из одного состояния в другое. Этот переход связан с нарушением равновесия системы. Равновесным процессом называется такой процесс, который состоит из ряда следующих друг за другом равновесных состояний. Равновесный процесс - бесконечно медленный процесс. При бесконечно медленном сжатии газа поршнем в цилиндре давление газа будет иметь в каждый момент определенное значение, а процесс будет равновесным. При изменении направления равновесного процесса (например, замена сжатия расширением газа) система будет проходить через те же равновесные состояния. Но в обратной последовательности. Поэтому равновесные процессы называют обратимыми. Равновесные процессы - идеализированные процессы. Рассмотрим равновесный обратимый (1-2,-) и необратимый (1-2,-) процессы.
Рис. 39.1. Равновесный обратимый и необратимый процессы. Процесс, при котором система после ряда изменений возвращается в исходное состояние, называется круговым процессом или циклом. На координатной плоскости цикл изображается замкнутой кривой.
| |||||||
БИЛЕТ-7
1) Третий закон Ньютона. Закон сохранения импульса, принцип реактивного движения.
Импульсом тела называется величина, равная произведению массы тела на его скорость.
Импульс обозначается буквой  и имеет такое же направление, как и скорость.
и имеет такое же направление, как и скорость.
Единица измерения импульса: 
Импульс тела вычисляется по формуле:  , где
, где 

Изменение импульса тела равно импульсу силы, действующей на него: 
Для замкнутой системы тел выполняется закон сохранения импульса:
в замкнутой системе векторная сумма импульсов тел до взаимодействия равна векторной сумме импульсов тел после взаимодействия.
 , где
, где 

Закон сохранения импульса лежит в основе реактивного движения.
Реактивное движение – это такое движение тела, которое возникает после отделения от тела его части.
Для вычисления скорости ракеты записывают закон сохранения импульса
 и получают формулу скорости ракеты:
и получают формулу скорости ракеты:  =
=  , где М – масса ракеты,
, где М – масса ракеты, 

10.Опыты Резерфорда по рассеянию α-частиц. Ядерная модель атома. Квантовые постулаты Бора.
Первая модель атома была предложена английским физиком Томсоном. По Томсону, атом представляет собой положительно заряженный шар, внутри которого находятся отрицательно заряженные электроны.
|
|
|
Модель атома Томсона была неверной, что подтвердилось в опытах английского физика Резерфорда в 1906 г.
В этих опытах узкий пучок α-частиц, испускаемых радиоактивным веществом, направлялся на тонкую золотую фольгу. За фольгой помещался экран, способный светиться под ударами быстрых частиц.
Было обнаружено, что большинство α-частиц отклоняется от прямолинейного распространения после прохождения фольги, т.е. рассеиваются. А некоторые α-частицы вообще отбрасываются назад.
Рассеяние α-частиц Резерфорд объяснил тем, что положительный заряд не распределён равномерно по шару, как предполагал Томсон, а сосредоточен в центральной части атома – атомном ядре. При прохождении около ядра α-частица, имеющая положительный заряд, отталкивается от него, а при попадании в ядро – отбрасывается назад.
Резерфорд предположил, что атом устроен подобно планетарной системе.

Но Резерфорд не мог объяснить устойчивости (почему электроны не излучают волны и не падают к положительно заряженному ядру).
Новые представления об особых свойствах атома сформулировал датский физик Бор в двух постулатах.
1-й постулат. Атомная система может находиться только в особых стационарных или квантовых состояниях, каждому из которых соответствует соя энергия; в стационарном состоянии атом не излучает.
2-й постулат. При переходе атома из одного стационарного состояния в другое испускается или поглощается квант электромагнитного излучения.
Энергия излученного фотона равна разности энергий атома в двух состояниях:
 постоянная Планка.
постоянная Планка.
2) Внутренняя энергия идеального газа.
В теории идеального газа потенциальная энергия взаимодействия молекул считается равной нулю. Поэтому внутренняя энергия идеального газа определяется кинетической энергией движения всех его молекул. Средняя энергия движения одной молекулы равна

Так как в одном киломоле содержится  молекул, то внутренняя энергия одного киломоля газа будет
молекул, то внутренняя энергия одного киломоля газа будет

Учитывая, что  , получим
, получим

Для любой массы m газа, т.е. для любого числа киломолей  внутренняя энергия
внутренняя энергия

| (10.12) |
Из этого выражения следует, что внутренняя энергия является однозначной функцией состояния и, следовательно, при совершении системой любого процесса, в результате которого система возвращается в исходное состояние, полное изменение внутренней энергии равно нулю. Математически это записывается в виде тождества

БИЛЕТ-8
1) Вынужденные колебания, резонанс.
Вынужденные колебания
ОПРЕДЕЛЕНИЕ
Вынужденные колебания – это колебания, происходящие под действием внешней периодически действующей силы.
В отличие от свободных колебаний, когда система получает энергию лишь один раз (при выведении системы из состояния равновесия), в случае вынужденных колебаний система поглощает эту энергию от источника внешней периодической силы непрерывно. Эта энергия восполняет потери, расходуемые на преодоление трения, и потому полная энергия колебательной системы no-прежнему остается неизменной.
Вынужденные колебания в отличие от свободных могут происходить с любой частотой. Частота вынужденных колебанийсовпадает с частотой внешней силы, действующей на колебательную систему. Таким образом, частота вынужденных колебаний определяется не свойствами самой системы, а частотой внешнего воздействия.
Примерами вынужденных колебаний являются колебания детских качелей, колебания иглы в швейной машине, поршня в цилиндре автомобильного двигателя, рессор автомобиля, движущегося по неровной дороге и т.д.
Резонанс
ОПРЕДЕЛЕНИЕ
Резонанс – это явление резкого возрастания амплитуды вынужденных колебаний при приближении частоты вынуждающей силы к собственной частоте колебательной системы.
Резонанс возникает из-за того, что при внешняя сила, действуя в такт со свободными колебаниями, все время имеет одинаковое направление со скоростью колеблющегося тела и совершает положительную работу: энергия колеблющегося тела увеличивается, и амплитуда его колебаний становится большой. Если же внешняя сила действует «не в такт», то эта силы попеременно совершает то отрицательную, то положительную работу и вследствие этого энергия системы меняется незначительно.
На рис.1 показана зависимость амплитуды вынужденных колебаний от частоты вынуждающей силы. Видно, что эта амплитуда достигает максимума при определенном значении частоты, т.е. при , где собственная частота колебательной системы. Кривые 1 и 2 отличаются величиной силы трения. При малом трении (кривая 1) резонансная кривая имеет резкий максимум, при большей силе трения (кривая 2) такого резкого максимума нет.

Рис.1. Резонансные кривые для различных значений силы трения.
С явлением резонанса мы часто встречаемся в повседневной жизни. Если в комнате задрожали стекла при прохождении по улице тяжелого грузовика, это значит, что собственная частота колебаний стекол равна частоте колебаний машины. Если морские волны попадают в резонанс с периодом корабля, то качка становится особенно сильной.
Явление резонанса необходимо учитывать при проектировании мостов, зданий и других сооружений, испытывающих вибрацию под нагрузкой, в противном случае при определенных условиях эти сооружения могут быть разрушены. Однако резонанс также может быть полезен. Явление резонанса используется при настройке радиоприемника на определенную частоту радиовещания, а также во многих других случаях.
2) Средняя квадратичная скорость молекул. Молекулярно кинетическое толкование абсолютной температуры.
Число молекул в единице объема n можно заменить отношением полного числа всех молекул газа N, находящихся в сосуде, к его
объему V, т.е.  , и уравнение (7.3) переписать в виде
, и уравнение (7.3) переписать в виде
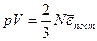 .
.
Из определения средней энергии поступательного движения молекул и средней квадратичной скорости следует, что
 ,
,
где  - суммарная кинетическая энергия поступательного движе-ния всех молекул газа, и уравнение (7.3) можно переписать в виде
- суммарная кинетическая энергия поступательного движе-ния всех молекул газа, и уравнение (7.3) можно переписать в виде
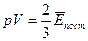 . (7.4)
. (7.4)
Следовательно, произведение объема газа на его давление численно равно 2/3 кинетической энергии хаотического поступательного движения всех молекул газа, заключенных в этом объеме. Это соотношение связывает макроскопические наблюдаемые и измеряемые величины р и V с основной характеристикой  микроскопических движений, происходящих внутри газа и обуславливающих наличие давления его на стенку. Из уравнения (7.4) следует, что
микроскопических движений, происходящих внутри газа и обуславливающих наличие давления его на стенку. Из уравнения (7.4) следует, что
 .
.
Поскольку в знаменателе стоит объем, занимаемый газом, то, очевидно, что вся дробь будет представлять кинетическую энергию молекул в единице объема, т.е. давление газа измеряется плотностью кинетической энергии движущихся молекул газа.
Подставляя произведение давления на объем из уравнения Менделеева-Клайперона

в выражение (7.4), получим
 . (7.5)
. (7.5)
Таким образом, энергия идеального газа прямо пропорциональна его абсолютной температуре. Под  мы понимаем полную энергию, так как рассматриваемый газ одноатомный и потенциальной энергией не обладает.
мы понимаем полную энергию, так как рассматриваемый газ одноатомный и потенциальной энергией не обладает.
Средняя кинетическая энергия поступательного движения одной молекулы равна полной энергии газа, деленной на число молекул.
Число молекул, содержащихся в  молей равно
молей равно
 , (7.6)
, (7.6)
где NA - число Авогадро.
Разделив (7.5) на (7.6), получим среднюю кинетическую энергию одной молекулы:
 .
.
Величины R и Na являются универсальными постоянными. Их отношение  также является универсальной постоянной и носит название постоянной Больцмана, равной k=1,38×10-23 Дж/к.
также является универсальной постоянной и носит название постоянной Больцмана, равной k=1,38×10-23 Дж/к.
Введя постоянную Больцмана, мы можем переписать выражение для средней кинетической энергии одной молекулы в виде
 . (7.7)
. (7.7)
Таким образом, средняя кинетическая энергия хаотического движения молекул идеального газа прямо пропорциональна его абсолютной температуре и является мерой интенсивности теплового движения молекул при заданной температуре. Это формула позволяет выявить молекулярно-кинетический смысл температуры.
Температура тела есть количественная мера энергии теплового движения молекул, из которых состоит тело. Из выражения (7.7) следует, что при одинаковой температуре средние кинетические энергии молекул всех газов одинаковы, несмотря на различие масс молекул разных газов. Подставляя в (7.7) (7.3), можно преобразовать основное уравнение кинетической энергии газов к виду
p = nkT. (7.8)
где р – давление газа, n – концентрация молекул, Т – абсолютная температура, k - постоянная Больцмана.
БИЛЕТ-9
1) Момент импульса вращающегося тела и системы тел. Закон сохранения момента импульса.
Дата добавления: 2018-04-04; просмотров: 747; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!

