Соль, образованная слабым основанием и сильной кислотой (гидролиз по катиону)


В растворе накапливаются ионы 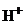 , в результате чего реакция смещается в кислую сторону, рН в растворах солей подобного типа меньше 7.
, в результате чего реакция смещается в кислую сторону, рН в растворах солей подобного типа меньше 7.
Соль, образованная сильным основанием и слабой кислотой (гидролиз по аниону).

В данном случае гидролиз ведет к увеличению концентраций ионов  в растворе, среда щелочная, рН>7.
в растворе, среда щелочная, рН>7.
Соль, образованная слабой кислотой и слабым основанием (гидролиз по катиону и по аниону).

В результате гидролиза ацетата аммония происходит образование двух слабых электролитов, раствор оказывается близким к нейтральному, рН~7.
4. Соль, образованная сильным основанием и сильной кислотой.
Соли подобного типа гидролизу не подвергаются. Их ионы не образуют с ионами 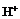 и
и  воды слабодиссоциируюших или труднорастворимых соединений, равновесие между ионами и молекулами воды не нарушается и раствор остается нейтральным, рН равен 7.
воды слабодиссоциируюших или труднорастворимых соединений, равновесие между ионами и молекулами воды не нарушается и раствор остается нейтральным, рН равен 7.
Особенности гидролиза солей, образованных слабыми многоосновными кислотами, а также солей, образованных слабыми многокислотными основаниями.
Гидролиз солей, образованных слабыми многоосновными кислотами, а также солей, образованных слабыми многоосновными основаниями, протекает ступенчато. В результате гидролиза по первой ступени образуются соответственно кислая или основная соль:

Накопление в растворах ионов  и
и 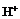 препятствует дальнейшему протеканию гидролиза, и по второй ступени гидролиз практически не протекает.
препятствует дальнейшему протеканию гидролиза, и по второй ступени гидролиз практически не протекает.
|
|
|
Вычисление pH растворов солей
В качестве примера возьмем гидролиз ацетата натрия:

Ионное уравнение:

Константа равновесия этой реакции
 ,
,
так как концентрация воды практически остается постоянной, ее можно объединить с константой равновесия:

где Кг - константа гидролиза.
Выразим  через ионное произведение воды [
через ионное произведение воды [  и
и
подставив эту величину в уравнение Кг получаем

где  - константа диссоциации слабой кислоты.
- константа диссоциации слабой кислоты.
В общем случае, если исходную концентрацию аниона слабой кислоты А  обозначить через С моль/л, то Ch моль/л – это концентрация той части аниона А
обозначить через С моль/л, то Ch моль/л – это концентрация той части аниона А  , которая подверглась гидролизу и образовала Ch моль/л слабой кислоты HA и Ch моль/л гидроксильных ионов:
, которая подверглась гидролизу и образовала Ch моль/л слабой кислоты HA и Ch моль/л гидроксильных ионов:




где: h – степень гидролиза, т.е доля молекул соли, подвергающихся гидролизу.
Константа гидролиза соли:

При малом значении h:  откуда
откуда  .
.
Так как 
 , то
, то 
Аналогично соотношение можно получить и при рассмотрении гидролиза соли слабого основания и сильной кислоты:

Принимая во внимание, что гидролиз солей, образованных сильными основаниями и многоосновными слабыми кислотами протекает преимущественно по 1-ой ступени:
|
|
|

Константа гидролиза определяется уравнением:

где  - константа диссоциации слабого основания по 2-ой ступени.
- константа диссоциации слабого основания по 2-ой ступени.
Пример 4. Определить pH 0.02Н раствора соды Na2C03, учитывая только первую ступень гидролиза.
Решение: Гидролиз соли протекает по уравнению

Для вычисления степени гидролиза необходимо вычислить молярную концентрацию раствора 

Дата добавления: 2018-02-28; просмотров: 560; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
