Витамины группы D (кальциферолы)
ВИТАМИНЫ.
12. Тиамин, строение, участие в образовании коферментов, биологическое значение, суточная потребность, распространение в природе, авитаминоз.
Источники
Черный хлеб, злаки, горох, фасоль, мясо, дрожжи.
Суточная потребность
2,0-3,0 мг.
Строение
В составе тиамина определяется пиримидиновое кольцо, соединенное с тиазоловым кольцом. Коферментной формой витамина является тиаминдифосфат.

| 
|
| Строение витамина В1 | Строение тиаминдифосфата |
Метаболизм
Всасывается в тонком кишечнике в виде свободного тиамина. Витамин фосфорилируется непосредственно в клетке-мишени. Примерно 50% всего В1 находится в мышцах, около 40% – в печени. Единовременно в организме содержится не более 30 суточных доз витамина.
Биохимические функции
1. Входит в состав тиаминдифосфата (ТДФ), который
· является коферментом транскетолазы- фермента пентозофосфатного пути.

Реакция пентозофосфатного пути с участием тиаминдифосфата
· входит в состав ферментов декарбоксилирования α-кетокислот пируватдегидрогеназы и α-кетоглутаратдегидрогеназы, которые участвуют в энергетическом обмене.
· входит в состав дегидрогеназы разветвленных α-кетокислот, необходимой для катаболизма лейцина, валина, изолейцина.
2. Входит в состав тиаминтрифосфата, который изучен еще недостаточно. Имеются разрозненные сведения об участии ТТФ в передаче нервного импульса, в генерации клеточного сигнала, в реакциях клеточного биоэлектрогенеза, в регуляции активности ион-ных каналов.
|
|
|
Гиповитаминоз
Причина
Основной причиной является недостаток витамина в пище, избыток алкоголь-содержащих напитков, которые снижают всасывание и повышают экскрецию витамина, или углеводныхпродуктов, повышающих потребность в тиамине.
Также причиной гиповитаминоза может быть потребление сырой рыбы (треска, форель, сельдь), сырых устриц, поскольку в них содержится фермент тиаминаза, разрушающий витамин. В кишечнике человека присутствует бактериальная тиаминаза.
Клиническая картина
Болезнь "бери-бери" или "ножные кандалы" – нарушение метаболизма пищеварительной, сердечно-сосудистой и нервной систем из-за недостаточного энергетического и пластического обмена.
Со стороны нервной ткани наблюдаются:
· полиневриты: снижение периферической чувствительности, утрата некоторых рефлексов, боли по ходу нервов,
· энцефалопатия: синдром Вернике – спутанность сознания, нарушение координации, галлюцинации, нарушение зрительной функции, синдром Корсакова – ретроградная амнезия, неспособность усваивать новую информацию, болтливость.
|
|
|
Со стороны сердечно-сосудистой системы отмечается нарушение сердечного ритма, боли в сердце и увеличение его размеров.
В желудочно-кишечном тракте нарушается секреторная и моторная функция, возникает атония кишечника и запоры, исчезает аппетит, уменьшается кислотность желудочного сока.
Антивитамины В1
В кишечнике имеется бактериальная тиаминаза, разрушающая тиамин. Также этот фермент активен в сырой рыбе, устрицах.
Пиритиамин, структурный аналог и антиметаболит тиамина, обнаружен в некоторых растениях (папоротник). Он конкурирует за переносчик тиамина на мембранах клеток: в кишечнике подавляет его всасывание, в тканях "вытесняет" витамин из клеток.
Лекарственные формы
13. Рибофлавин, строение, участие в образовании коферментов, биологическое значение, суточная потребность, распространение в природе.
1.Витамин B1 (тиамин). Структура витамина включает пиримидиновое и тиазоловое кольца, соединённые метановым мостиком.

· Источники.Витамин В1 - первый витамин, выделенный в кристаллическом виде К. Функом в 1912 г. Он широко распространён в продуктах растительного происхождения (оболочка семян хлебных злаков и риса, горох, фасоль, соя и др.). В организмах животных витамин В1, содержится преимущественно в виде дифосфорного эфира тиамина (ТДФ); он образуется в печени, почках, мозге, сердечной мышце путём фосфорилирования тиамина при участии тиаминкиназы иАТФ.
|
|
|
· Суточная потребностьвзрослого человека в среднем составляет 2-3 мг витамина В1. Но потребность в нём в очень большой степени зависит от состава и общей каяорийнос-ти пищи, интенсивности обмена веществ и интенсивности работы. Преобладание углеводов в пище повышает потребность организма в витамине; жиры, наоборот, резко уменьшают эту потребность.
· Биологическая рольвитамина В, определяется тем, что в виде ТДФ он входит в состав как минимум трёх ферментов и ферментных комплексов: в составе пируват- и ос-кетоглутаратдегидрогеназных комплексов он участвует в окислительном декарбоксилировании пирувата и ос-кетоглутарата; в составе транскетолазы ТДФ участвует в
125
пентозофосфатном пути превращения углеводов.
· Основной, наиболее характерный и специфический признак недостаточности витамина В1- полиневрит, в основе которого лежат дегенеративные изменения нервов. Вначале развивается болезненность вдоль нервных стволов, затем - потеря кожной чувствительности и наступает паралич (бери-бери). Второй важнейший признак заболевания - нарушение сердечной деятельности, что выражается в нарушении сердечного ритма, увеличении размеров сердца и в появлении болей в области сердца. К характерным признакам заболевания, связанного с недостаточностью витамина В1относят также нарушения секреторной и моторной функций ЖКТ; наблюдают снижение кислотности желудочного сока, потерю аппетита, атонию кишечника.
|
|
|
· Источники
· Достаточное количество содержат мясные продукты, печень, почки, молочные продукты, дрожжи. Также витамин образуется кишечными бактериями.
· Суточная потребность
· 2,0-2,5 мг.
· Строение
· В состав рибофлавина входит флавин – изоаллоксазиновое кольцо с заместителями (азотистое основание) и спирт рибитол.
· 
· Строение витамина В2
· Коферментные формы витамина дополнительно содержат либо только фосфорную кислоту –флавинмононуклеотид (ФМН), либо фосфорную кислоту, дополнительно связанную с АМФ –флавинадениндинуклеотид.
· 
· Строение окисленных форм ФАД и ФМН
· Метаболизм
· В кишечнике рибофлавин освобождается из состава пищевых ФМН и ФАД, и диффундирует в кровь. В слизистой кишечника и других тканях вновь образуется ФМН и ФАД.
· Биохимические функции
· Кофермент оксидоредуктаз – обеспечивает перенос 2 атомов водорода в окислительно-восстановительных реакциях.
· 
· Механизм участия флавинового кофермента а биохимической реакции
· Витамин содержат:
· 1. Дегидрогеназы энергетического обмена – пируватдегидрогеназа (окисление пировиноградной кислоты), α- кетоглутаратдегидрогеназа и сукцинатдегидрогеназа (цикл трикарбоновых кислот), ацил-КоА-дегидрогеназа (окисление жирных кислот), митохондриальная α-глицеролфосфатдегидрогеназа (челночная система).
· 
· Пример дегидрогеназной реакции с участием ФАД
· 2. Оксидазы, окисляющие субстраты с участием молекулярного кислорода, например прямое окислительное дезаминирование аминокислот или обезвреживание биогенных аминов.
· 
· Пример оксидазной реакции с участием ФАД
· Гиповитаминоз
· Причина
· Пищевая недостаточность, хранение пищевых продуктов на свету, фототерапия, алкоголизм и нарушения ЖКТ.
· Клиническая картина
· В первую очередь страдают высокоаэробные ткани – эпителий кожи и слизистых. Проявляется как сухостьротовой полости, губ и роговицы; хейлоз, т.е. трещины в уголках рта и на губах ("заеды"), глоссит(фуксиновый язык),шелушение кожи в районе носогубного треугольника, мошонки, ушей и шеи, конъюнктивити блефарит.
· Сухость конъюнктивы и ее воспаление ведут к компенсаторному увеличению кровотока в этой зоне и улучшению снабжения ее кислородом, что проявляется как васкуляризация роговицы.
· Антивитамины В2
· 1. Акрихин (атебрин) – ингибирует функцию рибофлавина у простейших. Используется при лечении малярии, кожного лейшманиоза, трихомониаза, гельминтозов (лямблиоз, тениидоз).
· 2. Мегафен – тормозит образование ФАД в нервной ткани, используется как седативное средство.
· 3. Токсофлавин – конкурентный ингибитор флавиновых дегидрогеназ.
Витамин В2 (рибофлавин). В основе структуры витамина В2 лежит структура изоаллоксазина, соединённого со спиртом рибитолом.

Рибофлавин представляет собой кристаллы жёлтого цвета (от лат. flavos - жёлтый), слабо растворимые в воде.
· Главные источникивитамина В2 - печень, почки, яйца, молоко, дрожжи. Витамин содержится также в шпинате, пшенице, ржи. Частично человек получает витамин В2 как продукт жизнедеятельности кишечной микрофлоры.
· Суточная потребностьв витамине В2 взрослого человека составляет 1,8-2,6 мг.
· Биологические функции.В слизистой оболочке кишечника после всасывания витамина происходит образование коферментов FMN и FAD по схеме:

· Коферменты FAD и FMN входят в состав флавиновых ферментов, принимающих участие в окислительно-восстановительных реакциях (см. разделы 2, 6, 9, 10).
· Клинические проявления недостаточностирибофлавина выражаются в остановке роста у молодых организмов. Часто развиваются воспалительные процессы на слизистой оболочке ротовой полости, появляются длительно незаживающие трещины в углах рта, дерматит носогубной складки. Типично воспаление глаз: конъюнктивиты, васкуляризация роговицы, катаракта. Кроме того, при авитаминозе В2 развиваются общая мышечная слабость и слабость сердечной мышцы.
3
· 14. Никотинамид, строение, участие в образовании коферментов, биологическое действие, суточная потребность, распространение в природе, авитаминоз.
. Витамин РР (никотиновая кислота, никотинамид, витамин B3)

· Источники.Витамин РР широко распространён в растительных продуктах, высоко его содержание в рисовых и пшеничных отрубях, дрожжах, много витамина в печени и почках крупного рогатого скота и свиней. Витамин РР может образовываться из триптофана (из 60 молекул триптофана может образоваться 1 молекула никотинамида), что снижает потребность в витамине РР при увеличении количества триптофана в пище.
· Суточная потребностьв этом витамине доставляет для взрослых 15-25 мг, для детей - 15 мг.
· Биологические функции.Никотиновая кислота в организме входит в состав NAD и NADP, выполняющих функции коферментов различных дегидрогеназ (см. раздел 2). Синтез NAD в организме протекает в 2 этапа:
126

· NADP образуется из NAD путём фосфорилирования под действием цитоплазматической NAD-киназы.
NAD+ + АТФ → NADP+ + АДФ
· Недостаточность витамина РРприводит к заболеванию "пеллагра", для которого характерны 3 основных признака: дерматит, диарея, деменция ("три Д"), Пеллагра проявляется в виде симметричного дерматита на участках кожи, доступных действию солнечных лучей, расстройств ЖКТ (диарея) и воспалительных поражений слизистых оболочек рта и языка. В далеко зашедших случаях пеллагры наблюдают расстройства ЦНС (деменция): потеря памяти, галлюцинации и бред.
·
·
азвание витамина PP дано от итальянского выражения preventive pellagra – предотвращающий пеллагру.
Источники
Хорошим источником являются печень, мясо, рыба, бобовые, гречка, черный хлеб, в молоке и яйцах витамина мало. Также синтезируется в организме из триптофана – одна из 60 молекул триптофана превращается в одну молекулу витамина.
Таким образом, можно считать, что 60 мг триптофана равноценны примерно 1 мг никотинамида. Если принять, что физиологическая норма потребления триптофана составляет 1 г, то в организме образуется около 17 мг никотинамида в сутки.
Суточная потребность
15-25 мг.
Строение
Витамин существует в виде никотиновой кислоты или никотинамида.

Две формы витамина РР
Его коферментными формами являются никотинамидадениндинуклеотид (НАД) и фосфорилированная по рибозе форма – никотинамидадениндинуклеотидфосфат (НАДФ).

Строение окисленных форм НАД и НАДФ
Биохимические функции
Перенос гидрид-ионов Н– (атом водорода и электрон) в окислительно-восстановительных реакциях

Механизм участия НАД и НАДФ в биохимической реакции
Благодаря переносу гидрид-иона витамин обеспечивает следующие задачи:
1. Метаболизм белков, жиров и углеводов. Так как НАД и НАДФ служат коферментами большинства дегидрогеназ, то они участвуют в реакциях
· при синтезе и окислении карбоновых кислот,
· при синтезе холестерола,
· обмена глутаминовой кислоты и других аминокислот,
· обмена углеводов: пентозофосфатный путь, гликолиз,
· окислительного декарбоксилирования пировиноградной кислоты,
· цикла трикарбоновых кислот.

Пример биохимической реакции с участием НАД-зависимой дегидрогеназы
2. НАДН выполняет регулирующуюфункцию, поскольку является ингибитором некоторых реакций окисления, например, в цикле трикарбоновых кислот.
3. Защита наследственной информации – НАД является субстратом поли-АДФ-рибозилирования в процессе сшивки хромосомных разрывов и репарации ДНК.
4. Защита от свободных радикалов – НАДФН является необходимым компонентом антиоксидантной системы клетки.
5. НАДФН участвует в реакциях ресинтеза тетрагидрофолиевой кислоты из дигидрофолиевой, например, после синтеза тимидилмонофосфата, восстановлении тиоредоксина при синтезе дезоксирибонуклеотидов.
Гиповитаминоз
Причина
Пищевая недостаточность ниацина и триптофана. Синдром Хартнупа.
Клиническая картина
Проявляется заболеванием пеллагра (итал.: pelle agra – шершавая кожа). Проявляется каксиндром трех Д:
· деменция(нервные и психические расстройства, слабоумие),
· дерматиты(фотодерматиты),
· диарея(слабость, расстройство пищеварения, потеря аппетита).
При отсутствии лечения заболевание кончается летально. У детей при гиповитаминозе наблюдается замедление роста, похудание, анемия.
В США в 1912-1216 гг. число заболевших пеллагрой составляло 100 тысяч человек в год, из них около 10 тысяч умирало. Причиной являлось отсутствие животных продуктов питания, в основном люди питались кукурузой и сорго, которые бедны триптофаном и содержат неусвояемый связанный ниацин.
Интересно, что у индейцев Южной Америки, у которых с древних времен основу питания составляет кукуруза, пеллагра не встречается. Причиной такого феномена является то, что они отваривают кукурузу в известковой воде, при этом ниацин высвобождается из нерастворимого комплекса. Европейцы, взяв у индейцев кукурузу, не потрудились также позаимствовать и рецепты.
Антивитамины
Производное изоникотиновой кислоты изониазид, используемый для лечения туберкулеза. По одной из гипотез, его механизм действия – замена никотиновой кислоты в реакциях синтеза никотинамидаденин-динуклеотида (изо-НАД вместо НАД) и невозможность протекания окислительно-восстановительных реакций.
· 15. Пиридоксин, строение, участие в образовании коферментов, биологическое значение, суточная потребность, распространение в природе, авитаминоз
· . Витамин В6(пиридоксин, пиридоксаль,
пиридоксамин)
· В основе структуры витамина В6 лежит пиридиновое кольцо. Известны 3 формы витамина В6, отличающиеся строением замещающей группы у атома углерода в п-положении к атому азота. Все они характеризуются одинаковой биологической активностью.
· 
· 127
· 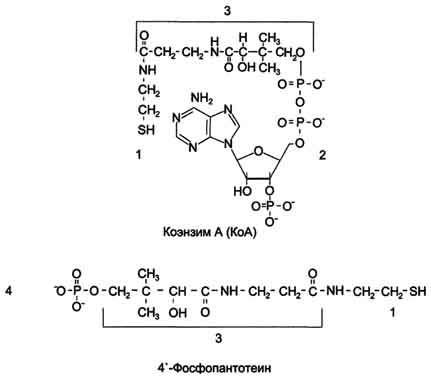
· Рис. 3-1. Строение КоА и 4'-фосфопантотеина. 1 - тиоэтаноламин; 2 - аденозил-3'-фосфо-5'-дифосфат; 3 - пантотеновая кислота; 4 - 4'-фосфопантотеин (фосфорилированная пантотеновая кислота, соединённая с тиоэтаноламином).
· Все 3 формы витамина - бесцветные кристаллы, хорошо растворимые в
·
· 16. Витамин Вс и В12, понятие о строении, участие в образовании коферментов. Биологическое значение, суточная потребность, распространение в природе,воде.
Сточники
Из пищевых продуктов витамин содержат только животные продукты: печень, рыба, почки, мясо. Также он синтезируется кишечной микрофлорой, однако не доказана возможность всасывания витамина в нижних отделах ЖКТ.
Суточная потребность
2,5-5,0 мкг.
Строение
Содержит 4 пиррольных кольца, ион кобальта (с валентностью от Co3+ до Co6+), группу CN–. В организме при синтезе коферментных форм цианидная группа CN– заменяется метильной или 5'-дезоксиаденозильной.
Метаболизм
Для всасывания в кишечнике необходим внутренний фактор Касла – гликопротеин, синтезируемый обкладочными клетками желудка.
В крови витамин транспортируется в виде гидроксикобаламина специфическими транспортными белками (α- и β-глобулинами).
Биохимические функции
Витамин В12 участвует в двух видах реакций – реакции изомеризациии метилирования.
1. Основойизомеризующего действия витамина В12 является возможность способствовать переносу атома водорода на атом углерода в обмен на какую-либо группу.

Общая схема реакции изомеризации
Это имеет значение в процессе окисления остатков жирных кислот с нечетным числом атомов углерода, на последних стадиях утилизации углеродного скелета валина, лейцина, изолейцина, треонина, метионина, боковой цепи холестерола в результате которых образуетсяметилмалонил-SКоА, который превращается в сукцинил-SКоА при участии витамина В12 и в дальнейшем утилизируется в цикле трикарбоновых кислот.

Участие витамина В12 в метаболизме метилмалонил-SКоА
Полученный в реакциях окисления указанных метаболитов остаток пропионил-SКоА карбоксилируется с образованием метилмалонил-SKoA при участии витамина Н (биотина).
Накопление метилмалоната является абсолютным диагностическим признаком дефицита витамина В12.
2. Участие в трансметилировании аминокислоты гомоцистеина при синтезе метионина. Метионин в дальнейшем активируется и используется для синтеза адреналина, креатина, холина, фосфатидилхолина и др.

Участие витамина В12 в реакции метилирования
и его взаимодействие с фолиевой кислотой
Данная реакция обеспечивает удержание свободной фолиевой кислоты в клетке. При нехватке витамина В12 метил-ТГФК накапливается в цитозоле, легко проникает через плазматические мембраны и выходит из клетки. Возникает внутриклеточная недостаточность фолиевой кислоты, хотя в крови ее может быть много.
Гиповитаминоз
Причина
Пищевая недостаточность – как правило, наблюдается у вегетарианцев. В то же время, если человек какое время жизни питался мясом, то запасы витамина в печени бывают настолько велики, что их хватает на несколько лет.
Однако чаще причиной гиповитаминоза В12 является не отсутствие витамина в пище, а плохое всасывание при заболеваниях желудка (атрофический и гипоацидный гастрит) в результате отсутствия внутреннего фактора Кастла и заболеваний кишечника.
Также иногда встречаются аутоиммунные нарушения, при которых образуются антитела против обкладочных клеток желудка и против внутреннего фактора Касла, что препятствует всасыванию витамина. При этом развивается анемия, называемая пернициозной.
Клиническая картина
1. Макроцитарнаяанемия, при которой количество эритроцитов снижено в 3-4 раза. Она возникает чаще у пожилых, но может быть и у детей. Непосредственной причиной анемии является потеря фолиевой кислоты клетками при недостаточности витамина В12 и, как следствие, замедление деления клеток из-за снижения синтеза инозинмонофосфата и, соответственно пуриновых нуклеотидов, и уменьшения синтеза тимидилмонофосфата, а значит и ДНК.
Нехватка витамина В12 без гематологических нарушений поразительно широко распространена, особенно среди пожилых.
2. Неврологическиенарушения:
· замедление окисления жирных кислот с нечетным числом атомов углерода и накопление токсичного метилмалоната вызывает жировую дистрофию нейронов и демиелинизациюнервных волокон. Это проявляется в онемении кистей, стоп, ухудшении памяти, нарушении походки, снижении кожной чувствительности, нарушении сухожильных рефлексов (ахиллов, коленный),
· нехватка метионина опосредует снижение активности реакций метилирования, в частности, уменьшается синтез нейромедиатора ацетилхолина.
Витамин Вс
Источники
Растительные продукты, дрожжи, мясо, печень, почки, желток яиц. Витамин активно синтезируется дружественной кишечной микрофлорой.
Суточная потребность
400 мкг.
Строение
Витамин представляет собой комплекс из трех составляющих – птеридина, парааминобензойной кислоты и глутаминовой кислоты. Остатков глутамата, соединенных через γ-карбоксильную группу, может быть разное количество.

Строение фолиевой кислоты
Биохимические функции
Коферментной формой витамина является тетрагидрофолиевая кислота (ТГФК, Н4ФК).

Строение тетрагидрофолиевой кислоты
Непосредственная функция тетрагидрофолиевой кислоты – перенос одноуглеродных фрагментов, которые присоединяются к атомам N5 или N10:
· формила– в составе N5-формил-ТГФК и N10-формил-ТГФК,
· метенила– в качестве N5,N10-метенил-ТГФК,
· метилена– в виде N5,N10-метилен-ТГФК,
· метила– в форме N5-метил-ТГФК,
· формимина – в составе N5-формимино-ТГФК.

Строение и взаимопревращение активных форм
тетрагидрофолиевой кислоты
Благодаря способности переносить одноуглеродные фрагменты, витамин:
· участвует в синтезе пуриновых оснований и тимидинмонофосфата, и, следовательно, в синтезе ДНК,
· участвует в обмене аминокислот – обратимое превращение глицина и серина,

Пример участия фолиевой кислоты в биохимической реакции
· N5-метил-ТГФК взаимодействует с витамином В12, являясь донором метильной группы при превращении гомоцистеина в метионин.
В клетке N5-метил-ТГФК образуется в необратимой реакции из N5,N10-метилен-ТГФК. При этом единственнымспособом получить свободную ТГФК для других клеточных нужд является реакция превращения гомоцистеина в метионин. При дефиците витамина В12 эта реакция нарушается и возникает внутриклеточный дефицит витамина B9, хотя и в клетке и в крови его (в виде метил-ТГФК) может быть много. Такое явление получило название "ловушка для фолата".
Гиповитаминоз
Причина
Пищевая недостаточность, кислые продукты, тепловая обработка пищи, прием лекарств (барбитураты, сульфаниламиды и антибиотики, некоторые цитостатики – аминоптерин, метотрексат), алкоголизм и беременность.
Клиническая картина
В первую очередь затрагиваются органы кроветворения: так как клетки не теряют способности расти, но в них происходит нарушение синтеза ДНК с остановкой деления, то это приводит к образованию мегалобластов (крупных клеток) и мегалобластической анемии. Лейкопения присутствует по той же причине.
Аналогично развивается поражение слизистых желудка и кишечного тракта (гастриты, энтериты), глоссит.
Отмечается замедление роста, конъюнктивит, ухудшение заживления ран, иммунодефициты, оживление хронических инфекций и субфебрилитет.
Лекарственные формы
Фолинат кальция.
Антивитамины
Антивитамином В9 является группа лекарственных антибактериальных соединенийсульфаниламидовструктурно схожих с компонентом фолиевой кислоты -парааминобензойной кислотой (ПАБК). В бактериальной клетке происходит конкуренция за активный центр фермента и нарушается использование ПАБК для синтеза фолиевой кислоты, что ведет к прекращению синтеза тимидилового нуклеотида, подавлению синтеза ДНК и размножения бактерии.

Сходство строения сульфаниламидов
и парааминобензойной кислоты, компонента витамина В9
Фолиевая кислота (витамин Вc, витамин B9)
Фолиевая кислота состоит из трёх структурных единиц: остатка птеридина (I), парааминобензойной (II) и глутаминовой (III) кислот.
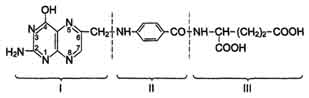
Витамин, полученный из разных источников, может содержать 3-6 остатков глутаминовой кислоты. Фолиевая кислота была вьщелена в 1941 г. из зелёных листьев растений, в связи с чем и получила своё название (от лат. folium - лист).
· Источники.Значительное количество этого витамина содержится в дрожжах, а также в печени, почках, мясе и других продуктах животного происхождения.
· Суточная потребностьв фолиевой кислоте колеблется от 50 до 200 мкг; однако вследствие плохой всасываемости этого витамина рекомендуемая суточная доза - 400 мкг.
· Биологическая рольфолиевой кислоты определяется тем, что она служит субстратом для синтеза коферментов, участвующих в реакциях переноса одноуглеродных радикалов различной степени окисленности: метальных, оксиметильных, формильных и других. Эти коферменты участвуют в синтезе различных веществ: пуриновых нуклеотидов, превращении с!УМФ в сПГМФ, в обмене глицина и серина (см. разделы 9, 10).
· Наиболее характерные признаки авитаминозафолиевой кислоты - нарушение кроветворения и связанные с этим различные формы малокровия (макроцитарная анемия), лейкопения и задержка роста. При гиповитаминозе фолиевой кислоты наблюдают нарушения регенерации эпителия, особенно в ЖКТ,
129
обусловленные недостатком пуринов и пиримидинов для синтеза ДНК в постоянно делящихся клетках слизистой оболочки. Авитаминоз фолиевой кислоты редко проявляется у человека и животных, так как этот витамин в достаточной степени синтезируется кишечной микрофлорой. Однако использование сульфаниламидных препаратов для лечения ряда заболеваний может вызвать развитие авитаминозов. Эти препараты - структурные аналоги парааминобензойной кислоты, ингибирующие синтез фолиевой кислоты у микроорганизмов (см. раздел 2). Некоторые производные птеридина (аминоптерин и метотрексат) тормозят рост почти всех организмов, нуждающихся в фолиевой кислоте. Эти препараты находят применение в лечебной практике для подавления опухолевого роста у онкологических больных.
17. Витамины С и Р, строение, физиологическое
природе, авитаминоз.
Источники
Свежие овощи и фрукты (по убыванию количества): шиповник, смородина, клюква, брусника, перец сладкий, укроп, капуста, земляника, клубника, апельсины, лимоны, малина.
При составлении рациона необходимо учитывать реальные условия. Например, несмотря на высочайшее содержание аскорбиновой кислоты в шиповнике (около 0,5 г на 100 г свежей ягоды), на практике он несущественный источник, т.к. мало кто ест шиповник как таковой, а при температурной обработке, длительном хранении и на свету большая часть витамина разрушается. Такая же ситуация с лимонами(0,4 г/100 г и 1 долька в кружке горячего чая), различнойзеленью, вареньем из различных ягод.
Суточная потребность
· младенцы 30-35 мг,
· дети от 1 до 10 лет - 35-50 мг
· подростки и взрослые - 50-100 мг.
Строение
Витамин является производным глюкозы. Его синтез осуществляют все организмы, кроме приматов и морских свинок.
Биохимические функции
Участие в окислительных процессах в качестве кофермента гидроксилаз.

Механизм участия аскорбиновой кислоты в биохимической реакции
1. Реакции гидроксилирования:
· пролина и лизина в их гидроксиформы при "созревании" коллагена,
· при синтезе гиалуроновой кислоты и хондроитинсульфата,
· при синтезе гормонов надпочечников (кортикостероидов и катехоламинов) и тиреоидныхгормонов,

Пример участия аскорбиновой кислоты в биохимической реакции
· при синтезе биогенного амина нейромедиатора серотонина,
· при синтезе карнитина (витаминоподобное вещество Вт), необходимого для окисления жирных кислот.
2. Восстановление иона железа Fe3+ в ион Fe2+ в кишечнике(улучшение всасывания) и вкрови(высвобождение из связи с трансферрином).
3. Участие в иммунных реакциях:
· повышает продукцию защитных белков нейтрофилов,
· высокие дозы витамина стимулируют бактерицидную активность и миграцию нейтрофилов.
Видимо, именно данная функция повышает потребность организма в аскорбиновой кислоте при простудных и инфекционных заболеваниях до 1,0-1,5 г.
4. Антиоксидантнаяроль:
· сбережение витамина Е,
· лимитирование свободнорадикальных реакций в делящихся тканях,
· ограничивает воспаление,
· снижает окисление липопротеинов в плазме крови и, таким образом, оказываетантиатерогенный эффект.
Показано, что прием аскорбиновой кислоты в дозе 300 мг/сут понижает возникновение сердечно-сосудистых заболеваний на 30%.
5. Активация фермента гексокиназы ("ловушки глюкозы"), обеспечивающего метаболизм глюкозы в клетке (реакция).
Гиповитаминоз
Причина
Пищевая недостаточность, тепловая обработка пищи (потери от 50 до 80%), длительное хранение продуктов (каждые 2-3 месяца количество витамина сокращается наполовину).
В весенне-зимний период дефицит витамина захватывает, в зависимости от региона, 25-75% населения России.
Клиническая картина
Так как особенно интенсивно аскорбиновая кислота накапливается в надпочечникахи тимусе, то ряд симптомов связана со сниженной функцией этих органов. Отмечается нарушение иммунитета, особенно легочного, развивается общая слабость, быстрая утомляемость, похудание, одышка, боли в сердце, отек нижних конечностей. У мужчин происходит слипание сперматозоидов и возникает бесплодие.
Снижается всасываемость железа в кишечнике, что вызывает снижение синтеза гема и гемоглобина и железодефицитную анемию. Уменьшается активность фолиевой кислоты – это приводит к мегалобластической анемии.
У детей дефицит аскорбиновой кислоты приводит к болезни Меллера-Барлоу, проявляющуюся в поражении костей: разрастание и минерализация хряща, торможение рассасывания хряща, корытовидное западение грудины, искривление длинных трубчатых костей ног, выступающие четкообразные концы ребер. Цинготные четки, в отличие от рахитических, болезненны.
Полное отсутствие витамина приводит к цинге – самому известному проявлению недостаточности аскорбиновой кислоты. При этом наблюдается нарушение синтеза коллагена, гиалуроновой кислоты и хондроитинсульфата, что приводит к поражению соединительной ткани, ломкости и проницаемости капилляров и к ухудшению заживления ран. Сопровождается дегенерацией одонтобластов и остеобластов, ухудшается состояние зубов.
Витамин р Название дано от лат. permeabilitas – проницаемость.
Источники
Растительные продукты – гречиха и другие злаки, бобовые, шиповник, чайный лист, цитрусовые, ягоды (клюква, брусника, черная смородина, ежевика, шиповник, виноград, черноплодная рябина, черешня, малина), яблоки, пряности, шоколад, белое и красное вино и т.д.
Суточная потребность
50-100 мг.
Строение
Витамин Р, строго говоря, является не витамином, а группой витаминоподобных веществ (до 600 представителей) разнообразного строения, содержащих в своей основе бензапироновое кольцо, соединенное с гидроксилированным фенолом, также имеются метильные группы, производные различных остатков сахаров (рамноза, глюкоза и др.).

Строение биофлавоноидов рутина и кверцетина
Биохимические функции
1. Антиоксидантная роль:
· реактивирование сульфгидрильныхгрупп белков и глутатиона,
· реактивирование витамина С и токоферола,
· снижение окисления липопротеинов очень низкой плотности(ЛПОНП).
2. Подавление активности гиалуронидазы– фермента, разрушающего межклеточный матрикс.
3. Является агонистом бенздиазепиновых рецепторов в структурах головного мозга, что обуславливает седативный, гипотензивный, обезболивающий эффекты.
Гиповитаминоз
Причина
Пищевая недостаточность в зимне-весенний период.
Клиническая картина
Ломкость и проницаемость капилляров, что проявляется кровоточивостью десен, мелкими кровоизлияниями в слизистых оболочках, коже, особенно в местах, подверженных нагрузке, проявления вазопатии с образованием петехий. Утомляемость, вялость, слабость, боли в плечах, в ногах при ходьбе.
Лекарственные формы
Название дано от лат. permeabilitas – проницаемость.Источники
Растительные продукты – гречиха и другие злаки, бобовые, шиповник, чайный лист, цитрусовые, ягоды (клюква, брусника, черная смородина, ежевика, шиповник, виноград, черноплодная рябина, черешня, малина), яблоки, пряности, шоколад, белое и красное вино и т.д.
Суточная потребность
50-100 мг.
Строение
Витамин Р, строго говоря, является не витамином, а группой витаминоподобных веществ (до 600 представителей) разнообразного строения, содержащих в своей основе бензапироновое кольцо, соединенное с гидроксилированным фенолом, также имеются метильные группы, производные различных остатков сахаров (рамноза, глюкоза и др.).

Строение биофлавоноидов рутина и кверцетина
Биохимические функции
1. Антиоксидантная роль:
· реактивирование сульфгидрильныхгрупп белков и глутатиона,
· реактивирование витамина С и токоферола,
· снижение окисления липопротеинов очень низкой плотности(ЛПОНП).
2. Подавление активности гиалуронидазы– фермента, разрушающего межклеточный матрикс.
3. Является агонистом бенздиазепиновых рецепторов в структурах головного мозга, что обуславливает седативный, гипотензивный, обезболивающий эффекты.
Гиповитаминоз
Причина
Пищевая недостаточность в зимне-весенний период.
Клиническая картина
Ломкость и проницаемость капилляров, что проявляется кровоточивостью десен, мелкими кровоизлияниями в слизистых оболочках, коже, особенно в местах, подверженных нагрузке, проявления вазопатии с образованием петехий. Утомляемость, вялость, слабость, боли в плечах, в ногах при ходьбе.
Лекарственные формы
18. Ретинол, понятие о строении, физиологическое (действие) значение, авитаминоз, суточная потребность, распространение в природе.
Источники.Витамин А содержится только в животных продуктах: печени крупного рогатого скота и свиней, яичном желтке, молочных продуктах; особенно богат этим витамином рыбий жир. В растительных продуктах (морковь, томаты, перец, салат и др.) содержатся каротиноиды, являющиеся провитаминами А. В слизистой оболочке кишечника и клетках печени содержится специфический фермент каротиндиоксигеназа, превращающий
Суточная потребностьвитамина А взрослого человека составляет от 1 до 2,5 мг витамина или от 2 до 5 мг р-каротинов. Обычно активность витамина А в пищевых продуктах выражается в международных единицах; одна международная единица (ME) витамина А эквивалентна 0,6 мкг β-каротина и 0,3 мкг витамина А.
· Биологические функции витаминаА. В организме ретинол превращается в ретиналь и ретиноевую кислоту, участвующие в регуляции ряда функций (в росте и дифференцировке клеток); они также составляют фотохимическую основу акта зрения.
· Наиболее детально изучено участие витамина А в зрительном акте (рис. 3-3). Светочувствительный аппарат глаза - сетчатка. Падающий на сетчатку свет адсорбируется и трансформируется пигментами сетчатки в другую форму энергии. У человека сетчатка содержит 2 типа рецепторных клеток: палочки и колбочки. Первые реагируют на слабое (сумеречное) освещение, а колбочки - на хорошее освещение (дневное зрение). Палочки содержат зрительный пигмент родопсин, а колбочки - йодопсин. Оба пигмента - сложные белки, отличающиеся своей белковой частью. В качестве кофермента оба белка содержат 11-цисретиналь, альдегидное производное витамина А.
· Ретиноевая кислота, подобно стероидным гормонам, взаимодействует с рецепторами в ядре клеток-мишеней. Образовавшийся комплекс связывается с определёнными участками ДНК и стимулирует транскрипцию генов (см. раздел 4). Белки, образующиеся в результате стимуляции генов под влиянием ретиноевой кислоты, влияют на рост, дифференцировку, репродукцию и эмбриональное развитие (рис. 3-4).
· Основные клинические проявления гиповитаминозаА. Наиболее ранний и характерный признак недостаточности витамина А у людей и экспериментальных животных - нарушение сумеречного зрения (гемералопия, или "куриная" слепота). Специфично для авитаминоза А поражение глазного яблока - ксерофтальмия, т.е. развитие сухости роговой оболочки глаза как следствие закупорки слёзного канала в связи с ороговением эпителия. Это, в свою очередь, приводит к развитию конъюнктивита, отёку, изъязвлению и размягчению роговой оболочки, т.е. к кера-томаляции. Ксерофтальмия и кератомаляция при отсутствии соответствующего лечения могут привести к полной потере зрения.
134

Рис. 3-3. Схема зрительного цикла. 1 - цис-ретиналь в темноте соединяется с белком опсином, образуя родопсин; 2 - под действием кванта света происходит фотоизомеризация 11-цисретинапя в транс-ретиналь; 3 - транс-ретиналь-опсин распадается на транс-ретиналь и опсин; 4 - поскольку пигменты встроены в мембраны светочувствительных клеток сетчатки, это приводит к местной деполяризации мембраны и возникновению нервного импульса, распространяющегося по нервному волокну; 5 - заключительный этап этого процесса - регенерация исходного пигмента. Это происходит при участии ретинальизомеразы через стадии: транс-ретиналь → транс-ретинол → цис-ретинол → цисретиналь; последний вновь соединяется с опсином, образуя родопсин.

Рис. 3-4. Действие ретиноидов в организме. Вещества (названия в рамках) - компоненты пищи.
135
· У детей и молодых животных при авитаминозе А наблюдают остановку роста костей, кератоз эпителиальных клеток всех органов и, как следствие этого, избыточное ороговение кожи, поражение эпителия ЖКТ, мочеполовой системы и дыхательного аппарата. Прекращение роста костей черепа приводит к повреждению тканей ЦНС, а также к повышению давления спинномозговой жидкости.
19. Кальциферолы, строение, особенно-активные формы витаминов биологическое значение, суточная потребность, распространение в природе, авитаминоз.
·
Витамины группы D (кальциферолы)
Кальциферолы - группа химически родственных соединений, относящихся к производным стеринов. Наиболее биологически активные витамины - D2 и D3. Витамин D2 (эргокалыщферол), производное эргостерина - растительного стероида, встречающегося в некоторых грибах, дрожжах и растительных маслах. При облучении пищевых продуктов УФО из эргостерина получается витамин D2, используемый в лечебных целях. Витамин D3, имеющийся у человека и животных, - холекальциферол, образующийся в коже человека из 7-дегидрохолестерина под действием УФ-лучей (рис. 3-5).
Витамины D2 и D3 - белые кристаллы, жирные на ощупь, нерастворимые в воде, но хорошо

Рис. 3-5. Схема синтеза витаминов D2 и D3. Провитамины D2 и D3 - стерины, у которых в кольце В две двойные связи. При воздействии света в процессе фотохимической реакции происходит расщепление кольца В. А - 7-дегидрохолестерин, провитамин D3, (синтезируется из холестерина); Б - эргостерин - провитамин D2.
136
растворимые в жирах и органических растворителях.
· Источники.Наибольшее количество витамина D3 содержится в продуктах животного происхождения: сливочном масле, желтке яиц, рыбьем жире.
· Суточная потребностьдля детей 12-25 мкг (500-1000 ME), для взрослого человека потребность значительно меньше.
· Биологическая роль.В организме человека витамин D3 гидроксилируется в положениях 25 и 1 и превращается в биологически активное соединение 1,25-дигидроксихолекальциферол (калыщтриол). Калыщтриол выполняет гормональную функцию, участвуя в регуляции обмена Са2+ и фосфатов, стимулируя всасывание Са2+ в кишечнике и кальцификацию костной ткани, реабсорбцию Са2+и фосфатов в почках. При низкой концентрации Са2+ или высокой концентрации D3 он стимулирует мобилизацию Са2+ из костей (см. раздел 11).
· Недостаточность.При недостатке витамина D у детей развивается заболевание "рахит", характеризуемое нарушением кальцификации растущих костей. При этом наблюдают деформацию скелета с характерными изменениями костей (Х- или о-образная форма ног, "чётки" на рёбрах, деформация костей черепа, задержка прорезывания зубов).
· Избыток.Поступление в организм избыточного количества витамина D3 может вызвать гипервитаминоз D. Это состояние характеризуется избыточным отложением солей кальция в тканях лёгких, почек, сердца, стенках сосудов, а также остеопорозом с частыми переломами костей.
20. Витамин К и Е, понятие о строении, биологическое значение, распространение в природе, суточная потребность, авитаминоз
Дата добавления: 2018-02-18; просмотров: 1743; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
