Розділ 2. Молекулярна фізика і термодинаміка.
Основні формули.
1. Рівняння стану ідеального газу:
 (для одного моля газу)
(для одного моля газу)
 (для довільної маси газу),
(для довільної маси газу),
де P– тиск, V- об’єм, Т – термодинамічна температура, m– маса, М – молярна маса, R– універсальна газова стала.
2. Закон Дальтона для тиску суміші газів:
 ,
,
де Pi– парціальний тиск і-ої компоненти газу.
3. Молярна маса суміші газів:
 ,
,
де m– маса і-ої компоненти, n - кількість молів і-ої компоненти.
4. Концентрація молекул однорідної системи:
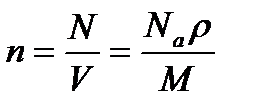 ,
,
де V – об’єм системи, r- густина речовини, N– число структурних елементів системи (молекул, атомів), Na– число Авогадро.
5. Основне рівняння молекулярно-кінетичної теорії газів:
 ,
,
або:
 ,
,
де vсер. – середня квадратична швидкістьмолекул, m0– маса одної молекули, N– число молекул в об’ємі газу V, n– концентрація молекул.
6. Швидкість молекул:
- найбільш ймовірна: 
 ;
;
- середня квадратична: 
 ;
;
середня арифметична: 
 .
.
7.Середня кінетична енергія поступального руху молекули ідеального газу:
 .
.
8.Середня кінетична енергія однієї молекули:
 ,
,
де і – число степенів свободи молекули.
9. Перший закон термодинаміки:
 ,
,
де dQ– кількість теплоти, отриманої тілом, dU– зміна внутрішньої енергії, dA – робота, виконана тілом.
Молярна теплоємність:
 ,
,
де n - кількість молей (кількість речовини).
10. Молярна теплоємність газів, що складаються із n компонентів:
 .
.
11. Питома теплоємність:
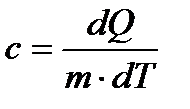
12. Внутрішня енергія ідеального газу:
|
|
|
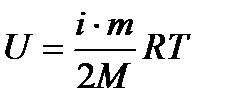
Приклади розв’язування задач.
Задача 2.1. Газ міститься в балоні ємністю V =75 л при температурі T=320 К і тиску P=2×10  Па. Знайти кількість молекул N в балоні, а також їх концентрацію n.
Па. Знайти кількість молекул N в балоні, а також їх концентрацію n.
V=75 л,
T=320 К,
P=2×10  Па
Па
N-?, n-?
Розв’язок.
Концентрація молекул n:
 =
=  .
.
Загальна кількість молекул:
 =3,4×10
=3,4×10 
Відповідь. N=4,5×1025 м-3, N=3,4×1024.
Задача 2.2В балоні місткістю V=10 л знаходиться гелій під тиском P1=1 Мпа при температурі T1=300 К. Після того, як із балону було взято Dm=10 г гелію, температура газу стaла дорівнювати T2=290 К. Визначити тиск газу P2, що залишився в балоні.
Дано:
V=10 л
P1=1 Мпа
T1=300 К
Dm=10 г
T2=290 К
P2-?
Розв’язок.
Запишемо рівняння Менделєєва-Клапейрона для початкового і кінцевого станів газу:
 ,
,  .
.
З цих рівнянь, враховуючи, що  , знаходимо:
, знаходимо:
 ,
,
звідки:
 .
.
Масу знайдемо із рівняння для початкового стану:
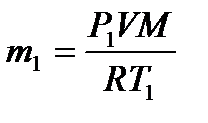 .
.
Після перетворень одержуємо:
 =3,64×105 Па.
=3,64×105 Па.
Відповідь. Р2=3,64×105 Па.
Задача 2. 3. Знайти середню арифметичну швидкість молекул газуvар., якщо відомо, що середня квадратична швидкість дорівнює vкв.=100 км/с.
Дано:
vкв.=100 км/с
vар.-?
Розв’язок.
Середня квадратична vкв. і середня арифметична швидкості vар.Визначаються за наступними співвідношеннями:
|
|
|
 ,
,
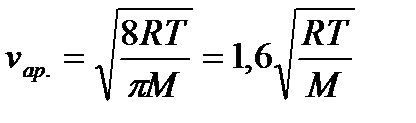 .
.
Розділивши один цих виразів на інший, одержимо:

звідки
 =925 м/с.
=925 м/с.
Відповідь.Vар.=925 м/с.
Задача 2. 4.Знайти концентрацію водню n в балоні, якщо він знаходиться під тиском Р=2,7×105 Па, а середня квадратична швидкість дорівнює vкв.=2400 м/с.
Дано:
Р=2,7×105 Па
vкв =2400 м/с
n-?
Розв’язок.
Концентрація молекул пов’язана із тиском формулою:
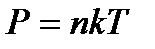 ,
,
звідки:
 .
.
Невідому температуру знайдемо із виразу для середньої квадратичної швидкості:
 ,
,  .
.
Підставивши цей вираз для температури у формулу для концентрації, одержуємо:
 =4,2×1025 м-3.
=4,2×1025 м-3.
Відповідь. N=4,2×1025 м-3.
Задача 2. 6.В балоні міститься m=140 г азоту при температурі T1=300 К під тиском P1=105 Па. Після ізохорного нагрівання тиск збільшився в n=5 разів. Знайти об’єм балона V, кінцеву температуру Т1 та кількість тепла DQ, що одержав газ.
Дано:
M=140 г
T1=300 К
P1=105 Па
n=5
V - ?, Т1 - ?, DQ-?
Розв’язок.
Об’єм балона визначимо із рівняння Менделєєва-Клапейрона для початкового стану газу:
 ,
,  =1,24×10-2 м3.
=1,24×10-2 м3.
Кінцеву температуру визначимо із рівняння ізохорного процесу:
 ,
,
звідки:
 =1500 К.
=1500 К.
Тепло, що поглинув газ в ізохорному процесі:
 =1,24×104 Дж.
=1,24×104 Дж.
Відповідь. V=1,24×10-2 м3, T2=1500 К, DQ=1,24×104 Дж.
Задача 2.7. Визначити температуру нагрівача T1, якщо ідеальна теплова машина, що працює за циклом Карно, віддає холодильнику N=75% теплоти, що одержує від нагрівача. Температура холодильника T2=300К.
|
|
|
Дано:
Q2=0,75Q1
T2=300K
T1– ?
Розв’язок.
Коефіцієнт корисної дії (ККД) теплової машини дорівнює:
h=  ;
;
Для ідеального циклу Карно ККД становить:
 .
.
Прирівняємо обидва значення ККД:
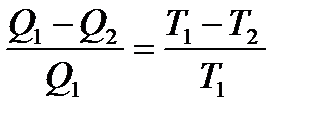 , або
, або  .
.
 ; T1=
; T1= 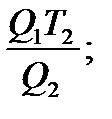 T1=
T1=  .
.
Відповідь: T1=400K.
Задача 2.8.Коефіцієнт дифузії і в’язкості кисню за деяких умов дорівнюють D=1,22×10-5 м/с і  . Знайти густину кисню r, середню довжину вільного пробігу l і середню арифметичну швидкість vсер. Його молекул.\
. Знайти густину кисню r, середню довжину вільного пробігу l і середню арифметичну швидкість vсер. Його молекул.\
Дано:
D=1,22×10-5 м/с

_________________________________________________________________
r - ?, l - ?, vсер.- ?
Розв’язок.
Скористаємось формулами, які визначають коефіцієнт дифузії і динамічну в’язкість:


де ?, vсер– середня арифметична швидкість; l- середня довжина вільного пробігу.
Звідси густина газу:
 .
.
Середня довжина вільного пробігу

де d– діаметр молекул кисню, n – кількість молекул в одиниці об’єму.
Оскільки:

де Р– тиск газу, k– стала Больцмана, Т- температура кисню, то:
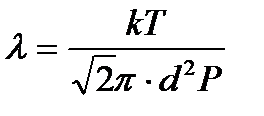 .
.
Густина газу, згідно з рівнянням Менделєєва- Клапейрона:
 =1,6 кг/м3.
=1,6 кг/м3.
Звідси:

В результаті:
 =84 нм.
=84 нм.
Середню арифметичну швидкість знайдемо з виразу для коефіцієнта дифузії з врахуванням виразу для середньої довжини вільного пробігу:
|
|
|
 =437,7 м/с.
=437,7 м/с.
Відповідь. r=1,6 кг/м3, l=84 нм, vсер.=437,7 м/с.
Задача 2.9. Нагрівник теплової машини, що працює за циклом Карно, має температуру Т1=473 К. Яка температура холодильника Т2, якщо за рахунок кожного кілоджоуля тепла, отримуваного від нагрівника, машина виконує роботу А=0,4 кДж?
Дано:
Т1=473 К
А=0,4 кДж
_____________________________________________________________
Т2 - ?
Розв’язок.
Температуру холодильника можна знайти, використавши вираз для К.К.Д. машини, яка працює за циклом Карно:
 ,
,
де Т  - абсолютна температура нагрівника, Т
- абсолютна температура нагрівника, Т  - абсолютна температура холодильника.
- абсолютна температура холодильника.
Звідси:

К.К.Д. машини:
 ,
,
де А – корисна робота, виконана машиною; Q– тепло, яке підводиться до машини за той же час.
Тоді:
Т2=283,8 К.
Відповідь. Т2=283,8 К.
Задача2.10. Балон, що містить V1=0,02м3повітря під тиском р1=4·105 Па, сполучають з балоном місткістю V2=0,06 м3, з якого викачане повітря. Знайти тиск р, який установився в посудинах. Температура стала.
Розв’язання:

Відповідь: р=105 Па.
Задача 2.11 Скільки ртуті увійде в скляний балончик об’ємом 5 см3, нагрітий до t1=4000C, при його охолодженні до t2=160C,якщо густина ртуті при t=160Cдорівнює ?=13,6 г/см3?
Розв’язання:

Використаємо закон Гей-Люссака:

Складемо пропорцію:

Знайдемо, що 
Тоді маса ртуті, яка ввійде в балончик, буде:
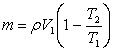
Підставивши числові значення, знайдемо:

Відповідь: т=0,4 г.
Задача 2.12 В балоні об’ємом V=10 лзнаходиться гелій під тиском р1=1 Мпапри температурі Т1=300 К.Після того, як з балона вийшло т=10 ггелію, температура в ньому зменшилась до Т2=290 К. Визначити тиск гелію, який залишився в балоні.
Розв’язання:
 де т1 і т2 – маси гелію в початковому і кінцевому стані.
де т1 і т2 – маси гелію в початковому і кінцевому стані.
З цих двох рівнянь виразимо маси: 
Визначимо їх різницю:

Тоді тиск гелію в балоні буде визначатись за формулою:

Підставимо числові значення:

Відповідь: р2=364 кПа.
Дата добавления: 2018-02-18; просмотров: 3544; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
