Natrii citras pro injectionibus

Получение
Лимонную кислоту получают из листьев хлопчатника, а затем нейтрализуют Na2CO3 до ph[7,8 - 8,0]
Свойства Бесцветные кристаллы или белый кристаллический порошок без запаха, солоноватого вкуса, выветривается на воздухе. Легко растворим в воде, практически нерастворим в спирте. Реакция водного раствора слабощелочная.
Подлинность
1. На Na+ см. выше.
2. На цитрат.
К раствору прибавляют CaCI2. Раствор остается прозрачным. При нагревании образуется белый кристаллический осадок.

Испытание на чистоту
- раствор препарата д.б. бесцветным и прозрачным
- не д.б. превышен предел щелочности
- хлоридов, сульфатов, тяжелых металлов и железа не более эталона.
Количественное определение
1.По ГФ. Метод ионообменной хроматографии.
Точную навеску препарата растворяют в воде и пропускают через колонку с катионитом в Н-форме. жидкости дают стекать со скоростью 20-25 капель в минуту.Выделевшуюся лимонную кислоту оттитровывают раствором щелочи до розовой окраски. Индикатор- ф/ф


2.Метод нейтрализации ВАК.
Ацидиметрия (в присутствии эфира) он необходим для извлечения выделяющейся лимонной кислоты, которая может влиять на окраску индикатора.
Точную навеску препарата помещают в колбу для титрования, прибавляют эфир, индикатор м/ор и титруют HCI до перехода желтой окраски в оранжево-розовую.

Применение. Для консервации крови в виде4-5% растворов
Хранение. В хорошо укупоренной таре.
|
|
|
Natrii hydrocitras pro injectionibus

Свойства.Бесцветные кристаллы или белый кристаллический порошок кисловатого вкуса. Легко растворим в воде, нерастворим в спирте. Реакция водного раствора слабокислая.
1. На Na+ - см. выше..
2. На цитрат.
К раствору прибавляют CaCI2. Раствор остается прозрачным. При нагревании образуется белый кристалический осадок.

Отличить цитрат от гидроцитрата можно по реакции среды водного раствора (см. свойства)
Количественное определение
Метод алкалиметрии.
Точную навеску препарата растворяют в воде, помещают в колбу и титруют раствором щелочи до розовой окраски. Индикатор ф/ф
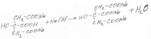
Применение. В качестве консерванта крови.
Хранение.В хорошо укупоренной таре.
Acidi glutaminicum
О О
// //
C-CH2-CH2-CH-C
/ / /
НО NH2 ОН
альфа- аминоглютаровая кислота.
Это соединение облодающее амфотерными свойствами: за счет карбоксильной группы может проявлять кислотные свойства и растворяться в щелочах, за счет аминогруппы проявляет основные свойства и может взаимодействовать с кислотами.
|
|
|
Получение.
Входят в состав жиров животного и растительного происхождения. В настоящее время получают синтетически.
Подлинность.
1.Общая реакция на аминокислоты

К раствору препарата прибaвляют нингидрин и нагревают, появляется сине-фиолетовое окрашивание.
Количественное определение
Метод Къельедаля (этот метод подходит для органических соединений имеющих в своем составе азот)
Т. Н. П. обрабатывают концент.H2SO4. При этом происходит минерализация органических соединений.
2NH3 + H2SO4 = (NH4)2 SO4
Полученный раствор обрабатывают избытком раствора щелочи.
(NH4)2 SO4 +2NaOH = 2NH3 + Na2SO4
Выделившийся аммиак улавливают специальном способом и затем титруют HCI по индикатору-м/ор
NH4OH + HCI = NH4CI + H2O
2.Метод нейтрализации в водной среде ( для глютаминовой кислоты этот метод возможен, т.к. у неё преобладают кислотные свойства)
Точную навеску препарата растворяют в горячей воде, охлаждают ,прибавляют индикатор бромтимоловый синий и титруют раствором щелочи до синей окраски раствора
Формула к-ты+NaOH NaOOC-CH2-CH2-CHNH2-CООН+H2O
Применение.
Увеличивает мозговое кровообращени, усиливает антитоксическое действие печени.
Хранение.В хорошо укупоренной таре, предохраняющей от действия света, в сухом прохладном, защищенном от света месте.
|
|
|
Acidum aminocapronicum
О
//
H2N-CH2-CH2-CH2-CH2-CH2-C
\
ОН
Е- аминокапроновая кислота
АФИБРИН- синоним
Это соединение обладающее амфотерными свойствами: за счет карбоксильной группы могут проявляться кислотные свойства и может растворяться в щелочах,за счет аминогруппы проявляет основные свойства.
Получение.
Входят в состав жиров животного и растительного происхождения. В настоящее время получают синтетически.
Свойства.
Белый кристалический порошок со слабым специфическим запахом, гигроскопичен.легко растворим в воде, трудно в спирте.Может растворяться в кислотах ищелочах.
Подлинность.
1.Общая реакция на аминокислоты

К раствору препарата прибавляют нингидрин и нагревают, появляется сине-фиолетовое окрашивание.
Количественное определение
Метод Къельедаля (этот метод подходит для органических соединений, имеющих в своем составе азот)
Точную навеску препарата обрабатывают концентратом H2SO4. При этом происходит минерализация органических соединений.
|
|
|
2NH3 + H2SO4 = (NH4)2 SO4
Полученый раствор обрабатывают избыточным количеством раствора щелочи.
(NH4)2 SO4 +2NaOH = 2NH3 + Na2SO4 + 2H2O
Выделившийся аммиак улавливают специальнsм способом и затем титруют HCI по индикатору-м/ор
NH4OH + HCI = NH4CI + H2O
метод по ГФ.
Метод кислотно-основного титрования в неводных средах.
Точную навеску препарата растворяют в ледяной CH3COOH и титруют раствором HCIO4 (растворена в ледяной CH3COOH) до зелено-голубой окраски. Индикатор- кристаллический фиолетовый)
H2N–(CH2)5 –COOH + HCIO4=[H3N+-(CH2)5-COOH]CIO4-
Применение
Проявляет гемостатическое (кровоостановливающее) действие. В организме окисляется до ГАМК. Назначают в виде гранул до 10-15 г в сутки или 5% раствора для инъекций.
Хранение
Список Б. В плотно укупоренной таре, предохраняющей от действия света, в сухом, прохладном, защищенном от света месте
АМИНОСПИРТЫ
Adrenalini hydrotartras

L-1-(3,4-дигидроксифенил)-2- метиламиноэтанола гидротартрат.
Свойства.Белый или беляй с сероватым оттенком кристаллический порошок без запаха. Легко изменяется под действием света и кислорода воздуха. Легко растворим в воде, мало растворим в спирте, практически нерастворим в эфире и хлороформе.
Подлинность
1. Реакция получения адренохрома.
К раствору препарата добавляют гидротартратный буфер ( для создания ph = 3,56 , т.е сильнокисл ) далее добавляют йод раствор и оставляют на несколько минут процесс окисления. К раствору добавляют Na2S2O3 для обесвечивания йода , раствор остается красно-бурого цвета ! Если провести аналогичную реакцию при ph= 6,5 эффект будет аналогичный (адреналин дает эффект в обоих случаях)
 адренохром
адренохром
2. с раствором FeCI3
При прибавления к раствору препарата раствора FeCI3 появляется изумрудно- зеленое окрашивание, которое от прибавления 1 капли раствора аммиака переходит в вишнево-красное окрашивание, а затем в оранжево-красное.
3.На кислотную часть.
К раствору препарата добавляют спирт и кристаллик HCI , при потирании стеклянной палочкой белый осадок.
H2C4H4O6 + KCl = KHC4H4O6(белый кристаллический)+HCl
Количественное определение
По ГФ. Кислотно-основное титрование в неводных средах.
Точную навеску препарата растворяют в ледяной CH3COOH , добавляют индикатор кристаллический фиолетовый и титруют раствором HCIO4 до зеленой окраски, т.к соль не образована галогеноводородной кислотой, то не добавляют ацетат окисной ртути 
Применение Симпатомиметическое средство (сосудосуживающее, бронхорасширяющее)
Хранение.сп.Б В герметически укупоренных банках оранжевого стекла или в запаянных ампулах, в защищенном от света месте.
Ephedrini hydrochloridum

L-1 фенил-2 метиламино пропанола-1 гидрохлорид
Получение. Природный алкалоид получают с помощью биосинтеза, который основан на сбраживании патоки из сахара дрожжами в присутствии бензальдегида. Затем левовращающий фенилацетилкарбинол подвергают восстановительному метиламинированию и полученное основание переводят в гидрохлорид.
В последнее время разрешен также дэфедрин, получаемый из побегов эфедры хвощевой.
Свойства. Белый кристаллический порошок без запаха ( дэфедрин – со слабым специфическим запахом).Легко растворим в воде, растворим ы спирте, практически нерастворим в эфире.
Подлинность
1 Образование медного производного
К раствору препарата прибавить раствор щёлочи и раствор гидрооксида меди, образуется раствор интенсивно-синего цвета, затем добавляют эфир и встряхивают. Водный слой становится синим, эфирный-розовый.

2 Реакция окисления и получения бензальдегида.
К раствору препарата прибавляют Fe3{Fe(CN)6} и нагревают. Ощущается запах бензальдегида.

3. На кислотную часть с AgNО3



Количественное определение
По ГФ.Метод кислотно-основного титрования в неводных средах.
ТНП растворяют в ледяной уксусной кислоте добавляют индикатор кристаллический фиолетовый и титруют раствором HClO4, до зелёной окраски. Необходимо добавить ацетат окисной ртути.

(CH3COO)2Hg+2HCl→2CH3COOH+HgCl2
ВАК
1 Метод нейтрализации в спирто-хлороформенной среде. Индикатор фенолфталеин.
эфедр.*HCl+NaOH→ эфедр.+NaOH+H2O
2 Метод аргентометрии по Фаянсу.( аргентометрия по Мору невозможна из-за кислой реакции среды в растворе)
ТНП растворяют в воде добавляют индикатор бромфеноловый синий и уксусную кислоту до жёлто-зелёной окраски и титруют раствором AgNО3 до синей окраски раствора.
эфедр.*HCl+AgNO3 →AgCl+ эфедр.*HNO3
4-3 Метод меркуриметрии
меркурометрии.
Титруют в азотнокислой среде индикатор дифинилкарбозон до фиолетовой окраски раствора.
4) 
5) 
Применение симпатомиметическое средство (сосудосуживающее, бронхорасширяющее)
Хранение СП.Б В плотноукупоренной таре.
ФЕНОЛЫ
Резорцин – Resorcinum

Мета-дигидроксибензол
Получение
Получают из природных источников путем сухой перегонки каменноугольной, древесной смолы или синтетически.
Свойства. Белый или со слабым желтоватым оттенком кристаллический порошок со слабым специфическим запахомю Под влиянием света и кислорода воздуха легко окисляется и приобретает розовое окрашивание. Очень легко растворим в воде, легко растворим в спирте, эфире, жирных маслах и в растворах щелочей.
Подлинность
1 С FeCl3 Появляется сине-фиолетовое окрашивание, исчезающее при добавлении кислоты, щелочи или спирта

2 Образование флуоресцеоната натрия ( специфическая реакция на резорцин)
Сухой препарат помещают в выпарительную чашку добавляют H2SO4 конц и фталевый ангидрид, нагревают. Образуется сплав желто-коричневого цвета, который при растворении в растворе щелочи дает раствор желто-бурого цвета с интенсивной зеленой флуоресценцией.

Количественное определение
ГФ и ВАК.Метод броматометрии (обратное титрование)
ТНП растворяют в мерной колбе, берут часть разведения пипеткой, туда помещают избыток титрованного раствора KBrO3 избыток раствора KBr и H2SO4, закрыв пробкой оставляют в темном месте на 10-15 минут, затем добавляют хлороформ и избыток KI выделившийся йод оттитровывают Na2S2O3 до обесцвечивания водного и хлороформенного слоя.


Применение.Применяют в качестве антисептического средства. Назначают при кожных заболеваниях в виде 2-5% водных или спиртовых растворов 5-20% мазей.
Хранение В хорошо укупоренных банках оранжевого стекла.
АРОМАТИЧЕСКИЕ КИСЛОТЫ И ФЕНОЛОКИСЛОТЫ
Acidum benzoicum

Получение
1 Окисление толуола
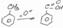
Свойства.Бесцветные игольчатые кристаллы или белый мелкокристаллический порошок. При нагревании возгоняется, перегоняется с водяным паром. Мало растворим в воде, растворим в кипящей воде, легко растворим в спирте, зфире, хлороформе и бензоле, растворим в жирных кислотах.
Подлинность
1.опр Тплав.122-124,50С
2 Реактив FeСl3
. Образуется осадок желто-розового цвета.

Нефармакопейные реакции.
1 Реакция позволяющая разделить две кислоты(бензойную и салициловую): растворяют в воде и хлороформе и прибавляют CuSO4. Водный слой окрашивается в зеленый цвет (салициловая кислота), хлороформенный слой окрашивается в бирюзовый цвет (бензойная кислота).
Количественное определение
1 Метод нейтрализации в спиртовой среде ( спирт необходим для растворения кислоты и уменьшения гидролиза продуктов реакции)
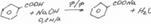
Применение Антисептическое средство.
Хранение. В хорошо укупоренной таре.
Acidum salicylicum

Орто-гидрокси бензойная кислота
Получение
1 Реакция карбоксилирование фенолята натрия (реакция идет при повышении давления, t=120-1300С)
Метод Кольбе, Шмидта

Полученную кислоту очищают путем многократной перекристаллизацией из воды
Свойства. Белые мелкие игольчатые кристаллы или легкий кристаллический порошок без запаха. Летуч с водяным паром, при осторожном нагревании возгоняется. Мало растворим в воде, растворим в кипящей воде, растворим в спирте, эфире, трудно растворим в хлороформе
Подлинность
1 Определение температуры плавления по ГФ 158-1610С
2 Реактив FeCL3
Салициловую кислоту растворяют в воде (t0) и прибавляют раствор FeCL3 появляется сине-фиолетовое окрашивание исчезающее при добавлении HCl,устойчивое при добавлении CH3COOH.

3 Реакция декарбоксилирования.
Сухой препарат нагревают с цитратом натрия, ощущается запах фенола.

4 В выпарительную чашку помещают несколько кристаллов салициловой кислоты и H2SO4 конц и нагревают осторожно. Выделившийся газ пропускают через известковую воду, которая мутнеет.
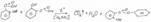 CO2 + Ca(OH)2=CaCO3+H2O
CO2 + Ca(OH)2=CaCO3+H2O
Нефармакопейные реакции
1 Реакция позволяющая разделить две кислоты растворяют в воде и хлороформе и прибавляют CuSO4. Водный слой окрашивается в зеленый цвет (салициловая кислота), хлороформенный слой окрашивается в бирюзовый цвет (бензойная кислота).
2 Получение ауринового красителя.
В выпарительную чашку помещают несколько кристаллов салициловой кислоты добавляют формальдегид и H2SO4. Появляется малиновое окрашивание.

Количественное определение
1 Метод нейтрализации в спиртовой среде (спирт добавляют для растворения кислоты и подавления гидролиза продуктов реакции)
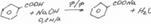
Нефармакопейный метод
Метод броматометрии




Примение.Антисептическое, кератолитическое средство.
Хранение В хорошо укупоренной таре, предохраняющей от действия света.
Natrii benzoas

Получение
Получают при нейтрализации кислот раствором Na2CO3. Полученный раствор выпаривают. Сухой остаток очищают многократной перекристаллизацией воды.

Свойства.Белый кристаллический порошок без запаха или с очень слабым запахом, сладковоъато-соленого вкуса.
Легко растворим в воде, трудно- в спирте. Реакция водных растворов щелочная.
Подлинность
1 На Na+
2 На кислотную часть
А) Реактив FeCl3
образуется осадок желто-розового цвета.

Б) К раствору препарата прибавляют соляную кислоту и образуется осадок кислоты, который отделяют, сушат и определяют температуру плавления = 120-1240С.
Количественное определение
Метод нейтрализации
ТНП растворяют в воде и добавляют эфир, добавляют смешанный индикатор метиловый синий и метиловый оранжевый (1:1). Раствор титруют раствором HCl с 0,5 моль/л и титруют до фиолетовой окраски водного слоя.
Эфир добавляют для извлечения кислоты, выделяющийся в процессе титрования.

Применение. Отхаркивающее средство.
Хранение. В хорошо укупоренной таре.
Дата добавления: 2018-02-18; просмотров: 823; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
