KBr Kalii bromidum
Получение:
Бромиды и йодиды получают одинаково. Железные стружки смешивают с водой и приливают избыток брома (йода). Тщательно перемешивают, а затем +К2CO3. Р-р фильтруют, фильтрат выпаривают.
4Br2+3Fe=>Fe3Br8 (FeBr2*2FeBr3)
Fe3Br8+4К2CO3+4H2O=>8КBr+Fe(OH)2+2Fe(OH)3+4CO2
Свойства. Бесцветные или белые блестящие кристаллы или мелкокристаллический порошок без запаха, соленого вкуса. Легко растворим в воде, мало растворим в спирте.
Подлинность.
1) К+
Крупинка соли окрашивает пламя в фиолетовый цвет.
2) Виннокаменная к-та в присутствии ацетата Na или гидротартрат Na.
COOH COOK
HCOH + KBr = HBr + HCOH
HCOH HCOH
COOH COOH (белый кристаллический осадок, растворимый в кислотах)
CH3COONa+HCl=>CH3COOH+NaCl
COONa COOK
HCOH + KBr = NaBr + HCOH
HCOH HCOH
COOH COOH (белый кристаллический осадок, растворимый в кислотах
2)Br-
Преп. р-ют в воде, подкисляют HNO3 и доб. AgNO3, обр. светло жёлтый творожестый ос., нерастворимый в HNO3, частично растворим в NH4OH.
КBr+ AgNO3=> AgBr+КNO3
AgBr+ NH4OH=> частично.
AgBr+ HNO3=>
2)С сильным окислителем.
В кач. сильного окислителя используют хлорамин или белильную известь. Несколько кристаллов препарата р-ют в воде, подкисляют соляной к-той, доб. сильный ок-ль и хлороформ, встряхивают, хлороформенный слой окр. в жёлтый или оранжевый цвет.
|
|
|
Хлорамин.
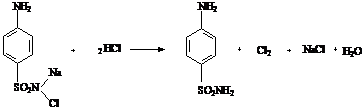
Белильная известь.
CaOCl2+2HCl=>Cl2+CaCl2+ H2O
СaClOCl - хлорид гипохлорит кальция
2КBr+Cl2===>Br2+2КCl
Количественное определение.
Аргентометрия по Мору.
ТНП предварительно высушенную в течение 4-х часов, пом. в колбу для титрования, доб. инд. K2CrO4 и титруют р-ром AgNO3, до оранжево- красного ос.
КBr+ AgNO3=>AgBr+КNO3
(.) 2 AgNO3+К2CrO4=>Ag2CrO4+2КNO3
ВАК.
1)По Мору.
2)Метод меркуриметрии.
ТНП берут пипеткой и пом. в колбу для титрования, подкисляют HNO3 и титруют р-ром нитрата окисной ртути с конц. 0,1 моль/л до сине-фиолетового окр. Инд.- дифенилкарбазон.
4 КBr+Hg(NO3)2=>К2(HgBr4)+2КNO3
(.)Hg(NO3)2+ДФК=> сине-фиол.
3)Метод меркурометрии.
ТНП пом. в колбу для титрования, подкисляют HNO3 и титруют нитратом закисной ртути (Hg2(NO3)2) до сине-фиол. окр. Инд.- ДФК.
2 КBr+ Hg2(NO3)2=>Hg2Br2+2КNO3
(.) Hg2(NO3)2+ДФК=> сине-фиол.
4)Метод аргентометрии по Фаянсу.
ТНП пипеткой пом. в колбу для титрования, + уксусную к-ту, поверхностно действующий инд. бромфеноловый синий и титруют р-ром нитрата серебра до сиреневого цвета ос.
КBr+ AgNO3=>AgBr+КNO3
Применение. Седативное средство.
Хранение. В защищенном от света месте.
|
|
|
NaI Natrii iodidum
Получение.
Бромиды и йодиды получают одинаково. Железные стружки смешивают с водой и приливают избыток йода. Тщательно перемешивают, а затем +Na2CO3. Р-р фильтруют, фильтрат выпаривают.
4 I2+3Fe=>Fe3I8 (FeI2*2FeI3)
Fe3I8+4Na2CO3+4H2O=>8NaI+Fe(OH)2+2Fe(OH)3+4CO2
Свойства. Белый кристаллический порошок, без запаха, соленого вкуса. На воздухе сыреет и разлагается с выделением йода. Очень легко растворим в воде, растворим в спирте, глицерине.
3)Определение I-.
Препарат р-ют в воде, подкисляют HNO3 и + р-р AgNO3. Обр. жёлтый ос. Нерастворимый в HNO3 и NH4OH.
NaI+AgNO3=>AgI+ NaNO3
AgI+ HNO3=>
AgI+ NH4OH=>
Cl-+ AgNO3=> AgCl – белый.
Br-+ AgNO3=> AgBr – светло жёлтый.
I-+ AgNO3=> AgI – жёлтый.
I- – сильный в-ль, поэтому его обнаруживают со слабым ок-ем – NaNO2/FeCl3.
Препарат растворяют в воде +HCl (H2SO4) и слабый ок-ль и хлороформ. Встряхивают, хлороформенный слой окр. в розовый цвет.
2FeCl3+2KI===>I2+2FeCl2+2KCl
2NaNO2+2KI+4HCl===>I2+2KCl+2NO+2NaCl+2H2O
Количественное определение.
Аргентометрия по Фаянсу
ТНП, предварительно высушенную(100С -4 ч.), р-ют в воде + уксусною к-ту. Инд. эозинат натрия. Титруют р-ром AgNO3 до :
1)Появления роз. ос.
2)Коагуляции осадка (просветление р-ра над осадком).
NaI+ AgNO3=>AgI+NaNO3
Na ind(эозинат натрия)=>Na+ind(роз.)
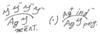
ВАК.
1)Метод меркуриметрии:
|
|
|
ТНП пипеткой пом. в колбу для титрования, подкисляют HNO3 и титруют р-ром Hg(NO3)2 с конц. 0,1 моль/л, без индекатора, до оброзования красно-оранж. ос.
4NaI+ Hg(NO3)2=>Na2(HgI4)+NaNO3
(.) Na2(HgI4)+ Hg(NO3)2=>2HgI2+2NaNO3
(.) 2NaI+ Hg(NO3)2=>HgI2+2NaNO3
2)Метод меркурометрии.
ТНП пипеткой пом. в колбу для титрования, подкисляют HNO3, доб. инд. дифенил карбазон.
2NaI+Hg2(NO3)2=>Hg2I2+2NaNO3
Применение.При недостатке йода в организме (эндемический зоб), некоторых воспалительных заболеваниях.
Хранение. В хорошо укупоренных банках оранжевого стекла, в сухом месте.
KI Kalii iodidum
Получение.
Бромиды и йодиды получают одинаково. Железные стружки смешивают с водой и приливают избыток йода. Тщательно перемешивают, а затем +К2CO3. Р-р фильтруют, фильтрат выпаривают.
4 I2+3Fe=>Fe3I8 (FeI2*2FeI3)
Fe3I8+4К2CO3+4H2O=>8КI+Fe(OH)2+2Fe(OH)3+4CO2
Свойства. Бесцветные или белые кубические кристаллы или белый мелкокристаллический порошок без запаха, солено-горького вкуса. Во влахном воздухе сыреет. Очень легко растворим в воде, растворим в глицерине, мало растворим в спирте.
Подлинность.
На катион калия.
1) Крупинка соли, внесенная в бесцветное пламя, окрашивает его в фиолетовый цвет.
2) Виннокаменая к-та в присутствии ацетата Na или гидротартрат Na.
|
|
|
COOH COOK
HCOH + KBr = HBr + HCOH
HCOH HCOH
COOH COOH (белый кристаллический осадок, растворимый в кислотах)
CH3COONa+HCl=>CH3COOH+NaCl
COONa COOK
HCOH + KBr = NaBr + HCOH
HCOH HCOH
COOH COOH (белый кристаллический осадок, растворимый в кислотах
3)Определение йодидов..
Препарат р-ют в воде, подкисляют HNO3 и + р-р AgNO3. Обр. жёлтый ос. Нерастворимый в HNO3 и NH4OH.
КI+AgNO3=>AgI+ КNO3
AgI+ HNO3=>не растворяется
AgI+ NH4OH=>не растворяется
Cl+ AgNO3=> AgCl – белый.
Br+ AgNO3=> AgBr – светло жёлтый.
I+ AgNO3=> AgI – жёлтый.
I – сильный в-ль, поэтому его обнаруживают со слабым ок-ем – NaNO2/FeCl3.
Препарат растворяют в воде +HCl (H2SO4) и слабый ок-ль и хлороформ. Встряхивают, хлороформенный слой окр. в розовый цвет.
2FeCl3+2KI===>I2+2FeCl2+2KCl
2NaNO2+2KI+4HCl===>I2+2KCl+2NO+2NaCl+2H2O
Количественное определение.
Аргентометрия по Фаянсу (с поверхностнодействующим индикатором).
ТНП, предварительно высушенную(10 С -4 ч.), р-ют в воде + уксусною к-ту. Инд. эозинат натрия(поверхностнодействующий индикатор=ПДИ). Титруют р-ром AgNO3 до :
1)Появления роз. ос.
2)Коагуляции осадка (просветление р-ра над осадком).
КI+ AgNO3=>AgI+КNO3
К ind(эозинат натрия)=>К+ind(роз.)

ВАК.
1)Метод меркуриметрии:
ТНП пипеткой пом. в колбу для титрования, подкисляют HNO3 и титруют р-ром Hg(NO3)2 с конц. 0,1 моль/л, без индекатора, до оброзования красно-оранж. ос.
4КI+ Hg(NO3)2=>К2(HgI4)+КNO3
(.) К2(HgI4)+ Hg(NO3)2=>2HgI2+2КNO3
(.) 2КI+ Hg(NO3)2=>HgI2+2КNO3
2)Метод меркурометрии.
ТНП пипеткой пом. в колбу для титрования, подкисляют HNO3, доб. инд. дифенил карбазон.
2КI+Hg2(NO3)2=>Hg2I2+2КNO3
Применение. При недостатке йода в организме, при некоторых воспалительных процессах.
Хранение. В хорошо укупоренных банках оранжевого стекла.
Solutio Iodi 5% spirituosa = Tinctura Iodi 5%
Состав:
Йода кристаллического – 50,0
Калия йодида – 20,0
Воды и спирта поровну до 1 литра.
Свойства. Прозрачная жидкость красно-бурого цвета с характерным запахом. Смешивается во всех соотношениях с водой и спиртом.
Подлинность.
К 10 мл. воды + 1 кап. р-ра йода и + крахмал => синее окр.
Испытание на чистоту.
Т.к. р-р устойчив готовится из чистых в-в, то испытание не проводится.
Количественное определение.
Определение йода и йодидов проходит в одном р-ре.
а)Опредиление йода.
ТНП пипеткой пом. в склянку с притёртой пробкой и титруют р-ром Na2S2O3 до обесцвечивания ( титрование ведут без крахмала, т.к. этот р-р будет использован для определения йодидов и крахмал мешает их титрованию).
I2+Na2S2O3===>2NaI+Na2S4O6 (тетратионат натрия).
б)Определение KI.
Р-р после титрования йода подкисляют CH3COOH, доб. индикатор эозинат натрия(ПДИ) и титруют р-ром AgNO3 до:
- роз. окраски ос.
- коагуляции ос.
KI+ AgNO3=>AgI+KNO3
NaI+ AgNO3=>AgI+NaNO3
% KI=(VAgNO3*K-VNa2S2O3*K)*TAgNO3/KI*100/навеска.
Применение. Антисептическое средство наружно, внутрь- в виде капель в молоке для профилактики атеросклероза.
Хранение. Сп.Б. В склянках оранжевого стекла, в защищенном от света месте. В.Р.Д.20 капель В.С.Д.60капель.
Элементы VI группы периодической системы
AQUAE PURIFICATA(ВОДА ОЧИЩЕНАЯ):
Получение:
Существует несколько способов очистки:
1)дистиляция в асептических условиях:
2)ионный обмен: воду пропускают через специальные смолы-иониты. 3)обратное амотическое давление: Под действием осмотического давления природная вода, оставляя все примеси проходит через полупроницаемые мембраны в виде чистого растворителя.
Испытание на чистоту:
Не должно быть: хлоридов, сульфатов, СО2 , Са, тяжёлых металлов, вост. В-ва. ; NH3 не более эталона .сухой остаток после выпаривания не д.б. более 0,001 процент. Микробиологическая чистота. Должна соответствовать требованиям на питьевую воду, т.е. не более 100 микроорганизмов в 1 мл, при отсутствии бактерий кишечной палочки и золотого стафилокока.
. Хранят не более 3-х суток.
AQUAE PRO INJECTIONITUS
Получение:
Вода очищенная не пригодная для инъекции, так как она может содержать природные вещества – погибшие микроорганизмы и продукты их жизнедеятельности или распада.Поэтому вода для инъекций должна быть пирогенной. С этой целью свежеперегнанную воду очищенную кипятят в течение 30 минут по ГФ. В настоящее время используют пирогенные электрические перегонные аппараты. Пирогенные вещества не летучие и не перегоняются с водяным паром. Они могут попасть в дистиллят с капельками воды при бурном образовании пара. Поэтому в аппаратах должен быть встроен брызгоулавливатель.
Вода годна к употреблению не более 24 часов.
Внутриаптечный контроль воды очищенной и воды для иньекции:
Вода очищенная и вода для инъекций ежедневно подвергаются качесвтенному анализу: на отсутствие хлоридов, сульфатов и кальция.
Вода, предназначенная для изготовления стерильных растворов, кроме указанных выше испытаний должна быть проверена на отсутствие востанавливающих веществ солей амония и углерода диоксида. Ежеквартально вода очищенная должна направляется в территориальную КАЛ для полного контроля.
Один раз в квартал – на отсутствие пирогенных веществ.
Два раза в квартал – на отсутствие бактерий.
SOLUTIO HYDROGENII PEROXYDI DILUTA (раствор перекиси водорода):
Получение:
электролетический способ. При электролизе концентрированной серной кислоты выделяется надсерная кислота.

Надсерная (пероксодисерная) кислота устойчива только при очень низких температурах.
При более высоких температурах она подвергается гидролизу с образованием перекиси водорода.
H2S2O8 + 2H2O -> 2H2SO4 + H2O2
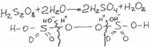
Путем перегонки в вакууме получают раствор перекиси водорода концентрированной или пергидроль (30%). Сведения о концентрированном растворе в ГФ Х.
Фармакопейный трёхпроцентный раствор получают путем разведения пергидроля в отношении 1:10.
Состав: пергидроля 10 г.; антифебрина (бензоата натрия) 0,05 г.; воды до 100 мл.
Приготовление:
В части воды растворяют пергидроль, а в другой части при нагревании растворяют антифебрин, его прибавляют к раствору пергидроля и перемешивают.
Описание: Бесцветная прозрачная жидкость со слабым специфическим запахом. Устойчива в кислой среде, в щелочной - разлагается.
Подлинность:
Реакция образования надхромовой кислоты
Препарат подкисляют серной кислотой, + эфир и по каплям р-р дихромата калия. Эфирный слой окрашивается в синий цвет
K2CrО7 + H2SO4-> H2Cr2O7 + K2SO4
Дихромовая кислота
H2Cr2O7 + H2O2 ->H2Cr2O3 +H2O
Надхромовая кислота

При стоянии синяя окраска переходит в зелёную, Cr +6 переходит в Cr +3.
H2Cr2O8 + 3H2SO4 -> Cr2(SO4)3 + 4H2O + 2O2 ^
Количественное определение:
По ГФ 10. Метод пермангонатометрии.
10 мл. препарата помещают в мерную колбу на 100 мл и доводят объем до метки. К 10 мл полученного разведения прибавляют серную кислоту и титруют 0, 1 моль/л раствором перманганата калия до слабо розового окрашивания (без индикатора).
2KMnO4 + 5H2O2 + 3H2SO4 -> 2MnSO4 + K2SO4 + 8H2O + 5O2 ^

Natrii thiosulfas.
Na2S2O3*5H2O
Получение.
Кипячением или сплавлением.
Na2SO3+S===> Na2S2O3
Свойства.
Б/ц кристаллы, без запаха, солёно-горького вкуса. В сухом воздухе выветривается, во влажном отсыревает. При нагревании до 500 плавится в собственной кристоллической воде.
Растворимость.
Очень легко растворим в воде, не растворим в спирте. Водные р-ры имеют слабо щелочную р-цию среды(щелочная- на лакмусе; фенол-фтолеиновая – нейтральная).
Подлинность.1) на катион натрия (см. хлорид натрия)
2) S2O3-2
а) Сильная минеральная к-та.(череэ некоторое время ощущается запах жженой серы и наблюдают образование осадка свободной серы )
Na2S2O3+2HCl=>2NaCl+ H2S2O3
H2S2O3=>S+SO2+ H2O
б)Избыток AgNO3.
К р-ру преп.+ AgNO3 в изб. => обр. белый осадок, переходящий в жёлтый, коричневый, чёрный(если присудствуют сульфиды, то осадок сразу чёрный).
Na2S2O3+2AgNO3=> Ag2S2O3+2NaNO3
Ag2S2O3=>Ag2SO3+S
Ag2SO3 +H2O=>H2SO4+Ag2S
Испытание на чистоту.
1)Р-р препарата д.б.б/ц и прозрачным.
2)Не д.б. превышен предел щёлочности.
3)Не д.б. недопустимых примесей: SO4, SO3, S, NH4, As, Se, Ca.
4)Хлоридов и жнлеза не более эталона.
Количественное определение.
1)Метод йодометрии.
ТНП растворяют в воде + инд. крахмал и титруют до синей окраски. Сод. препарата д.б. не менее 99% и не более 102%.(завышение объясняется возможным выветриванием препарата.)
2Na2S2O3+I2==> Na2S4O6+2NaI
Применение. Детоксицирующее средство ( при отравлении цианидами, хлором, солями тяжелых металлов), наружно как инсектицидное средство (для лечения чесотки по прописи Демьяновича)
Хранение В хорошо укупоренной таре.
Элементы IV группы периодической системы
Natrii hydrocarbonas NaHCO3
Получение.
По методу Сольбе (аммиачный способ). Р-р NaCl при пониженной t и повышеном давлении насыщают аммиаком и CО2.
2NH3+CO2+H2O==>2NH4HCO3
NaCl+NH4HCO3==>NaHCO3 +NH4Cl
NaHCO3 отделяют от р-ра и прокаливают карбонат натрия р-ют в воде, которую насыщают углекислым газом=>получ. NaHCO3 пригодный для инд. применения.
Свойства.Белый кристаллический порошок без запаха, солено-щелочного вкуса, устойчив в сухом воздухе, медленно разлагается во влажном. Растворим в воде сообразованием растворов щелочной реакции среды. Практически нерастворим в спирте.
Подлинность. 1) на катион натрия – см. натрия хлорид.
2) На гидрокарбонат ион -сильная мин. к-та.
NaHCO3+HCl==>H2CO3+NaCl

Кол-венное определение.
1)Метод нейтрализации (ацидиметрия).
ТНП р-ют в воде + инд. м/ор; титруют р-ром HCl с С=0,5 моль/л до ораньж. окр. р-ра.
NaHCO3+HCl==>H2CO3+NaCl
2)Рефрактометрией не опр. т.к. из за щел. р-ции среды может произойти порча прибора.
Применение. Антацидное средство ( для уменьшения раздражающего действия выделяющегося углекислого газа назначают со слизями=кисель или молоком), как антисептическое средство виде щелочных растворов, полосканий. ! Растворы натрия гидрокарбоната для инъекций открывают только через 2
часа после остывания раствора. Флаконы заполняются только на 0,5 объёма из-за реакции:2NaHCO3 Na2CO3+CO2+H2O
Хранение. В хорошо укупоренной таре.
Элементы 111 группы периодической системы
Acidum boricum H3BO3 кислота борная
Получ. из природного материала – тинкала.
Na2B4O2*10H2O
Na2B4O7+2HCl+5H20=>4H3BO3+2NaCl
Свойства:
Белые чешуйчатые кристаллы, слегка жирные на ощупь или белый кристаллический порошок, без запаха, кислого вкуса. Летуч с парами воды и спирта. При продолжительном нагревании теряет часть воды, переходя в мета-борную кислоту, при более сильном нагревании образуется стекловидная сплавленная масса, которая при дальнейшем нагревании, вспучиваясь, теряет всю водуЮ оставляя борный ангидрид. Мало растворим в воде, растворим в кипящей воде, мало растворим в спирте и медленно растворим в глицерине. Водные растворы имеют кислую реакцию среды.
Подлинность
1.Получение борноэтилового эфира
В выпарительную чашку помешают сухой порошок ( если раствор то выпаривают)+ спирт+H2SO4 конц.
Смесь горит пламенем с зелёной каёмкой.

2.Куркумовая бумага ее смачивают раствором борной кислоты и раствором хлористоводородной кислоты. После высыхания бумага становится розовой.
После обработки в парах аммиака окраска становится зелёно-чёрной.
Количественные определения – метод нейтрализации в среде глицерина
Борная кислота относится к очень слабым кислотам> при титрований в водном растворе реакция будет из-за гидролиза обратимой.
Борную кислоту в водной среде титровать нельзя , т.к образуется несколько продуктов реакций.
H3BO3+NaOH=>NaBO2
=>Na2B4O7

При растворений борной кислоты в глицерине образуется глицероборная кислота, которая является более сильной кислотой по сравнению с борной и является одноосновной кислотой, может образовывать только одну соль.
ТНП растворяют в глицерине и добавляют индикатор ф/ф и титруют раствором щёлочи с концентрацией 0,1 моль/л до розового окрашивания, затем снова добавляют глицерин если раствор обесцветился, то продолжают титровать до розового окрашивания .

Или в упрощенном виде:

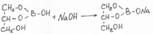
Применение. Антисептическое средство в наружной практике. Борная кислота несовместима с веществами щелочного характера.
Хранение. В хорошо укупоренной таре.
Дата добавления: 2018-02-18; просмотров: 2019; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
