Скорости газовых молекул. Распределение молекул газа по скоростям. Закон Максвелла. Наиболее вероятная, средняя квадратичная и средняя арифметическая скорости молекул.
Скорости газовых молекул (3.3. Распределение Максвелла)
Молекулы газа при своем движении постоянно сталкиваются. Скорость каждой молекулы при столкновении изменяется. Она может возрастать и убывать. Однако среднеквадратичная скорость остается неизменной. Это объясняется тем, что в газе, находящемся при определенной температуре, устанавливается некоторое стационарное, не меняющееся со временем распределение молекул по скоростям, которое подчиняется определенному статистическому закону. Скорость отдельной молекулы с течением времени может меняться, однако доля молекул со скоростями в некотором интервале скоростей остается неизменной.
Нельзя ставить вопрос: сколько молекул обладает определенной скоростью. Дело в том, что, хоть число молекул очень велико в любом даже малом объеме, но количество значений скорости сколь угодно велико (как чисел в последовательном ряде), и может случиться, что ни одна молекула не обладает заданной скоростью.
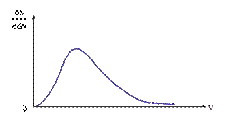 Рис. 3.3 Рис. 3.3
|
Задачу о распределении молекул по скоростям следует сформулировать следующим образом. Пусть в единице объема nмолекул. Какая доля молекул 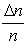 имеет скорости от v1 до v1 + Δv? Это статистическая задача.
имеет скорости от v1 до v1 + Δv? Это статистическая задача.
Основываясь на опыте Штерна, можно ожидать, что наибольшее число молекул будут иметь какую-то среднюю скорость, а доля быстрых и медленных молекул не очень велика. Необходимые измерения показали, что доля молекул 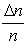 , отнесенная к интервалу скорости Δv, т.е.
, отнесенная к интервалу скорости Δv, т.е.  , имеет вид, показанный на рис. 3.3. Максвелл в 1859 г. теоретически на основании теории вероятности определил эту функцию. С тех пор она называется функцией распределения молекул по скоростям или законом Максвелла.
, имеет вид, показанный на рис. 3.3. Максвелл в 1859 г. теоретически на основании теории вероятности определил эту функцию. С тех пор она называется функцией распределения молекул по скоростям или законом Максвелла.
|
|
|
Аналитически она выражается формулой
 , ,
|
где m – масса молекулы, k – постоянная Больцмана.
Установление этой зависимости позволило определить кроме уже известной среднеквадратичной скорости еще две характерные скорости – среднюю и наиболее вероятную. Средняя скорость – это сумма скоростей всех молекул, деленная на общее число всех молекул в единице объема.
Средняя скорость, подсчитанная на основании закона Максвелла, выражается формулой

|
или
 . .
|
Наиболее вероятная скорость – это скорость, вблизи которой на единичный интервал скоростей приходится наибольшее число молекул. Она рассчитывается по формуле:
 . .
|
Сопоставляя все три скорости:
1) наиболее вероятную  ,
,
2) среднюю  ,
,
3) среднюю квадратичную  , – видим, что наименьшей из них является наиболее вероятная, а наибольшей – средняя квадратичная. Относительное число быстрых и медленных молекул мало (рис. 3.4).
, – видим, что наименьшей из них является наиболее вероятная, а наибольшей – средняя квадратичная. Относительное число быстрых и медленных молекул мало (рис. 3.4).
 Рис. 3.4 Рис. 3.4
|
При изменении температуры газа будут изменяться скорости движения всех молекул, а, следовательно, и наиболее вероятная скорость. Поэтому максимум кривой будет смещаться вправо при повышении температуры и влево при понижении температуры. Высота максимума не будет оставаться постоянной. Дело в том, что площадь заштрихованной фигуры численно равна доле 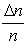 общего числа молекул n, которую образуют молекулы со скоростями в указанном интервале. Общая площадь, ограниченная кривой распределения и осью абсцисс (скоростей), таким образом, равна единице и не меняется при изменении температуры (рис. 3.5). Поэтому высота максимума и меняется при изменении температуры.
общего числа молекул n, которую образуют молекулы со скоростями в указанном интервале. Общая площадь, ограниченная кривой распределения и осью абсцисс (скоростей), таким образом, равна единице и не меняется при изменении температуры (рис. 3.5). Поэтому высота максимума и меняется при изменении температуры.
|
|
|
 Рис. 3.5 Рис. 3.5
|
Кривые распределения молекул по скоростям начинаются в начале координат, асимптотически приближаются к оси абсцисс при бесконечно больших скоростях. Слева от максимума кривые идут круче, чем справа. То, что кривая распределения начинается в начале координат, означает, что неподвижных молекул в газе нет. Из того, что кривая асимптотически приближается к оси абсцисс при бесконечно больших скоростях, следует, что молекул с очень большими скоростями мало. Это легко объяснимо. Для того чтобы молекула могла приобрести при столкновениях очень большую скорость, ей необходимо получить подряд много таких столкновений, при которых она получает энергию, и ни одного столкновения, при котором она ее теряет. А такая ситуация маловероятна.
|
|
|
Закон МАКСВЕЛЛА.
Для газа, находящегося в замкнутом сосуде, результатом многочисленных столкновений молекул между собой и со стенками сосуда, является достаточно быстрое установление универсального распределения молекул по скоростям, которое было теоретически получено Максвеллом в 1860.
На уровне макроскопического описания газамаксвелловскому распределению молекул по скоростям соответствует состояние теплового равновесия в газе: давление и температура во всех местах внутри сосуда оказываются одинаковыми.
В газе, находящемся в состоянии равновесия, установится некоторое стационарное (не меняющееся со временем) распределение молекул по скоростям, которое подчиняется вполне определенному статистическому закону.
Такой закон был теоретически выведен Максвеллом в 1859 г. и был опубликован в 1860 г.

МАКСВЕЛЛ, Джеймс Клерк ( 1831 - 1879 )
Молекулы газа даже в равновесии движутся беспорядочно, сталкиваясь между собой и со стенкой сосуда, беспрерывно меняя свою скорость. Это означает, что в каждый момент времени в газе есть молекулы, которые имеют самые различные скорости. Вместе с тем, поскольку давление и температура в газе остаются постоянными, то, как бы не менялась скорость молекул, среднее значение ее квадрата остается постоянным. Это оказывается возможным лишь при наличии неизменного во времени и одинакового во всех частях сосуда распределения молекул по скоростям.
|
|
|
При выводе этого закона Максвелл предполагал, что газ состоит из очень большого числа N тождественных молекул, находящихся в состоянии беспорядочного теплового движения при одинаковой температуре. Предполагалось также, что внешние поля на газ не действуют. Закон Максвелла описывается некоторой функциейf(v), называемой функцией распределения молекул по скоростям.
Сpедняя скоpость опpеделяется фоpмулой

Дата добавления: 2018-02-18; просмотров: 2926; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
