Реальный газ. Межмолекулярные взаимодействия. Уравнение Ван-дер-Ваальса. Критические параметры. Фазы и фазовые переходы.
Реальный газ - отличается от ид. тем, что надо учитывать собственный объем молекул и их взаимодействие между собой.
Между молекулами одновременно действуют и силы притяжения, и силы отталкивания.
Вблизи отталкиваются, а при отдалении притягиваются.
На определенном расстоянии силы притяжения и отталкивания равны, а на очень больших расстояниях не взаимодействуют. Радиус молекулярного действия- это минимальное расстояние взаимодействия, можно пренебречь 


Молекулы притягиваются – газ сжат – давление больше, чем давление на стенки сосуда.
1) 
2)молекулы могут двигатся в объеме меньшем, чем сосуд


Замечание:
1)учитывается только притяжение; молекула – шарик
2)если газ разряжен (занимат большой объем) 
Уравнение Ван дер Вальса : 

Критическая точка – это такая точка, в которой состояние жидкости и пара совпадают.

Фаза – это термодинамически равновестное, однородное по физическим св-вам состояние в-ва; это совокупность однородных частей системы.
Фазовый переход 1 рода сопровождается выделением или поглощением теплоты.
Фазовый переход 2 рода не сопровождается выделением или поглощением теплоты, а резко меняется какое-то св-во в-ва.
Тройная точка – это когда со существуют 3 фазы одновременно, это только при одной единственной температуре для данного в-ва, а 2 фаза со существует в целом интервале T и P.


Внутренняя энергия идеального газа: 
|
|
|
Кристаллическое состояние, его характеристика. Типы кристаллических решеток. Механические свойства твердых тел. Закон Гука.
Твердое тело: кристаллическое, аморфное(изотермы, близки к жидкостям).
Кристаллическое: монокристаллы(анизотропы), поликристаллы(как и аморфные тело, изотермы).

Все:

Грани центрированная объемно центрированная
 кол-во атомов приходящихся на 1 линейку
кол-во атомов приходящихся на 1 линейку
Физические типы решеток.
Подразделяются в зависимости от рода частиц в узлах решетки и от хар-ра сил взаимодействия между атомами. Типы решеток:
1)ионные NaCl (в узлах + и – ионы связаны ионной связью)
2)атомные C, Ce, Si (в узлах целые атомы, связаны ковалентной связью)
3)молекулярная (в узлах целые молекула, связаны между собой Ван дер Вальскими силами).
4) металлические, все Ме (в узлах только + ионы связанные металлической связью)
Деформация и напряжение. Деформацию сжатия и растяжения можно характеризовать абсолютным удлинением Δl , равным разности длин образца до растяжения l0 и после него l :
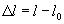 .Абсолютное удлинение
.Абсолютное удлинение  при растяжении положительно, при сжатии имеет отрицательное значение.
при растяжении положительно, при сжатии имеет отрицательное значение.
Отношение абсолютного удлинения  к длине образца
к длине образца  называется относительным удлинением
называется относительным удлинением 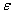 :
:  .
.
|
|
|
При деформации тела возникают силы упругости. Физическая величина, равная отношению модуля силы упругости к площади сечения тела, называется механическим напряжением  :
:
 . За единицу механического напряжения в СИ принят паскалъ (Па).
. За единицу механического напряжения в СИ принят паскалъ (Па).  .
.
Модуль упругости. При малых деформациях напряжение прямо пропорционально относительному удлинению:  . Коэффициент пропорциональности Е в уравнении называется модулем упругости. Модуль упругости одинаков для образцов любой формы и размеров, изготовленных из одного материала:
. Коэффициент пропорциональности Е в уравнении называется модулем упругости. Модуль упругости одинаков для образцов любой формы и размеров, изготовленных из одного материала:
 . Из формулы следует, что
. Из формулы следует, что  .
.
Сравнив выражение с законом Гука, получим, что жесткость k стержня пропорциональна произведению модуля Юнга на площадь поперечного сечения стержня и обратно пропорциональна его длине.
Дата добавления: 2018-02-18; просмотров: 626; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
