Также электросорбционная технология обладает высокой производительностью, не снижающейся со временем (в отличие от мембранных или волоконных фильтрационных систем).
И основное преимущество, это то, что аппараты, использующие электросорбционную технологию очистки, не требуют периодической замены каких-либо элементов в процессе эксплуатации, т.е. не требуют замены картриджей, мембран или сорбентов для своей работоспособности.
Этот процесс похож на электродиализ, но не является непрерывным. Набор мембран для этого процесса состоит из ряда сплющенных мембранных мешков, причем одна сторона мешка проявляет катионо-, а другая – анионообменные свойства (см. Рис. 2.8). При подаче электрического тока катионы, содержащиеся в исходной воде, омывающей мешок, переходят в него через сторону, проявляющую катионообменные свойства, а анионы – через другую сторону. Раствор, находящийся с внешней стороны мешков, обедняется солями, а раствор внутри мешков концентрируется. Сконцентрированный раствор может быть затем удален из мембранных мешков путем изменения направления приложенного постоянного тока на противоположное. Здесь не требуется ни прокладок, ни коллекторов для растворов [21]. 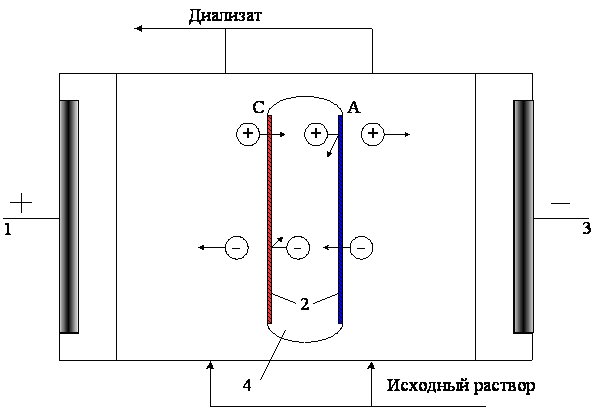
Рис. 2.8. Схема процесса электросорбции:
С – катионообменная мембрана; А – анионитовая мембрана; 1 – анод;
2 – повторяющийся элемент; 3 – катод; 4 – мембранный мешок.
http://www.membrane.msk.ru/books/?id_b=14&id_bp=423
2.2.6 Электрофорез
Электрофорез – это электрокинетическое явление перемещения частиц дисперсной фазы ( коллоидных или белковых растворов) в жидкой или газообразной среде под действием внешнего электрического поля.
|
|
|
В биологических системах и сбросных водах большинство коллоидов при обычных условиях имеют отрицательный заряд. Такие коллоиды можно удалить или сконцентрировать. Электрофоретическая ячейка состоит из ряда мембран и фильтров. Через мембраны свободно проходят небольшие ионы под действием электрического тока, а большие коллоиды задерживаются. С другой стороны, большинство коллоидов и вода свободно проходят через фильтры. Когда в мембранном наборе используют достаточно высокий внешний электрический потенциал, то отрицательно заряженные коллоиды концентрируются в секции с анодной стороны фильтра.
При наложении внешнего давления на исходный поток растворитель – вода выдавливается через фильтр а противоположную секцию. В тоже время, небольшие анионы, которые могут присутствовать в секции с исходным раствором, переносятся через мембрану в секцию, обращенную к анодной ее стороне, а катион переносится через фильтр в секцию, к которой обращена катодная сторона фильтра (см. Рис. 2.13). 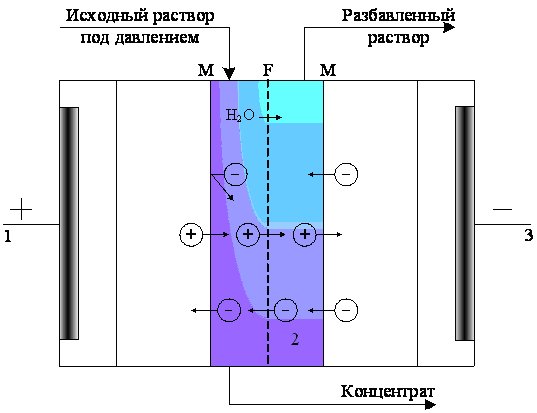
Рис. 2.13. Схема процесса с вынужденным электрофоретическим потоком:
М – плотная мембрана; F – фильтр; 1 – анод;
2 – повторяющийся элемент; 3 – катод.
|
|
|
Если бы из исходного потока надо было непрерывно удалять содержащиеся в нем небольшие ионы, то вместо нейтральных мембран было бы эффективнее применение ионообменных.
Катионообменные мембраны обладают такой высокой емкостью и настолько плотны, что практически полностью задерживают анионы, но их проницаемость по воде очень мала. Однако нейтральная мембрана высокопроницаема для воды, но не обладает достаточно большимсолезадержанием. В этом наборе (см. Рис. 2.14 ) внешний электрический потенциал заставляет соль оставаться в секции исходного раствора, а внешнее давление выдавливает воду через нейтральную мембрану в секцию, которая контактирует с ее анодной стороной.
Таким образом, этот мембранный процесс осуществляется под действием электричества и давления. Главные преимущества – это относительно небольшие затраты энергии и применение небольшого внешнего давления. Кроме того, нет необходимости нейтральные мембраны делать такими же тонкими, как активный слой у обратноосмотических мембран [21]. 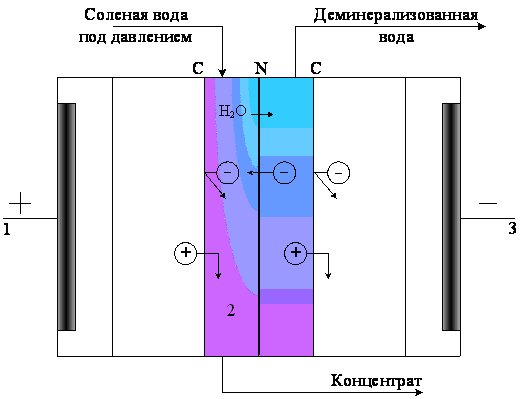
Рис. 2.14. Схема процесса обессоливания при вынужденном электрофорезе: С – катионообменная мембрана; N – нейтральная мембрана; 1 – анод;
2 – повторяющийся элемент; 3 – катод.
|
|
|
Электрофильтрование
Электрофильтрование – это метод электрообработки при котором осаждение и удерживание частиц ведут на поляризованной внешним электрическим полем диэлектрической загрузки в коллекторе и внутри ее.
Данный метод применяется в технологии использующей ионнообменные смолы.
Удержание веществ мембраной зависит от их размеров и формы молекул. В качестве индикатора удерживающей способности используется молекулярная масса растворенного вещества, при которой мембрана удерживает до 90 % молекул.
Многие вещества обладают способностью к коагуляции в стесненных условиях, вследствие чего действительный размер молекул у поверхности мембраны может оказаться намного больше, чем в исходной жидкости. Для максимального удержания данного вида молекул рекомендуется применять мембраны, граница фильтрации которых намного ниже молекулярной массы вещества. В основе данного процесса лежат эффекты воздействия на движущиеся с потоком воды частицы примесей сил однородного и неоднородного электрических полей, обеспечивающие коагуляцию частиц и их отделение от воды.
В однородном электрическом поле движение частиц обусловлено силами электрофореза, а их взаимодействие — поляризационными силами. В неоднородном электрическом поле, напряженность которого является функцией пространственных координат, на частицу помимо электрофоретической силы действует диполофоретическая сила, вызванная тем, что к одному заряду диполя частицы прикладывается поле большей напряженности, чем к другому.
|
|
|
Электроэкстракция
Электродиализ
Процесс очистки сточных вод электродиализом основан на разделении ионизированных веществ под действием электродвижущей силы, создаваемой в растворе по обе стороны мембран. Этот процесс широко используют для опреснения соленых вод. В последнее время его начали применять и для очистки промышленных сточных вод.
Методом электродиализа осуществляется разделение и концентрирование ионных при-
месей в воде. Сущность метода заключается в использовании направленного движения ионовв растворе в соответствии со знаками их заряда под действием разности потенциалов, приложенной к электродам.
Метод электродиализа целесообразно применять для очистки локальных стоков. Это даетвозможность использовать в рецикле не только очищенную воду, но исконцентрированныевещества: кислоту, щелочь. Промывные воды при наличии механических примесей направляются на фильтр, заполненный активированным углем, а при отсутствии примесей - сразу вэлектродиализатор.
Электродиализатор разделен чередующимисякатионитовыми и анионитовымимембра-
нами, образующими те же чередующиеся концентрирующие (рассольные) иобессоливающие(диэлюатные) камеры. Через такую систему пропускается постоянный ток, под действием которого катионы, двигаясь к катоду ("-"), проникают через катионитовые мембраны, но задерживаются анионитовыми, а анионы, двигаясь в направлении анода ("+"), проходят через анионитовые мембраны, но задерживаются катионитовыми. В результате этого из одного ряда камер, например, из ряда четных камер, ионы обоих знаков выводятся в смежный, нечетный, рядкамер (рис.19).
Рис.. Схема процесса электродиализа: К – катионитовые мембраны; А - анионитовые мембраны; (-) – катод; (+) – анод.
Таким образом, происходит очистка загрязненной ионами воды, которая из четных камер
собирается в один поток, а сконцентрированные соли из нечетных камер - в другой поток.
На рис. представлена принципиальная схема электродиализной очистки промывных и
сточных вод. Катоды в электродиализаторах изготавливаются из нержавеющей стали или титана, аноды - из платинированного титана или графита. Анионитовые и катионитовые мембраны марок МА-40 и МК-40 выпускаются серийно.
Очистка сточных вод в электродиализаторах ведется при следующих условиях: величина рН сточной воды - 4-9; начальная концентрация ионов тяжелых металлов до 100 мг/л,
конечная концентрация ионов тяжелых металлов до 0,1 мг/л солесодержание в сточной воде100-5000 мг/л; плотность тока - 0,8-1,8 А/дм2; скорость потока - 0,5-0,7л/мин; температура - 18-30 0С.
Периодически электродиализный комплекс промывается серной кислотой. Эта операция
позволяет содержать электродиализатор в работоспособном состоянии и избегать избыточногоэлектросопротивления от образования пленки солей на мембранах.[9.2]
Рис.. Принципиальная схема электродиализной очистки промывных и сточных вод: 1 – на-
копитель стоков; 2 – насос; 3 – механический фильтр; 4 – сорбционный фильтр; 5 – электро-
диализатор; 6 – выпрямитель.
При использовании электрохимически активных (ионообменных) диафрагм повышается эффективность процесса и снижается расход электроэнергии. Ионообменные мембраны проницаемы только для ионов, имеющих заряд того же знака, что и у подвижных ионов.
Для обессоливания воды применяют гомогенные и гетерогенные мембраны. Гомогенные мембраны состоят только из одной смолы и имеют малую механическую прочность. Гетерогенные мембраны представляют собой порошок ионита, смешанный со связующим веществом — каучуком, полистиролом, метилмер-каптаном и др. Из этой смеси вальцеванием получают пластины. Мембраны должны обладать малым электрическим сопротивлением. На эффективность работы электродиализатора большое влияние оказывает расстояние между мембранами. Обычно оно составляет 1—2 мм. Во избежание засорения мембран сточные воды перед подачей в электродиализатор должны быть очищены от взвешенных и коллоидных частиц.[9.1]
Достоинства метода [9.1]
1) Возможность очистки до требований ПДК.
2) Возврат очищенной воды до 60% в оборотный цикл.
3) Возможность утилизации ценных компонентов.
4) Отсутствие фазовых переходов при отделении примесей
что позволяет вести процесс при небольшом расходе энергии.
5) Возможность проведения при комнатных температурах без
применения или с небольшими добавками химических реагентов.
6) Простота конструкций аппаратуры.
Недостатки метода [9.1]
1) Необходимость предварительной очистки стоков от масел ПАВ органики растворителей солей жесткости взвешенных веществ.
2) Значительный расход электроэнергии.
3) Дефицитность и дороговизна мембран.
4) Сложность эксплуатации.
5) Отсутствие селективности.
6) Чувствительность к изменению параметров очищаемых
вод
Список использованных источников информации:
1) http://refy.ru/113/342427-ochistka-stochnyh-vod-galvanicheskih-proizvodstv.html
2) Сосновская Н.Г., УЧЕБНОЕ ПОСОБИЕ «ЭКОЛОГИЧЕСКИЕ ПРОБЛЕМЫ
ЭЛЕКТРОХИМИЧЕСКИХПРОИЗВОДСТВ»
Электрокатализ
Степень окисления органических загрязнений значительно увеличивается при вводе в обрабатываемую воду поваренной соли, при электролизе которой образуется активный хлор, обладающий высоким окислительным потенциалом. Для снижения затрат и повышения эффективности очистки используют катализаторы восстановления активного хлора - активированный уголь, гидроксиды и оксиды металлов переменной валентности.
Процесс электрохимической деструкции с каталитическим окислением органических
примесей осуществляют двумя методами: введением в электродное пространство вместе с потоком жидкости подвижного или гранулированного неподвижного катализатора и введением катализатора в поток после электролиза в специальном реакторе.
Преимуществом первой схемы является возможность многократного использования хло-
рид-иона в том же реакторе, поскольку атомарный кислород немедленно вступает в реакцию окисления из-за своей термодинамической неустойчивости, а хлорид-ион опять разряжается на аноде и образует активный хлор. Концентрация хлорид-ионовв растворе остается почти неизменной, хотя они непрерывно участвуют в окислительно-восстановительных процессах, благодаря чему увеличивается общий выход активного хлора. Используя подвижные катализаторы, в поток жидкости обычно вводят металлы переменной валентности в виде легкорастворяющихся солей или гидроксидов. Таким же образом используются порошкообразные активированные угли.
Для очистки различных категорий сточных вод расход катализаторов по активномуве-
ществу достигает 40 кг/м3, поэтому если катализаторы не возвращать повторно в цикл
очистки, то себестоимость обработки жидкости будет высокая. Снизить себестоимость можно созданием дополнительных узлов улавливания и регенерации катализаторов, что, в свою очередь, усложняет технологическую схему.
Размещение гранулированных катализаторов, активированных углей или материалов, со-
держащих оксиды металлов переменной валентности, в межэлектродном пространстве
несколько упрощает технологическую схему очистки. Следует также отметить, что в межэлектродном пространстве гранулы катализатора работают как биполярные микроэлектроды, вследствие чего катализаторы разрушаются и уносятся вместе с потоком очищенной жидкости. Возможно забивание пор между гранулами и уменьшение пропускной способности электролизера.
Основным недостатком этого метода является разрушение активного слоя анодныхпла-
стин, выполненных с применением неблагородных металлов. Для электролиза рекомендуются аноды на титановой основе с покрытиями из оксидов кобальта и марганца, магнетита и других металлов.
По второму варианту катализ осуществляется в отдельном реакторе. В этом случае элек-
тролизер может служить для минерализации легкоокисляемых органических загрязнений и получения активного хлора в необходимом количестве. Катализ в отдельном реакторе можно проводить как с растворенным, так и с гранулированным катализатором. Растворенные имелкодиспергированные катализаторы также требуют улавливания и возврата. Процесс технологически проще выполняется с гранулированными катализаторами. Известны два основных варианта контакта гранулированной загрузки с потоком жидкости — в виде насыпных устройств и в виде взвешенного слоя.
Данные химической технологии свидетельствуют, что наиболее эффективным является
контакт во взвешенном слое катализатора. В реакторе с гранулированной загрузкой окислению подвергается оставшаяся трудноокисляемая органика и обеспечивается дехлорированиеочищенной воды, поэтому оптимальное сочетание электролиза и последующего катализа может обеспечить высокую эффективность очистки при минимальных затратах электроэнергии. Такая технологическая схема является наиболее перспективной.
Электрокаталитическая очистка сточных вод является новой и еще мало исследованной,
особенно в области использования недорогих и доступных катализаторов, в том числе отходов промышленности, содержащих оксиды металлов переменной валентности.
Однако растущее в последнее время количество публикаций по данному вопросу, позво-
ляющих оценить состояние исследований в этой области, дает основание для определенного оптимизма. Так, например, исследован метод электрокаталитической очистки сточных вод от красителей, поверхностно-активных и текстильно-вспомогательных веществ, при котором в качестве катализатора рекомендуется использовать гранулированный активированный пиролюзит — отход термического производства диоксида марганца.
Для реализации этого метода очистки разработан комбинированный аппарат (рис.), ко-
торый имеет два блока электродов 6 с нерастворимыми анодами и камеру доочистки 4 с гранулированной каталитической загрузкой 8. Вода подается в аппарат с двух сторон через штуцеры 7, последовательно проходит по электролитическим ячейкам и переливается через верхнюю кромку катодных пластин в камеру 4. Если в процессеэлектролиза возможно образование над электродами слоя пены, как, например, при электрофлотации поверхностно-активных веществ, то эта пена наклонными козырьками крышки 1 вытесняется также в камеру 4. Местная вытяжная вентиляция 3, предназначенная для обеспечения взрывобезопасности, используется для интенсификации пеногашения за счет создания направленной струи воздуха над слоем пены из щелевого впускного канала 2.
Рис..Комбинированный аппарат для электрокаталитической очистки сточных вод.
Струя поступающего воздуха изменяет направление движения пенного слоя, прижимает
его к стенке камеры, по которой стекает очищенная вода из электродного блока. Потоки воздуха и воды, двигаясь параллельно друг другу, создают местное разрежение, что ускоряет дегазацию пены, которая быстро гасится на поверхности гранулированной загрузки. Поступающие в камеру доочистки потоки воды вместе с пеной распределяются сетчатым устройством 5 по поверхности загрузки 8.
При прохождении воды и пеноконденсата через загрузку происходит восстановление ак-тивного хлора, при котором образующийся атомарный кислород окисляет находящиеся в жидкости остаточные органические загрязнения. Очищенная вода собирается в пространстве между ложным днищем 9 и дном камеры 4 и отводится через патрубок 10.
Список использованных источников информации:
1) Сосновская Н.Г., УЧЕБНОЕ ПОСОБИЕ «ЭКОЛОГИЧЕСКИЕ ПРОБЛЕМЫ
ЭЛЕКТРОХИМИЧЕСКИХПРОИЗВОДСТВ»
Электрохимическая деструкция
При электрохимической деструкции происходит изменение рН иЕв объеме раствора за
счет электродных процессов. В прикатодном слое происходит подщелачиваниеэлектролита приразряде на катоде ионов или молекул воды, в прианодном слое раствора — подкисление средыза счет разряда ионов ОН—или молекул воды на поверхности анода. Если катодный или анодный процесс исключает разряд молекул воды, то происходит накопление только ионов Н+ илиОН—.
Величина E изменяется аналогично изменению величины рН с той разницей, что на по-
верхности электродов и в объеме раствора происходят электронные изменения, а в растворенакапливаются продукты окислительно-восстановительных реакций. Численно величина E в общей форме может быть определена по известному уравнению Нернста.
Существенное влияние на величину E раствора оказывают ионы металлов переменной
валентности, выделяющиеся в раствор при ионизации металлических анодов (катодов). В первую очередь к ним следует отнести ионы Fe2+, преимущественно выделяющиеся при растворении железных анодов. Ионы Fe2+, обладающие восстановительными свойствами, находятся врастворе в равновесии с ионами Fe3+ и молекулярным кислородом, обладающим окислительнымисвойствами. Ионы хрома Сr6+, выделяющиеся при использовании анодов из хромоникелевых сталей, придают раствору окислительные свойства.
Наибольший сдвиг в область положительных значений E ≥ (1,0÷1,2) В, превышающих потенциалы верхнего предела устойчивости воды, обеспечивают ионы хлора, разряжающиеся нааноде. За счет хорошей растворимости в воде газообразного хлора в слабокислых и нейтральных растворах образуется ион гипохлорита, а при высоких рН — хлорноватистая кислота. Этисоединения должны окислять воду до тех пор, пока E не сдвинется в область термодинамической устойчивости.
Менее существенно влияют на величину E выделяющиеся при электролизе кислород и водород. Как установлено расчетами, величину E воды, нейтральной с точки зрения окислительно-восстановительного взаимодействия, можно повысить за счет растворения кислорода толькона 0,526 В (до верхнего предела устойчивости +0,814 В), а за счет растворения водорода — понизить на 0,9 В (до нижнего предела устойчивости —0,414 В). Разумеется, если жидкость содержит вещества, легко окисляющиеся кислородом или восстанавливающиеся водородом, топри сдвиге потенциала от равновесного достижение предельных значений E возможно толькопосле их полного окисления иливосстановления.
Величина E природных и сточных вод, подвергающихся электролизу, зависит от многих
факторов:
- температуры раствора и ее изменения;
- перемешивания электролита;
- продолжительности контакта с воздухом;
- координаты точки отбора пробы для оценки этого значения.
Для электрокорректирования рН и E применяют как бездиафрагменные, так и диафрагменные электролизеры.
Бездиафрагменные электролизеры используются в тех случаях, когда процессы, протекающие на поверхности рабочего электрода, необратимы или изменение свойств раствора в приэлектродных зонах не влияет отрицательно на выход требуемых продуктов.
Диафрагменные электролизеры обеспечивают разделение продуктов электродных реак-
ций, смешение которых исключает эффект изменения рН и E. Как правило, разделение продуктов реакций осуществляется с помощью ионообменных или инертных диафрагм. Разделение можно производить также без диафрагм, отбирая католит и анолит непосредственно из приэлектродных зон.
Наиболее широко в практике водоочистки используется бездиафрагменный электролиз с
нерастворимыми электродами в присутствии хлор-ионов, при котором редокси-потенциал обрабатываемой воды повышается до значений 0,9÷1,1 В за счет образования молекулярного хлора, хорошо растворяющегося в воде. Этот метод нашел также применение для окисления простыхи комплексных цианидов.
При растворении железных анодов в бездиафрагменном электролизере происходит снижение E среды до значений — (0,4÷ 0,8) В за счет перехода в раствор ионов двухвалентного железа, обладающего восстановительными свойствами. Это позволяет восстанавливать шестивалентный хром в сточных водах гальванического производства, меховых фабрик и др.
Базовыйэлектрокорректор рН состоит из катодных и анодных камер, разделенных элек-
тродными блоками-модулями, подводящих и отводящих лотков и арматуры (рис.).
Конструктивной особенностью блока электродов является то, что он состоит из перфори-
рованных катодов и инертных анодов (ОРТА, графит, нержавеющая сталь и др.). При этом сами электроды и диафрагма плотно прижаты друг к другу с изоляцией внутренней поверхности электродов специальным материалом (лаки, краскии др.). Электрокорректоры могут быть выполнены фильтр-прессного или емкостного типов.
При обработке воды с высоким солесодержанием (1÷5 г/л) возможно обычное размещение
электродов или устройство блоков-модулей без диафрагмы с уменьшением размеров отверстий в электродах до 1÷3 мм. Вместо диафрагмы можно использовать сплошную диэлектрическую пластину, не доходящую до дна корпуса аппарата.
Рис.. Диафрагменный электрокорректор рН безнапорного типа: 1 — боковые стенки; 2 —электродные блоки; 3 — катодные камеры; 4 — анодные камеры; 5 — лоток для сбора анолита; 6 — распределительная система исходной воды; 7 — лоток для сбора католита; 8 — катод; 9 — анод; 10 — диафрагма
Электрохимическое корректирование рН и E имеет существенные преимущества перед
химическим. Кроме исключения ввода дефицитных реагентов, предотвращающих загрязнениеводы катионными и анионными остатками кислот и щелочей, преимуществом является такжеи то, что в результате электролиза изменяются многие физико-химические характеристикиводы, обеспечивающие ее ≪активность≫. Такая вода обладает лучшими обезжиривающими и моющими свойствами, биологически активна и можетиспользоваться по самому широкому назначению.
Список использованных источников информации:
1)Сосновская Н.Г., УЧЕБНОЕ ПОСОБИЕ «ЭКОЛОГИЧЕСКИЕ ПРОБЛЕМЫ
ЭЛЕКТРОХИМИЧЕСКИХПРОИЗВОДСТВ»
Дата добавления: 2018-02-15; просмотров: 1013; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
