Примеры решения типовых задач по теме жёсткость воды
Задача 1: Рассчитайте общую жесткость воды (ммоль/л), если в 0,15 л воды содержится 16,2мг гидрокарбоната кальция, 2,92мг гидрокарбоната магния, 11,10 мг хлорида кальция и 9,50мг хлорида магния.
Решение: Выразим общую жесткость воды как сумма милимолярных концентраций эквивалентов двухзарядных катионов металлов (или соответствующих их солей) в воде:
Жобщ =  ;
;
где m1, m2, mi - массы двухзарядных катионов металлов (или соответствующих им солей) в воде, мг;
M1, M2 и Mi – миллимолярные массы эквивалентов двухзарядных катионов металлов (или соответствующих им солей) в воде, мг/ммоль;
V- объем воды, л.
Определим миллимолярные массы эквивалентов солей, обуславливающих жесткость воды:
| Соль | Са(HCО3)2 | Mg(HCО3)2 | СаCl2 | Mg Cl2 |
| М(1/2), ммоль/л | 81 | 73 | 55.5 | 48 |
Общая жесткость данного образца воды равна сумме временной и постоянной жесткости и обуславливается содержанием в ней солей, придающих ей жесткость:
Жобщ =  = 2,56 ммоль/л
= 2,56 ммоль/л
Ответ: Жобщ = 2,56 ммоль/л
Задача 2: Найдите временную жесткость воды, если на титрование 0,1л образца воды, содержащий гидрокарбонат магния, израсходовано 7,2  10-3 л 0,14н HCl.
10-3 л 0,14н HCl.
Решение: При титровании воды соляной кислотой происходит реакция
Mg(HCO3)2 + 2НС1 = MgCl2 + 2Н2О + 2СО2
Воспользуемся уравнением (1):
Жврем =  =
= 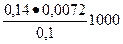 =10,08 ммоль/л
=10,08 ммоль/л
Ответ: Жврем = 10,08 ммоль/л
Задача 3: Для устранения общей жесткости по известково-содовому методу добавлено 7,4г Са(ОН)2 и 5,3г Na2CO3. Рассчитать временную и постоянную жесткость воды.
|
|
|
Решение: Добавление к воде Са(ОН)2 может устранить временную жесткость, а добавление Na2CO3 – постоянную жесткость. При добавлении этих реагентов к воде происходят следующие реакции:
Mе(HCО3)2 + Са(ОН)2 = МеCО3  + СаCО3
+ СаCО3  + 2Н2О
+ 2Н2О
Mе(NО3)2 + Na2CO3 = MeCO3  + 2NaNO3
+ 2NaNO3
(где Ме2+ = Са2+; Mg2+; Fe2+ и др. )
Временную жесткость воды Жвр измеряют количеством гидроксида кальция, участвующую в реакции, а постоянную жесткость Жпост- количеством карбоната натрия.
Жвр= 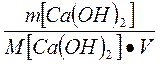 ;
;
Жпост =  ;
;
M[1/2 Са(ОН)2] = 74/2=37мг/ммоль; M(1/2 Na2CO3) = 106/2=53мг/ммоль;
Жвр = 7400/(37  50) = 4 ммоль/л;
50) = 4 ммоль/л;
Жпост = 5300/(53  50) = 2 ммоль/л;
50) = 2 ммоль/л;
Общая жесткость воды равна: Жобщ = Жвр + Жпост = 4 + 2 = 6 ммоль/л
Ответ: Жвр = 4 ммоль/л; Жпост = 2 ммоль/л.
Окислительно-восстановительные реакции
Теоретические пояснения
Реакции, протекание которых связано со смещением или полным переходом электронов от одних атомов или ионов к другим, называются окислительно-восстановительными. Число электронов, смещенных от атома (иона) данного элемента к атому (иону) данного элемента в соединении, называют степенью окисления. Степень окисления может быть положительной (электроны смещены от атома или иона) и отрицательной (электроны смещены к атому или иону).
|
|
|
Процесс отдачи электронов, т.е. повышения степени окисления элемента, называют окислением, а вещества отдающие электроны, восстановителями. К типичным восстановителям относятся простые вещества, атомы которых характеризуются невысокой электроотрицательностью (металлы, водород, углерод), некоторые анионы (Cl - , S 2- , SO 3 2- и др.), катионы, у которых степень окисления может возрастать (Fe 2+ , Sn 2+ и др.), некоторые соединения углерода (углеводороды, оксид углерода), азота (азотоводороды), бора (бороводороды) и др.
Процесс присоединения электронов, т.е. понижение степени окисления, называют восстановлением, а вещества, принимающие электроны, называют окислителями. К окислителям относятся простые вещества, атомы которых характеризуются высокой электроотрицательностью (элементы VI и VII групп главных подгрупп), катионы с высокой степенью окисления (Pb +4 , Cr +6 , Ge +4), анионы, в которых электроположительный элемент имеет высокую степень окисления (NO 3 - , Cr 2 O 7 2- , MnO 4- и др.), высшие оксиды, а также пероксиды.
Окислительно-восстановительные реакции – это одновременно протекающие процессы окисления и восстановления. Реакции, в которых окислители и восстановители представляют собой разные вещества, называют межмолекулярными. Если окислителями и восстановителями служат атомы или ионы одной и той же молекулы, то такие реакции называют внутримолекулярными.
|
|
|
Направление окислительно-восстановительных реакций определяется вторым законом термодинамики. Если процесс протекает при изобарно-изотермических условиях, то прямая реакция возможна при условии, что энергия Гиббса ее ниже нуля:  .
.
Окислительно-восстановительную способность вещества определяет окислительно-восстановительный потенциал реакции (редокс-потенциал) окислительная способность веществ тем выше, чем больше положительное значение окислительно-восстановительного потенциала реакции.
В общем виде обратимую реакцию окисления-восстановления можно записать уравнением
 (9.1)
(9.1)
где Ox – окисленная форма веществ;
Red – восстановленная форма веществ.
Уравнение окислительно-восстановительного потенциала (  ) для этой реакции имеет вид:
) для этой реакции имеет вид:
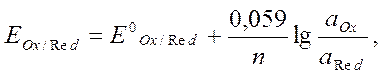 (9.2)
(9.2)
где  – стандартный окислительно-восстановительный потенциал;
– стандартный окислительно-восстановительный потенциал;
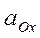 ,
,  – активности соответственно окисленной и восстановленной форм веществ.
– активности соответственно окисленной и восстановленной форм веществ.
В случае если в окислительно-восстановительных реакциях участвуют ионы водорода или гидроксида, потенциалы этих реакций зависят от pH, например, для реакции
|
|
|
NO 3 - + 3 H + + 2 e - = HNO 2 + H 2 O (9.2)


Дата добавления: 2019-09-08; просмотров: 5053; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
