Стволовые клетки, или Сделай сам

«У господа бога впервые появился конкурент», – не так давно во всеуслышание заявил один из авторов журнала Nature. Он имел в виду успехи синтетической биологии последнего десятилетия. Однако прежде чем говорить о конструировании искусственных микроорганизмов, закончим разговор о стволовых клетках, начатый в предыдущей главе.
Помните о клоне наиболее пластичных стволовых клеток, умеющих превращаться в любую ткань? Их называют эмбриональными стволовыми клетками, потому что они образуются в процессе эмбрионального развития и откладываются в организме «про запас». Эти клетки получают в наши дни методом терапевтического клонирования. Суть его сводится к тому, что у человека в любом возрасте берут самую обычную клетку и пересаживают ее ядро в донорскую яйцеклетку, которая немедленно начинает дробиться – прямо в пробирке. Через пять дней она достигает стадии бластоцисты – полого шарика из нескольких сотен клеток, значительная часть которых приходится на универсальные стволовые. Такие клетки можно размножать и неограниченно долго поддерживать в виде клеточной культуры, а их полная генетическая идентичность тканям пациента исключает проблемы с иммунитетом.
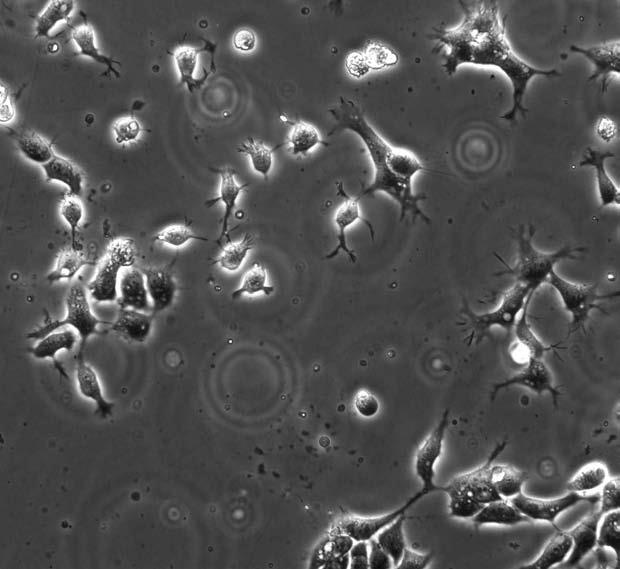
Эмбриональные стволовые клетки человека под микроскопом
Но в клинической медицине их используют крайне редко – только по жизненным показаниям, когда никакое другое лечение уже не помогает. Беда в том, что они способны превратиться во что угодно, очень плохо понимают химические команды взрослого организма и склонны к неограниченному делению. Если их ввести в организм, они легко могут спровоцировать злокачественный рост или вызвать образование тератом[51], что и было не раз показано в экспериментах на животных. Например, крысам, страдающим искусственно вызванной болезнью Паркинсона[52], пересадили эмбриональные стволовые клетки и добились массового их превращения в нейроны. Сначала все шло хорошо, и состояние крыс заметно улучшилось вплоть до полного исчезновения симптомов болезни. Однако на 10-й неделе эксперимента дифференцировку[53] сохранили всего 25 % нейронов, остальные же вновь превратились в неспециализированные клетки, которые начали активно размножаться, заселяя крысиный мозг. Руководитель опытов Стивен Голдман так прокомментировал наблюдаемую картину: «Не нужно быть нейроонкологом, чтобы понять, что этот процесс – начало образования опухоли».
|
|
|
Однако не все так безнадежно. Стволовые клетки находят применение в ортопедии: с помощью особого сигнального белка ученые стимулируют их трансформацию в остеобласты – клетки костной ткани. Биологи научились выращивать образцы различных тканей прямо в лабораторной посуде, если удается как следует «объяснить» универсальным стволовым клеткам, во что они должны превратиться. Больному пересаживают уже готовый продукт.
|
|
|
Биолог Борис Жуков пишет:
В лабораториях разных стран сегодня выращивают лоскуты живой кожи (для пересадок на обожженные места), хрящи в форме уха и даже участки кровеносных сосудов – настоящие, многослойные, с эпителием внутри и мышцами в толще стенки.
А совсем недавно пришло сообщение о том, что американские ученые сумели восстановить у цыплят ранее ампутированные крылья, «запустив» группу генов семейства Wnt. Эти гены управляют формированием конечностей в период эмбрионального развития, но у взрослых животных они «молчат». Американцам удалось заставить их работать, в результате чего произошла полная регенерация удаленного крыла. А поскольку удалось активизировать эти гены у цыплят, то, в принципе, их можно «разбудить» и у человека, так как в нашем геноме они тоже присутствуют. Быть может, пройдет не так уж много лет, и технология по отращиванию утраченных рук и ног станет реальностью.
А теперь вернемся к синтетической биологии. Под ней понимается не банальная генная инженерия наподобие внедрения в бактериальную клетку полезных генов (генно-инженерный инсулин применяется с 1982 года), а создание искусственных микроорганизмов, которые будут делать абсолютно все, что мы захотим. Сотруднику швейцарского политехнического института в Цюрихе Свену Панке это видится примерно так:
|
|
|
Мы примемся собирать бактерии из отдельных модулей, так что они станут соответствовать нашим представлениям <…> о производстве того или иного вида сырья, и вовсе не будут отвечать своему природному назначению.
Перспективы открываются воистину ошеломляющие. Ведь запасы нефти на нашей планете неуклонно тают, а с биотопливом из растительного сырья, о котором рассказывалось выше, дела обстоят не так хорошо, как хотелось бы. Например, энергоемкость спирта почти вдвое уступает бензину, поэтому и в бак его придется заливать в два раза больше, чтобы проехать то же самое расстояние. Выходом из положения мог бы стать бутиловый спирт, но его в процессе дрожжевого брожения образуется сравнительно немного. Если же заменить крахмал целлюлозой, то технология ощутимо усложнится, потому что целлюлозу нужно будет разлагать на отдельные компоненты.
|
|
|
А вот если «перепрограммировать» дрожжевые грибы таким образом, чтобы они питались целлюлозой вместо сахара и крахмала, хитрая проблема разрешится сама собой. По словам Джея Каслинга, сотрудника Калифорнийского университета, подобная технология станет реальностью уже к середине текущего десятилетия. Использование модифицированных дрожжей позволит получать биологическое топливо из древесины, соломы и других сельхозотходов. «На смену нефтяной индустрии должна прийти биология», – уверенно заявляет Крейг Вентер, бесспорный первопроходец в области микробного конструирования.

Крейг Вентер
Работы Вентера как раз и положили начало синтетической биологии. Первым делом он реконструировал бактериофаг phi X 174, кольцевая молекула ДНК которого содержит 11 генов и 5386 нуклеотидных пар. Это серьезное достижение, ибо фаги, паразитирующие на бактериях, устроены достаточно сложно.

Бактериофаг phi X174 (его объемная модель). Относительная простота этого микроорганизма позволила американским ученым «собрать» его в лаборатории из отдельных «деталей»
А вот самая примитивная среди известных вирусоподобных частиц (вироидов) носит очень длинное название – «вироид кокосовой пальмы каданг-каданг» и состоит всего из 246 нуклеотидов. Однонитчатая РНК этого вироида замкнута в кольцо и не содержит даже истинных генов, кодирующих белки, поэтому у него отсутствует белковая оболочка, позволяющая ввести генетический материал через неповрежденную клеточную стенку.
Российский биолог Александр Чубенко пишет:
Геном наиболее простых вирусов содержит всего три гена, которые кодируют белки, необходимые для воспроизводства: белок, вызывающий разрыв клеточной стенки хозяина; фермент, обеспечивающий многократную репликацию своего генома; и белок капсида – оболочки, покрывающей вирусную ДНК или РНК. Пример такого вируса – бактериофаг Q, инфицирующий кишечную палочку Escherichia coli. Его РНК состоит примерно из 3500 нуклеотидов. Самые большие вирусы содержат две-три сотни генов, закодированных в двухцепочечной нити ДНК длиной в несколько сотен тысяч пар нуклеотидов.
Усилия биологов по реконструкции вирусных частиц могут со временем пролить свет на проблему происхождения жизни на Земле (если, конечно, не считать, что она была занесена из космоса в ходе астероидной и кометной бомбардировки нашей планеты на заре ее образования). Современные вирусы, как мы помним, являются строгими внутриклеточными паразитами, поэтому выжить в «мертвой» они среде не могли. Но можно ли допустить, что некий доисторический протовирус умел размножаться самостоятельно, без помощи белков-ферментов, а впоследствии эту способность утратил?
Как известно, современным нуклеиновым кислотам такие подвиги не под силу: ДНК и РНК всех без исключения организмов, от простейших вирусов до высших животных и человека, нуждаются в услугах целой армии специфических белков, чтобы передавать закодированную информацию в ряду поколений. Сегодня ни одна из нуклеиновых кислот не может себя копировать без посторонней помощи. Выходит, что наш гипотетический вирус обречен: он должен появиться на свет только после того, как клеточные формы жизни с их сложным набором ферментов станут полноправными обитателями первобытного океана.
Но клетка (даже самая элементарная) – чересчур громоздкая структура, чтобы возникнуть скачком, в одночасье. И если мы хотим избавиться от «божественного» представления о зарождении жизни на Земле, нам требуется нарисовать закономерную и непротиворечивую картину возникновения естественным путем сложных макромолекул, способных к самосборке, что со временем приведет к рождению генетического кода, а затем и первых клеток. Жизнь – процесс антиэнтропийный (энтропия – мера беспорядка), для нее характерно самопроизвольное упорядочение и структурное усложнение, а суть этого упорядочения заключается в ограничении свободы. Порядок наводят тысячи белков-ферментов, благодаря которым химические реакции идут в нужном направлении, но беда в том, что белки не умеют сами себя воспроизводить. Способностью к воспроизведению обладают нуклеиновые кислоты, но они лишены каталитической активности и потому нуждаются в помощи ферментов. Таким образом, два важнейших свойства, необходимых для эволюции, – способность к упорядочению и способность к воспроизведению – оказались разделены между двумя классами органических структур. Как природа сумела их объединить?
В 1970-х годах были обнаружены совершенно необычные ферменты, включавшие в свой состав кроме белка еще и молекулу РНК. Когда белок полностью удалили, неожиданно выяснилось, что оставшаяся РНК способна катализировать свою специфическую реакцию. Это было сенсацией, поскольку всегда считалось, что к катализу способны только белки и уж никак не нуклеиновые кислоты. Способные к катализу молекулы РНК назвали рибозимами (по аналогии с энзимами – белковыми ферментами). Многие ученые сразу же заговорили о том, что «в начале была РНК». И действительно, вообразим себе молекулу, которая не только является носителем информации, но и вдобавок умеет катализировать химические реакции. Это же готовый кандидат на роль нашего искомого протовируса, давшего со временем начало всем остальным живым существам!
Но Вентер не остановился на полпути: ведь существуют еще и бактерии, которые тоже подлежат оптимизации. Крэйг Вентер решил, что для его целей больше всего подходят микоплазмы – очень мелкие бактерии, сопоставимые по размерам с крупными вирусами.
Если воздействовать на бактериальную клетку определенными веществами (например, лизоцимом), можно получить формы, лишенные клеточной стенки. Такие «рукотворные» микроорганизмы, получившие название L-форм, чрезвычайно уязвимы и весьма чувствительны к факторам среды. Они способны выживать только в особо благоприятных условиях, когда внешнее осмотическое давление находится в равновесии с внутриклеточным.
Однако микроорганизмы без клеточной стенки найдены и в природе. К их числу относятся микоплазмы – паразиты животных, растений и человека, наиболее примитивные бактериоподобные существа, имеющие клеточное строение. К тому же они самые мелкие из всех бактерий и по размерам приближаются к вирусам. Если, например, вирус гриппа чуть меньше одной десятой микрона, а размеры вируса коровьей оспы колеблются в пределах от 0,22 до 0,26 микрон, то диаметр микоплазмы, вызывающей повальное воспаление легких у рогатого скота, находится в пределах 0,1–0,2 мкм. При этом неприхотливые микоплазмы в отличие от вирусов могут расти и размножаться на синтетической питательной среде, то есть являются полноценными одноклеточными микроорганизмами.
Микоплазменная клетка построена из сравнительно небольшого числа молекул (около 1200), но имеет полный набор компонентов, необходимых для самостоятельного выживания (ДНК, РНК, белки), и содержит около трехсот ферментов. По некоторым признакам микоплазмы стоят ближе к животным, чем к растениям: их клетки заключены в гибкую цитоплазматическую мембрану, а их липидный состав близок к аналогичному показателю в животных клетках.
Крэйг Вентер работал с Mycoplasma genitalium – условно-патогенным обитателем мочеполовых путей, который состоит всего из 517 генов (из них 480 кодируют белки, а 37 – различные молекулы РНК), тогда как нуклеоид средней бактериальной клетки содержит от двух до четырех тысяч генов. Такая неслыханная простота делает микоплазмы идеальным объектом для генно-инженерных манипуляций.
Александр Чубенко отмечает:
Для выживания простейшей «версии» микроорганизма эти гены (имеется в виду полный набор из 517 генов. – Л.Ш .) не являются обязательными. Аккуратно, один за другим, вырезая эти гены из хромосомы M. genitalium, исследователи установили, что в ее лаконичном геноме только около 300 генов действительно необходимы для существования бактерии в питательном бульоне.
Проект «Минимальный геном» направлен на создание простейшего из простейших жизнеспособного одноклеточного организма. После этого можно будет проводить «апгрейдинг устройства с минимальной конфигурацией». В обычной бактериальной клетке избыточная продукция естественных метаболитов или синтез белка, закодированного в трансгене, конфликтует с основными программами, записанными в тысячах генов и обеспечивающими выживание клетки в природных условиях. В клетке с минимальным геномом все ресурсы, кроме необходимых для жизни и деления в тепличных условиях биореактора, будут направлены на синтез необходимых человеку белков.
Микоплазменный геном сотрудники института Крэйга Вентера собрали в 2008 году, а в 2010-м был предпринят решающий эксперимент, вобравший в себя все многолетние наработки. Синтетический геном бактерии Mycoplasma mycoides длиной более миллиона нуклеотидов внедрили в бактерию другого вида – Mycoplasma capricolum, ДНК которой была заранее удалена. Клетка, где поселился геном-агрессор, отныне выглядела как бактерия Mycoplasma mycoides, успешно размножалась и синтезировала именно те белки, которые ей и положено синтезировать.
Разумеется, никто не утверждает, что Крэйгу Вентеру действительно удалось создать искусственную жизнь. Не следует забывать, что Вентер работал исключительно с геномом, а цитоплазму и внутриклеточные органеллы использовал в готовом виде.
Австрийский биолог Маркус Шмидт пишет:
ДНК составляет примерно один процент сухого веса клетки. Если мы синтезировали всего один процент содержимого клетки, то у нас нет никакой причины утверждать, что мы создали живую клетку. Ведь нам не по силам пока синтезировать цитоплазму. Этого не делал никто.
Однако недооценивать и работы Вентера тоже не стоит, поскольку современные биотехнологии находят сегодня очень широкое применение. Так, совсем недавно ученые сумели «приручить» кишечную палочку – бактерию Escherichia coli, внедрив в нее гены полыни и дрожжей. Отныне она будет синтезировать артемизинин – лекарство, получаемое из однолетней полыни и незаменимое при лечении малярии, которой ежегодно заболевает около 250 миллионов человек. А уже знакомый нам Джей Каслинг собирается наладить массовый выпуск этого препарата и обещает снизить его цену с 2,2 доллара до 25 центов.
В обозримом будущем модифицированные бактерии помогут людям заселить землеподобные планеты – Марс или даже Венеру. А почему бы и нет? В полярных шапках Красной планеты хватает воды, а разреженная марсианская атмосфера, состоящая в основном из двуокиси углерода, может обеспечить неплохой парниковый эффект, если ее дополнительно насытить газами вроде метана. На Земле до сих пор существуют древние бактерии (археи), которые гораздо примитивнее обычных микроорганизмов и могут выживать в исключительно неблагоприятных условиях.
Например, некоторые археи имеют оптимальную температуру роста свыше 100 °C, за что получили название экстремальных термофилов. Прокариоты этой группы обитают на океанском дне, на глубинах порядка двух с половиной километров, где давление составляет 260 атмосфер, а температура воды в зонах выхода горячих термальных источников достигает 250–300 °C. Описаны археи, предпочитающие всему на свете кислую среду, и такие анаэробные формы, метаболизм которых связан с молекулярной серой. Надо сказать, что метаболизм этих необычных микроорганизмов в высшей степени уникален и никогда не встречается у типичных бактерий или эукариот. Например, только у архей обнаружены бесхлорофилльный фотосинтез и особый тип анаэробного (бескислородного) дыхания, в процессе которого происходит образование метана. Такие архебактерии получили название метанобразующих. Кстати, весьма любопытно, что среди прокариот этой группы отсутствуют патогенные и паразитические формы.

Древние бактерии (археи) под микроскопом
Вскоре после успеха Крэйга Вентера и его команды профессор Принстонского университета Майкл Хечт создал гены, кодирующие не существующие в природе белки. Белковая молекула построена всего из 20 аминокислот, однако этого более чем достаточно, поскольку в состав белковой молекулы входит несколько сотен аминокислот. Если их перетасовать, мы получим новый белок с принципиально иными свойствами. Число мыслимых комбинаций многократно превышает количество реальных белков, но это не означает, что любая комбинация даст на выходе работоспособный продукт. Одни белки окажутся нестабильными, другие – токсичными, ну а третьи – просто бесполезными. И все же среди бесчисленного множества виртуальных белков наверняка должны отыскаться аминокислотные последовательности, способные катализировать нужную организму реакцию. Именно такие белки и попытались создать принстонские ученые.
Биолог Борис Жуков пишет:
Для начала специальная компьютерная программа составила более миллиона аминокислотных последовательностей – термодинамически устойчивых и не похожих на известные белки. Из них ученые отобрали 27, трехмерная структура которых (рассчитанная опять-таки компьютером) позволяла предполагать, что они могут проявлять ферментативную активность[54]. Для каждого такого белка была написана последовательность нуклеотидов, которая могла бы его кодировать, – то есть ген. Каждый такой ген был искусственно синтезирован, а затем внедрен в ДНК бактерии, у которой перед этим был удален один из «естественных» генов. После этого «реконструированные» клетки были высажены на специальную среду, для жизни на которой необходим белок, кодируемый удаленным геном. На такой среде бактерия могла выжить лишь в том случае, если небывалый белок, считанный с искусственного гена, заменит утраченный фермент.
В четырех случаях из 27 именно это и произошло: клетки, лишенные жизненно важного гена, успешно росли и размножались. Белок, придуманный исследователями, не только успешно считывался в клетке, но и работал в ней.
Комментарии излишни: если эксперимент принстонских специалистов завершится созданием надежной технологии, можно будет не только синтезировать практически любые вещества, но и создавать организмы, не существующие в природе.
Хотя успехи молекулярной биологии последних десятилетий буквально ошеломляют, обольщаться сверх меры все же не стоит. Например, сравнительно недавно большой коллектив ученых во главе с профессором Киотского университета Акирой Иритани объявил о начале работ по воссозданию живого мамонта из палеолитических останков, похороненных в вечной мерзлоте. По мнению участников проекта, цель может быть достигнута уже через пять-шесть лет.

Источники генетического материала для клонирования – замороженные мамонтята
Большинство ученых весьма скептически относятся к таким заявлениям. Дело в том, что генетический материал мамонтов сохранился в виде мелких фрагментов, поскольку кристаллики льда при замерзании необратимо нарушают тончайшую клеточную структуру, в том числе ядерную мембрану. А цитоплазматические ферменты – нуклеазы, получив доступ к молекулам ДНК, за десятки тысячелетий успели поработать на совесть. Поэтому вместо строгой линейной последовательности генов мы имеем «кашу» из отдельных субъединиц, своего рода рассыпанный типографский набор.
Борис Жуков пишет:
Современные методы работы с нуклеиновыми кислотами позволяют сложить эти фрагменты в исходную последовательность – но, естественно, виртуально. Синтезировать по ней реальные молекулы ДНК длиной в сотню миллионов пар нуклеотидов (средний размер хромосомы мамонта) пока еще никто не пытался. К тому же сначала надо бы как-то узнать, какой фрагмент в какой хромосоме находится, – притом что обычные методы генетического картирования неприменимы к ископаемому материалу.
Но главная трудность даже не в этом. Ведь хромосома – это не просто молекула ДНК, а сложное нуклеопротеидное соединение, куда входят так называемые гистоновые белки. Мы пока еще слишком мало знаем о тонкой структуре хромосом, чтобы воссоздать ее в законченном виде. А как быть с клеточным ядром – ведь в ископаемых тканях целых ядер не сохранилось? Между тем ядра тоже придется собирать заново, потому что современные технологии клонирования предусматривают пересадку в донорскую яйцеклетку именно ядра, а не отдельных хромосом и уж во всяком случае не «голых» молекул ДНК. И совершенно непонятно, каким образом участники проекта намереваются обойти эти трудности.
Однако это еще далеко не все. Коротко напомним читателю, к чему сводится технология клонирования. Генетический материал (обязательно в виде клеточного ядра) помещают в донорскую яйцеклетку, из которой удалено ее собственное ядро, а затем подсаживают эту яйцеклетку в полость матки суррогатной матери. Именно так появилась на свет знаменитая овечка Долли.

Овечка Долли и ее «создатель» английский эмбриолог Ян Вилмут
На бумаге, конечно, все выглядит гладко, но следует иметь в виду, что клонирование – очень трудоемкая и капризная процедура. Большая часть пересаженных яйцеклеток отторгается, и даже сегодня в самых лучших современных лабораториях эффективность клонирования составляет всего лишь несколько процентов. И это при том, что технология хорошо обкатана, а все три особи (источник генетического материала, суррогатная мать и донор яйцеклетки) принадлежат к одному биологическому виду. Понятно, что при работе с генетическим материалом мамонта выход уменьшится как минимум на порядок, а это значит, что потребуются многие сотни слоних в качестве суррогатных матерей. Поэтому, похоже, мы еще очень нескоро сможем увидеть живого мамонта.
Венец творения

Античные философы боготворили человека, доходя в своем почитании до откровенного антропоцентризма. «Человек есть мера всех вещей», – утверждал Протагор, живший в V веке до рождества Христова.
Христианство низвергло человека с этого пьедестала, однако оставило ему почетное второе место, ибо человек был сотворен по образу и подобию божьему. На заре эпохи Просвещения, когда наука теснила религию по всему фронту, споры о природе человека вспыхнули с новой силой. Одни мыслители усматривали в нем едва ли не венец творения, а другие занимали абсолютно противоположную точку зрения.
Сегодня эти дебаты представляют сугубо исторический интерес. В наши дни серьезные ученые не сомневаются в близком родстве Homo sapiens и высших приматов. Даже Ватиканский собор в конце концов признал, что теория Дарвина правильно толкует вопросы происхождения человеческого тела (о душе лучше не вспоминать) и мы многое унаследовали от общего предка, жившего семь или восемь миллионов лет назад.
Не стоит обольщаться: человек – животное весьма несовершенное, обремененное кучей врожденных генетических программ, работающих хаотично и вразнобой. На гребень успеха нас вынесли членораздельная речь и понятийное мышление, благодаря которым мы в значительной степени освободились от жесткого диктата естественного отбора, завоевали планету и выстроили современную цивилизацию. Однако неистребимая биология никуда не делась, и печать нашего животного происхождения все время дает о себе знать.
Но почему наши генетические программы так плохо подогнаны друг к другу? Дело в том, что любой биологический вид (и человек здесь вовсе не исключение) получает в наследство от предков полный набор разнообразных поведенческих программ. Инстинкт отнюдь не противоречит разуму. Рассудочная деятельность составляет как бы второй этаж поведения, она не игнорирует унаследованные программы, а плодотворно сотрудничает с ними. Если бы человек, как и все прочие животные, продолжал развиваться спокойно и неспешно, естественный отбор рано или поздно привел бы противоречивые программы в соответствие друг другу. Лишнее было бы убрано, что-то – подчищено, и на выходе получился бы стандартный биологический вид, идеально вписанный в среду.
Все испортил стремительный социальный прогресс. Речь позволила надежно фиксировать в длинном ряду поколений ценные навыки, и критерием успеха популяции отныне стали не унаследованные с генами полезные признаки, а внегенетически передаваемая информация. Неторопливый отбор оказался в плену у скоропалительных социальных перемен. Многочисленные врожденные программы заработали хаотично, и такая лихорадочная гонка в конце концов привела к тому, что проект Homo был выпущен в черновом, неотредактированном варианте.
Здесь не место подробно разбирать поведенческие программы нашего вида. Отметим только, что у нас очень плохо работают (а порой не работают вовсе) механизмы торможения внутривидовой агрессии, крайне запутанны и сложны программы полового поведения и многие другие врожденные регуляторы поведения. Вдобавок на определенном этапе своей истории человек разумный прошел через каннибализм, что нехарактерно для большинства млекопитающих. Кстати, и в наши дни некоторые архаические народы (скажем, новогвинейские папуасы) широко практикуют людоедство. Подчеркнем еще раз: в значительной степени тому виной скоропалительный социогенез, выдернувший человека из привычной среды обитания и сведший почти на нет влияние естественного отбора.
Настало время поговорить о нашей анатомии и физиологии. Так ли они безупречны, чтобы человек мог претендовать на титул венца творения?
Как известно, мы ходим на двух ногах, чем решительно отличаемся от большинства других животных. Еще сравнительно недавно прямохождение (бипедию) рода Homo увязывали с орудийной деятельностью: наш предок встал на две ноги, чтобы освободить руки для обработки камня. Однако этот аргумент можно отмести: ведь между вполне уверенным передвижением на двух ногах и появлением первых каменных орудий прошло как минимум семь миллионов лет. Совершенно очевидно, что мы получили бипедию по наследству. Но для чего она понадобилась нашим предкам, если об орудиях труда в ту далекую эпоху не могло быть и речи? Ведь природа ничего и никогда не делает с расчетом «на потом»; любое новшество немедленно подхватывается отбором только в том случае, если оно обеспечивает виду преимущества в борьбе за существование здесь и сейчас.
Хотя прямохождение не уникальное завоевание приматов и человека (на двух ногах, как известно, ходили мезозойские ящеры и до сих пор бегают кенгуру), все же оно встречается сравнительно редко, ибо наряду с явными преимуществами имеет массу недостатков, прежде всего анатомо-физиологических.

Мезозойские ящеры ходили на двух ногах
Вертикальное положение тела приводит к нарушениям гемодинамики и пищеварения, болям в спине, варикозному расширению вен нижних конечностей и множеству других специфических расстройств, от которых избавлены четвероногие. Двуногое существо резко теряет в скорости: из-за бипедии мы довольно медленно и неуклюже бегаем, и почти любое животное легко может нас догнать. Сколько-нибудь серьезная травма голеностопного сустава обрекала нашего далекого предка на неминуемую гибель – или от голода, или от нападения хищников.
Мы заметно уступаем физически своим двоюродным братьям – человекообразным обезьянам, даже тем из них, которые мельче или находятся в одной с нами весовой категории. Британская исследовательница Джейн Лавик-Гудолл, много лет изучавшая высших приматов в дикой природе, пишет, что взрослый самец шимпанзе гораздо сильнее четырех крепких мужчин.
По сравнению с другими млекопитающими, мы в разы чаще страдаем остеохондрозом и дегенеративными заболеваниями крупных суставов (в первую очередь тазобедреннего и коленного) – артрозами. Наконец, хождение на двух ногах чрезвычайно осложняет вынашивание плода и роды.
Биолог В.Р. Дольник пишет:
У четвероногих животных строение таза таково, что он одинаково хорошо приспособлен и для бега, и для родов. Чтобы голова плода легко проходила сквозь родовой канал между образующими таз костями, таз должен быть широким. У четвероногих широкий таз не препятствует бегу, и некоторые из них рожают очень крупных детенышей. У шимпанзе голова плода относительно большая, но и она проходит сквозь родовой канал, не делая ни одного поворота.
А вот у нашего прямоходящего предка – афарского австралопитека – таз очень узкий, поэтому его самки рожали детенышей с маленькой головой. Когда размер мозга начал увеличиваться, рожать детей стало намного труднее. Из этого тупика было два выхода: или расширить таз, или рожать в тот момент, когда голова плода еще не успела как следует вырасти.
Однако оба решения небезупречны. Широкий таз приведет к значительной потере в скорости, и самки будут отставать от самцов при длинных переходах и бегстве. Во втором случае придется производить на свет мелких недоношенных детенышей, которые будут в течение долгого времени нуждаться в уходе. Сначала природа двинулась как раз по последнему пути, но когда голова плода у неандертальца и человека разумного выросла еще больше, естественный отбор вплотную занялся реконструкцией женского таза, что немедленно отразилось на биомеханике доисторических женщин, и они стали ходить и бегать гораздо медленнее мужчин. А поскольку беспредельно расширять таз нельзя (плата за это слишком высока), роды стали сложным и опасным делом. У современной женщины голова плода с большим трудом протискивается через родовой канал, совершая при этом три поворота.
Можно привести еще много примеров несовершенства нашей телесной организации, но мы ограничимся только одним. Из-за быстрого роста черепа у места перехода глотки в пищевод образуется перегиб. Когда струя воздуха проходит через этот участок, здесь возникают турбулентные завихрения воздушного потока, и на стенке глотки оседает огромное количество частиц пыли и бактерий, которых в атмосферном воздухе всегда полным-полно. В результате зев стал входными воротами самых разнообразных инфекций. Эволюция решила устранить этот вопиющий непорядок, окружив «слабое звено» защитным кольцом из лимфатической ткани, но ее импровизация не увенчалась успехом, ибо лимфоидный конгломерат сделался излюбленным местом очаговой инфекции.
Разумеется, животные тоже не являются полным совершенством во всех отношениях. Стремление к идеалу – сугубо человеческая черта, а природу такие пустяки не занимают. С точки зрения эволюции, «идеальным» будет тот вид, который способен выжить и дать здоровое потомство. Но ведь мы-то хотим добиться гораздо большего! Строго говоря, медицина испокон веков только тем и занималась, что устраняла эволюционные промахи.
Чтобы улучшить качество жизни, мы создаем все более эффективные лекарственные препараты, изобретаем новые вакцины, пересаживаем органы и ткани. На очереди – «адресная» доставка лекарств непосредственно к очагу поражения. Сердечникам вшивают под кожу кардиостимуляторы, нормализующие ритм, а больным с артрозом меняют утратившие подвижность родные суставы на искусственные аналоги (так называемое эндопротезирование, ставшее в наши дни рутинной процедурой). Разработаны протезы, управляемые мышечными биотоками. Замена помутневшего хрусталика синтетическим – элементарная операция. Уже создана достаточно надежная модель искусственной сетчатки.
Манипуляции с генетическим материалом стали сегодня привычным делом, и трансгенные растения и животные – от банального помидора с геном морозоустойчивости северных рыб до обыкновенных буренок, молоко которых перенасыщено железом, – давно никого не удивляют. И даже генетическая модификация человека – факт почти уже состоявшийся. На этом пути открываются поистине ослепительные перспективы, сулящие победу над раком, окончательное искоренение наследственных хворей, почти неограниченное долголетие, а в очень далеком будущем – радикальную реконструкцию вида. А почему бы, в конце концов, и нет, если Homo sapiens – отнюдь не венец творения, а существо на редкость несовершенное даже анатомически?
Разумеется, всерьез о Homo novus (или даже Homo superior[55]) сегодня пока никто не говорит. Это только в романах братьев Стругацких прививка «бактерии жизни» на несколько порядков увеличивает сопротивляемость организма ко всем известным инфекциям, а стимуляция гипоталамуса особым микроволновым излучением позволяет легко переносить запредельные дозы жесткой радиации и чувствительные температурные перепады. Реальные достижения генных технологий куда скромнее.
Новые полезные свойства – это голубая мечта, а пока неплохо бы разобраться со старыми болячками, имеющими наследственную природу, – с гемофилией, некоторыми формами рака, старческими дегенеративными недугами вроде болезни Альцгеймера, врожденной неврологической патологией и так называемыми «большими» психозами – шизофренией, эпилепсией и маниакально-депрессивным психозом (МДП). Правда, не следует забывать о том, что унификация человечества путем исправления «неправильного» генотипа приведет к утрате изрядной доли генетического разнообразия, что может иметь самые непредсказуемые последствия.
Критерии оптимизации (или, другими словами, критерии улучшения человеческой породы) настолько тесно переплетены между собой, что взвесить бесчисленные «за» и «против» даже при дозированном и бережном вмешательстве будет непросто. Ведь идеального генотипа в природе не существует, и нередко явный сбой в одном звене соседствует с неким весьма полезным качеством в другом. Наследственная патология может оказаться своеобразной генетической платой за редкие способности и таланты. Как мы уже знаем, существует статистически достоверная связь между душевными болезнями и гениальностью. Так что вмешиваться в геном – святая святых человеческого организма – нужно крайне бережно.
Мы уже не говорим о евгенических программах улучшения человека – оптимизации таких, например, анатомо-физиологических параметров, как рост, пропорции тела, скорость реакции или даже интеллект. Конечно, весьма заманчиво, чтобы все люди появлялись на свет красивыми и умными. Но вопрос упирается в отсутствие надежных критериев. Что значит «красивый и умный»?
Когда специалисты улучшают породу коров, они точно знают, чего хотят: буренка должна давать как можно больше молока и мяса. А что такое улучшенный человек? Кроме того, здесь возникает множество щекотливых проблем этического свойства. Например, рост, бесспорно, запрограммирован генетически, но эти гены активно трудятся в детском и подростковом возрасте, а потом умолкают навсегда. Будить их у взрослого человека слишком опасно.
То же самое касается интеллекта и многих других психических феноменов: соответствующие гены работают в определенном временном интервале – с третьей недели внутриутробного развития и до шестисеми лет. Кто решится дать санкцию на вмешательство в организм маленького ребенка?
И все же реконструкция вида Homo sapiens – дело практически неизбежное. Ступив несколько тысяч лет тому назад на дорогу технологического развития, мы будем вынуждены пройти ее до конца. От примитивных механизмов античности до паровой машины прошло четыре тысячи лет, от паровой машины Уатта до двигателя внутреннего сгорания – чуть более двухсот, а от автомобиля Бенца до ядерного реактора – всего пятьдесят. В 1903 году неуклюжий аэроплан братьев Райт кое-как оторвался от земли и пролетел несколько сотен метров, а всего сорок лет спустя самолеты стали покрывать огромные расстояния. Одним словом, после промышленной революции XVIII века технологический рост только набирал обороты.
Уже сегодня биотехнологические достижения впечатляют настолько, что ученые всерьез толкуют о генетической терапии наследственных болезней и даже о создании искусственных микроорганизмов с заданными полезными свойствами, и нет никаких оснований считать, что только этим дело и ограничится. Рано или поздно неминуемо наступит эра управляемой автоэволюции – радикальной перестройки человеческого организма.
Конечно, преград на этом пути будет немало. Почти наверняка сначала против этого выступят самые разные общественные институты. Сопротивление примет жесточайшие формы, вплоть до уголовного преследования тех, кто вмешивается в геном. Однако, как показывает история науки, любое открытие, любой фундаментальный прорыв, любая новая технология в конечном счете непременно реализуются, какие бы потенциальные опасности они в себе ни таили.
Сегодня нас пугают непредсказуемые последствия генетических манипуляций, но происходит это оттого, что мы пока еще очень мало знаем о тонких механизмах функционирования клеточного генома. Однако жизнь не стоит на месте. Всего лишь сто пятьдесят лет назад человек даже не мечтал подняться в небо на аппарате тяжелее воздуха. А через сто лет на орбите уже кружил первый искусственный спутник Земли.
Маховик технического прогресса будет только набирать обороты. Пройдет совсем немного времени, и хитрая внутриклеточная машинерия, пугающая своей невообразимой сложностью, сделается простой и понятной. И устоит ли тогда наш потомок перед соблазном перекроить свое несовершенное тело?
Успехи генетики и молекулярной биологии порой ошеломляют, но мы пока еще не можем на равных состязаться с Природой. Однако это вовсе не означает, что ее нельзя превзойти. Эволюция – очень близорукий конструктор, она действует методом пошаговых изменений и не умеет заменять органы и системы целыми блоками, как это делает инженер. Поэтому в организмах людей и животных накопилась уйма всякого хлама – наследие миллионов лет неспешных изменений. Например, в основу системы кровообращения мог бы лечь принцип электромагнитного насоса. Тогда сердце стало бы электрическим органом, генерирующим меняющиеся поля, а эритроциты (клетки красной крови) превратились бы либо в диполи, либо в структуры, имеющие ферромагнитные включения. Нагрузка на стенку сосудов упала бы в разы – сейчас она вынуждена компенсировать перепады давления при сердечном выбросе за счет своих эластических свойств. Кроме того, легко и безболезненно решилась бы проблема питания самой сердечной мышцы. И хотя эволюция умеет создавать как дипольные молекулы, так и электрические органы, электромагнитный насос никогда не был реализован. Для этого пришлось бы затеять фундаментальную и глубокую перестройку сразу нескольких изолированных систем, а биологическая эволюция к таким фокусам, увы, не готова.
К тому же эволюция часто забывает о своих прошлых находках. Каждый раз ей приходится искать решение заново. Вот и получается, что удачные конструктивные находки разбросаны по боковым и крайне специализированным линиям. Скажем, орган кобры, реагирующий на инфракрасное излучение, обнаруживает температурную разницу порядка 0,001 °C, а электрический орган некоторых рыб реагирует на перепад напряжения около 0,01 микровольта на миллиметр. Глаз человека улавливает отдельные кванты света, осы и пчелы видят в ультрафиолетовом диапазоне, а обоняние некоторых насекомых находится на пороге приема молекулярных колебаний. Киты и дельфины освоили гидролокацию и умеют сравнительно долго обходиться без доступа воздуха – например, кашалоты задерживают дыхание на срок до двух с половиной часов, аккумулируя кислород в так называемых черных мышцах, насыщенных белком особого типа – миоглобином. Разве не соблазнительно взять на вооружение все эти эволюционные находки, беспорядочно рассованные по классам и отрядам? Модифицированный человек научится видеть в темноте и легко обходиться без воздуха, станет гораздо быстрее двигаться и соображать, а его иммунная система будет успешно гасить инфекционные хвори еще в зародыше.

Киты и дельфины умеют сравнительно долго обходиться без доступа воздуха
Пройдет совсем немного времени, и биотехнология, породнившаяся с информатикой, научится создавать искусственные разумные существа, ничем не отличающиеся от естественных, но значительно превосходящие их по целому ряду параметров. Возможно, именно так и выглядит магистральный путь эволюции материи во Вселенной: неживая материя – живая материя – естественные разумные существа – искусственные разумные существа.
Уже первые шаги в космосе показали, насколько человек укоренен в своей земной экологической нише и насколько он хрупок и непрочен за пределами земной атмосферы. Колонизация иных миров потребует реконструкции вида. А когда грань между искусственным и естественным сотрется окончательно, вполне можно ожидать появления высокоразвитых неантропоморфных форм жизни.
Словарь терминов

Аллели (аллеломорфы, аллельные гены) – разновидности одного и того же гена, расположенные в одинаковых участках парных хромосом и определяющие варианты развития одного и того же признака.
Антиген – любой чужеродный агент (паразит, бактерия, бактериальный токсин, вирус, пересаженная ткань, мутантная клетка собственного организма, например раковая и т. п.).
Антитела – высокоспецифические белки особого типа, принимающие участие в иммунных реакциях; синтезируются в ответ на проникновение в организм антигена.
Аппарат Гольджи (комплекс Гольджи) – система внутриклеточных полостей различной величины и формы, которая управляет ростом цитоплазматической мембраны и принимает участие в обмене белков и углеводов.
Бактериофаг (или просто фаг) – вирус, поражающий бактерии.
Биота – исторически сложившаяся совокупность животных, растений и микроорганизмов, объединенных общей областью распространения.
Вакуоли – внутриклеточные полости, служащие для регуляции давления и выведения наружу продуктов распада.
Вирион (вироспора) – полноценная вирусная частица до ее проникновения в клетку. На этой стадии вирус не обнаруживает никаких признаков жизнедеятельности.
Гамета – половая клетка.
Гаметогенез – процесс развития и формирования половых клеток (гамет).
Гаплоидная клетка – клетка с одинарным набором хромосом (половая клетка).
Ген – элементарная единица наследственной информации, отвечающая за формирование какого-либо признака. Морфологически и структурно представляет собой фрагмент молекулы ДНК.
Генеративная мутация – мутация, вмешивающаяся в генетический аппарат гамет; отражается на последующих поколениях.
Генная (точковая) мутация – мутация, затрагивающая отдельные гены.
Геном – совокупность генов, передаваемых от родительской особи к дочерней.
Геномная мутация – мутация, связанная с изменением числа хромосом.
Генотип – совокупность всех генов, локализованных в хромосомах данного организма. В более широком смысле – совокупность всех наследственных факторов организма.
Генотипическая изменчивость – изменения признаков и свойств организма, обусловленные изменениями наследственной информации (генотипа).
Гетерозиготный организм – организм, в наследственном наборе которого гомологичные хромосомы несут разные варианты (аллели) того или иного гена.
Гибрид – потомство, полученное в результате скрещивания двух генетически различающихся родительских форм.
Гомозиготный организм – организм, в наследственном наборе которого гомологичные хромосомы несут один и тот же вариант данного гена.
Гомологичные хромосомы – парные хромосомы в соматических клетках, отличающиеся высокой структурной идентичностью (даже если различаются между собой по нескольким генам). Одну хромосому ребенок получает от отца, а другую – от матери.
Дезоксирибонуклеиновая кислота (ДНК) – спиральная двухцепочечная макромолекула, построенная из азотистых оснований (нуклеотидов) и сахарофосфатного остова, который содержит углевод дезоксирибозу. Располагается в основном в клеточных ядрах и является носителем генетической информации.
Джанк – внегенные участки ДНК, никак не связанные ни с продукцией белков или ферментов, ни с регуляторной деятельностью функциональных наследственных структур.
Дигибридное скрещивание – скрещивание родительских форм, отличающихся по двум парам признаков.
Диплоидная клетка – клетка с двойным набором хромосом (соматическая клетка).
Доминантный ген – один из парных (аллельных) генов, который проявляется фенотипически как в гетеро-, так и в гомозиготном состоянии (то же самое относится и к доминантному признаку).
Дупликация – тип хромосомной мутации, при которой происходит удвоение участка хромосомы; играет существенную роль в наследственной патологии.
Зигота – оплодотворенное яйцо, возникшее в результате слияния мужской и женской половых клеток, то есть будущий зародыш.
Капсид – белковый чехол вирусной частицы, внутри которого содержится нуклеиновая кислота (вирусный геном).
Дата добавления: 2019-02-13; просмотров: 273; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
