ХИМИЧЕСКИЕ СВОЙСТВА КАРБОНОВЫХ КИСЛОТ.
КАРБОНОВЫЕ КИСЛОТЫ.
Карбоновыми кислотами называются производные углеводородов, в молекуле которых содержится одна или несколько карбоксильных групп

Общая формула предельных одноосновных карбоновых кислот: СnH2nO2
Классификация карбоновых кислот.
1. По числу карбоксильных групп:
- одноосновные (монокарбоновые)

- многоосновные (дикарбоновые, трикарбоновые и т.д.).
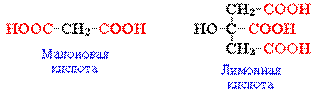
- По характеру углеводородного радикала:
- предельные CH3-CH2-CH2-COOH; бутановая кислота.
- непредельные CH2=CH-CH2-COOH; бутен-3-овая кислота.
- ароматические
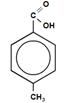 пара-метилбензойная кислота
пара-метилбензойная кислота
НАЗВАНИЯ КАРБОНОВЫХ КИСЛОТ.
| Название | Формула кислоты | ||
| кислоты | её соли и (эфиры) | ||
| муравьиная | метановая | формиат | HCOOH |
| уксусная | этановая | ацетат | CH3COOH |
| пропионовая | пропановая | пропионат | CH3CH2COOH |
| масляная | бутановая | бутират | CH3(CH2)2COOH |
| валериановая | пентановая | валерат | CH3(CH2)3COOH |
| капроновая | гексановая | гексанат | CH3(CH2)4COOH |
| пальмитиновая | гексадекановая | пальмитат | С15Н31СООН |
| стеариновая | октадекановая | стеарат | С17Н35СООН |
| акриловая | пропеновая | акрилат | CH2=CH–COOH |
| олеиновая | цис-9-октадеценовая | олеат | СН3(СН2)7СН=СН(СН2)7СООН |
| бензойная | бензойная | бензоат | C6H5 -COOH |
| щавелевая | этандиовая | оксалат | НООС - COOH |
ИЗОМЕРИЯ КАРБОНОВЫХ КИСЛОТ.
1. Изомерия углеродной цепи. Начинается с бутановой кислоты (С3Н7СООН), которая существует в виде двух изомеров: масляной (бутановой) и изомасляной (2-метилпропановой) кислот.
|
|
|
2. Изомерия положения кратной связи в непредельных кислотах, например:
СН2=СН—СН2—СООН СН3—СН=СН—СООН
Бутен-3-овая кислота Бутен-2-овая кислота
(винилуксусная кислота) (кротоновая кислота)
3. Цис -, транс-изомерия в непредельных кислотах, например:

4. Межклассовая изомерия: Карбоновые кислоты изомерны сложным эфирам:
Уксусная кислота СН3-СООН и метилформиат Н-СООСН3
5. Изомерия положения функциональных групп у гетерофункционалъных кислот.
Например, существуют три изомера хлормасляной кислоты: 2-хлорбутановая, 3-хлорбутановая и 4-хлорбутановая.
СТРОЕНИЕ КАРБОКСИЛЬНОЙ ГРУППЫ.
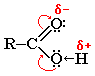 Карбоксильная группа сочетает в себе две функциональные группы – карбонил и гидроксил, взаимно влияющие друг на друга
Карбоксильная группа сочетает в себе две функциональные группы – карбонил и гидроксил, взаимно влияющие друг на друга
Кислотные свойства карбоновых кислот обусловлены смещением электронной плотности к карбонильному кислороду и вызванной этим дополнительной (по сравнению со спиртами) поляризацией связи О–Н.
В водном растворе карбоновые кислоты диссоциируют на ионы:

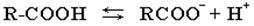
Растворимость в воде и высокие температуры кипения кислот обусловлены образованием межмолекулярных водородных связей. С увеличением молекулярной массы растворимость кислот в воде уменьшается.
|
|
|
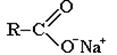
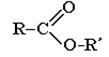
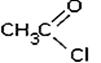
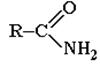
ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ – в них гидроксогруппа замещена на некоторые другие группы. Все они при гидролизе образуют карбоновые кислоты.
| Соли | Сложные эфиры | Галогенангидриды | Ангидриды | Амиды. |
| 
| 
| 
| 
|
ПОЛУЧЕНИЕ КАРБОНОВЫХ КИСЛОТ.
| 1. Окисление спиртов в жестких условиях – раствором перманганата или дихромата калия в кислой среде при нагревании. | 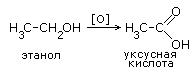
|
| 2.Окисление альдегидов: раствором перманганата или дихромата калия в кислой среде при нагревании, реакцией серебряного зеркала, гидроксидом меди при нагревании. | 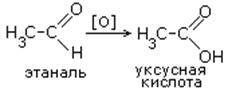
|
| 3. Щелочной гидролиз трихлоридов: | R-CCl3 + 3NaOH à [R-C(OH)3] + 3NaCl неустойчивое вещество [R-C(OH)3] à RCOOH + H2O |
| 4. Гидролиз сложных эфиров. | R-COOR1 + KOH à RCOOK + R1OH RCOOK + HCl à R-COOH + KCl |
| 5. Гидролиз нитрилов, ангидридов, солей. | 1)нитрил: R-CN + 2H2O –(H+)à RCOOH 2)ангидрид: (R-COO)2O + H2O à 2RCOOH 3)натриевая соль: R-COONa+HClàR-COOH + NaCl |
| 6. Взаимодействие реактива Гриньяра с СО2: | R-MgBr + CO2 à R-COO-MgBr R-COO-MgBr -(+H2O)à R-COOH +Mg(OH)Br |
| 7. Муравьиную кислоту получают нагреванием оксида углерода (II) с гидроксидом натрия под давлением: | NaOH + CO (200oC,p)à HCOONa 2HCOONa+ H2SO4à2HCOOH + Na2SO4 |
| 8. Уксусную кислоту получают каталитическим окислением бутана: | 2C4H10 + 5O2 à 4CH3-COOH + 2H2O |
| 9. Для получения бензойной кислоты можно использовать окисление монозамещенных гомологов бензола кислым раствором перманганата калия: | 5C6H5–CH3+6KMnO4+9H2SO4à5C6H5-COOH+3K2SO4 + MnSO4 + 14H2O |
ХИМИЧЕСКИЕ СВОЙСТВА КАРБОНОВЫХ КИСЛОТ.
Дата добавления: 2019-02-13; просмотров: 344; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
