Семинар №4 Структура реальных кристаллов.
Семинар №1 Основы теории кристаллизации. Рост реальных растворов. Задача 1 Дано: гомогенная кристаллизация материала GaSb переохлаждение ΔT = 70K поверхностное натяжение σтв-ж = 1,6·10-5Дж/см2 температура плавления Тпл = 998 К плотность ρ = 5,614 г/см3 постоянная Авогадро NА = 6,02·1023 ат/моль теплота плавления ΔН = 65,15 кДж/моль Найти: r* – критический размер зародыша П – число атомов в зародыше РЕШЕНИЕ: GL – GS = HL – TSL – HS + TSS = (HL – HS) – T(SL – SS) = ΔHпл – TΔSпл = ΔHпл – (T ΔHпл/Tпл) = ΔHпл(1 – (T/Tпл) = ΔHпл(ΔT/Tпл) – ΔGоб = ΔHпл(ΔT/Tпл) Молярная масса МGaSb = 191,4 г/моль ΔGгом = (V/Ω)(GS – GL) + σ·S V – Объем зародыша S – Площадь зародыша ΔGоб = (GS – GL) – объемная свободная энергия Куб a = 2r V1/3 = 2r; k = 6 число сторон V2/3 = 4r2 Ω = M/ρ – мольный объем S = kV2/3 Дифференцируем: V*1/3 = – (2/3)(kσΩ/ΔGоб) Получаем для кубического зародыша со стороной 2r* и сферического с радиусом r* Объем сферического зародыша Объем кубического зародыша ; V*СФ = 4/3π(2,4·10-7)3см3 = 5,79·10-20см3 V*КУБ = θr3 = θ(2,4·10-7)3 = 1,1·10-19 см3 Число атомов в 1 см3: N=(ρ·NA)/M = (5,6г/см3·6,02·1023 ат/моль)/191,4 г/моль = 1,76·1022 ат/см3 Число атомов в зародыше: n = V*N nСФ = 5,79·10-20см3 · 1,76·1022ат/см3 = 1019 ат. nКУБ = 1,1·10-19см3 · 1,76·1022ат/см3 = 1936 ат. Задача 2 Дано: Материал GaAs Молекулярная масса М = 144,6 г/моль Энтальпия плавления ΔН = 108 кДж/моль Температура плавления Т = 1553 К Плосность ρ = 5,3 г/см3 Дано: (1) Сферический зародыш Критический объем V* = 1·106 эл. ячеек Параметр решетки a = 0,565 нм σ = 2,1·10-5 Дж/см2 Найти: Поверхностное натяжение Критическое переохлаждение ΔTгом Дано: (2) Гетерогенное зарождение Кубический зародыш V* = 1·106 эл. ячеек Угол смачивания Θ = 120° Найти: Критическое переохлаждение ΔTгет Дано: (3) Гетерогенное зарождение Переохлаждение ΔT = ΔTгом = 4,7 К 2-х мерный зародыш 3-х мерный зародыш Найти: Критический размер зародыша r* (1) Vяч = a3 = (0,565·10-7см)3= = 1,8·1022см3/яч V* = 1·106 эл.яч·Vяч = 1·106 эл.яч·1,8· ·10-22см3/яч=1,8·10-16 см3 ; (2) Возьмем сферический зародыш Гомогенная Гетерогенная Возьмем кубический зародыш ; ; Sгет = 24r2Ф; ; ; Sгет = 24(Vгет/8Ф)2/3; Ф = 24·(1,8·10-16/(8Ф))2/3·0,656 = 1,66·10-10 см2 (3) Рассмотрим 3-х мерный зародыш (Vгет/Vгом) = Ф r*гет = r*гом V*гет = V*гом r*гет ≠ r*гом r*~(1/ΔT) r*гет > r*гом ΔTгет < ΔTгом (2/3)S*гет σ = -(V*гет/Ω)·ΔGоб (2/3)·24r2Фσ = (8r3/ Ω) ·Ф· (ΔHпл ΔTгет/Tпл) После сокращения получим: ΔTгет = ΔTгом = 4,7 К Критический объем при гетерогенном зарождении для зародыша кубической формы: V*КУБ = 8r*3Ф = 8·(3,5·10-6)3·0,656 = 2,25 · 10-16 см3 Критический объем при гетерогенном зарождении для зародыша сферической формы: ; ; Рассмотрим 2-х мерный зародыш. ΔGГом = (V2/3/Ω)·ΔGоб + 4·V1/3σ (V*-1/3/Ω) · (2/3)·ΔGоб + (1/3)·V*-2/3·4σ = d(ΔG)/dV (2/3)·(ΔGоб/Ω) = – (4/3)·V*-1/3σ | ·V*2/3 (2/3)·(V*2/3/Ω)·ΔGоб = – (4/3)·V*1/3σ (V*2/3/Ω)·ΔGоб = – 2·V*1/3σ kV*2/3 = S V1/3 =2r = a V2/3 = a2 = 4r2 l* = 4a = 8r 4·V*1/3σ – 2·V*1/3σ = 2·V*1/3σ = ΔG*гом = 2aσ = 4rσ = 0,5·l*σ = ΔG*гом – энергия образования 2-х мерных зародышей Следовательно: (1/2) · l*σ = (V*2/3/Ω) · ΔGоб Гетерогенное зарождение =1,7·10-6 см r*гом = r*гет (S*гет/S*гом) = Ф S*гом = 4r*2 = 4 · (1,7·10-6)2 = 1,16·10-11 см2 S*гет = S*гом · Ф = 1,16 · 10-11 · 0,656 = 7,58 · 10-12 см2 Задача 3 Дано: Материал GaAs Направленная кристаллизация Осевые температурные градиенты В расплаве: (dT/dx)ж = 30 K/см В кристалле: (dT/dx)тв = 20 K/см Энтальпия плавления ΔHпл = 108кД/моль Плотность кристалла ρ = 5,3 г/см3 Теплопроводность кристалла εтв = 0,37 кал/см·с·К в расплаве: εж = 146 Вт/м·К M = 144,6 г/моль Найти: Скорость роста кристалла V 1 кал = 4,18 Дж εтв = 0,37 · 4,18 = 1,55 Дж/(см·с·К) εж = 1,46 Дж/(см·с·К) εтв(dT/dx)тв – εж(dT/dx)ж = ρLV L – Теплота плавления отнесенная к единице массы L = – ΔHпл/M = – 108·103 Дж/моль / 144,6 г/моль = –746,9 Дж/г V – Скорость роста кристалла Семинар №2 Распределение примеси в процессах кристаллизации Задача 1 Распределение примеси в полупроводниковых материалах на основе модельных представлений термодинамических растворов, используя для жидкой и твердой фаз приближение: а) идеальных растворов б) регулярных растворов Материал: Ge Примесь: Bi Температура Т = 805° С = 1123 К Концентрация примеси в жидкой фазе XжBi = 0,10 ат. доли Температура плавления ТBiпл = 544 К Энтальпия плавления ΔHBiпл = 11014 Дж/моль Параметры взаимодействия в твердой фазе Ge – Bi ωтв = 23,29 ккал/моль = = 97,42 кДж/моль Газовая постоянная R = 8,31 Дж/моль·К Для температуры Т = 900° С = 1173 К XжBi = 0,08 ат. доли Найти: Равновесный коэффициент распределения К0 Химический потенциал: μ0тв = μ0ж μ0тв + RTlnaAтв = μ0ж + RTlnaAж a = γ · X a – активность γ – коэффициент активности Х – концентрация RTlnaAтв – RTlnaAж = μ0ж – μ0тв – чистый компонент А Примем за стандартный потенциал при ТBiпл ΔHАпл = Т ΔSАпл = RTlnaAтв – RTlnaAж = RTlnγтвXAтв – RTlnγтвXAж ΔHАпл – ТΔSАпл = RTln XAтв + RTlnγAтв – RTln ХAж = RTln(XAтв/ ХAж) + RTlnγAтв – RTln ХAж K0 = XAтв/ ХAж ΔHАпл – ТΔSАпл = RTln K0 + ωтв·(1 – ХАтв)2 – ωж·(1 – ХАж)2 – для регулярных растворов а) Идеальные растворы: γAж = γAтв = 1 ΔHАпл – ТΔSАпл = RTln K0 ΔHАпл – Т(ΔHАпл/Tпл)= RTln K0 K0 = 0,28 а) Регулярные растворы: γAж ≠ γAтв ≠ 1 Для нахождения ωж возьмем исходные данные для температуры близкой к заданной и примем для этого температурного интервала К0 = const XAтв = ХAж · K0 ΔSпл = ΔHпл/Tпл T1 = 1123 K Х1ж = 0,10 ат.доли T1 = 1173 K Х1ж = 0,08 ат.доли Подбираем К0, при котором ω1ж = ω2ж ω1ж = a1ln K0 + b1·(1– 0,1·K0)2 + C1 ω1 ж = ω2 ж ω2ж = a2ln K0 + b2·(1– 0,08·K0)2 + C2 (a1 – a2)ln K0 = b2·(1– 0,08·K0)2 – b1·(1-0,1·K0)2 +(C1 – C2) (11521,15 – 11516,6)ln K0 = 115099,2·(1-0,08 K0)2 – 120271,6·(1– 0,1·K0)2 + (14472,4 – 15046) 4,55·ln K0 – 573,6 = 115099,2 – 2·115099,2·0,08·K0 + 115099·0,082·K02 – 120271,6 + + 120271,6·2·0,1·K0 – 120271,6·0,12·K02 = – 5172,4 + 5638,45·K0 – 466,08·K02 4,55·ln K0 + 4598,8 = 5638,45·K0 – 466,08·K02 левая часть правая часть K0 = (0÷1) Левая часть уравнения Правая часть уравнения Δ = левая часть – правая часть 0,5 4595,65 2702,70 1892,94 0,9 4598,32 4697,08 – 98,759 0,8 4598,32 4212,47 385,85 0,85 4598,32 4455,94 142,38 0,87 4598,32 4552,67 45,64 0,88 4598,32 4600,90 – 2,58 0,879 4598,32 4596,08 2,23 0,8795 4598,32 4598,49 – 0,174 K0 = 0,8795 ω1ж = 113039,2 Дж/моль ω2ж = 113039,49 Дж/моль Задача 2 Выращивание легированного кристалла по методу Чохральского Скорость вытягивания fmin = 2 см/час fmax = 20 см/час Угловая скорость вращения кристалла ωmin = 10 об/мин = 62,8 рад/мин ωmax = 40 об/мин = 251,3 рад/мин Коэффициент диффузии примеси D = 1·10-5 см2/с Кинематическая вязкость расплава ν = 2,5·10-3 см2/с Равновесный коэффициент распределения K0 = 1·10-2 Оценить пределы изменения эффективного коэффициента распределения Кэф Толщина диффузионного приграничного слоя δ = 1,6·D1/3·ν1/6·ω-1/2 ωmin = 62,8 рад/мин δmax = 1,6·(1·10-5)1/3·(2,5·10-3)1/6·(62,8/60)-1/2 = 0,0124 см ωmax = 251,3 рад/ мин δmin = 1,6·(1·10-5)1/3·(2,5·10-3)1/6·(251,3/60)-1/2 = 0,0062 см fmax = 20 = Для ωmin: Для ωmax: fmax = 2 = Для ωmin: Для ωmax: fmax ωmin 0,908 Кэф ωmax 0,240 fmin ωmin 0,019 ωmax 0,014 ΔHпл(Ge) = 34320 Дж/моль Tпл = 1210 К Задача 3 Дано: Материал: Ge Примесь: Bi Температура плавления Энтальпия плавления жидкий раствор – идеальный твердый раствор – регулярный B – примесь ликвидус А – основа T 0,280 1200 2,13·10-4 0,050 1190 1,80·10-4 0,057 1185 1,68·10-4 0,10 1175 1,56·10-4 0,13 1160 1,37·10-4 0,15 1150 1,21·10-4 0,17 1145 1,11·10-4 020 1130 9,35·10-5 0,25 1115 7,13·10-5 0,30 1110 7,10·10-5 0,33 1080 4,42·10-5 Семинар №3 Легирование полупроводников Задача 1 Дано: Выращивание полупроводника методом Чохральского Скорость вращения кристалла: ω = 25 об/мин = 157,08 рад/мин Скорость вытягивания: f = 11 см/час = Коэффициент диффузии примеси: D = 1·10-5 см2/с Кинематическая вязкость расплава: ν = 1,35·10-3 см2/с Материал: Ge Фоновая примесь: In Содержание в шихте: ПIn = 1·1016 ат/см3 Легирующая примесь: As Требуемая концентрация носителей в монокристалле n-типа: Пn = 5·1016 см-3 Равновесный коэффициент распределения: Ge – As K0 = 2·10-2 Ge – In K0 = 6·10-5 Масса расплава: mж = 2000 г Плотность Ge: ρж = 5,571 г/см3 Найти: навеска легирующей примеси, введенной в расплаве mAs Толщина пограничного диффузионного слоя в расплаве у фронта кристаллизации δ = 1,6·D1/3·ν1/6·ω-1/2 Эффективный коэффициент распределения: Kэф для Ge – In: Kэф для Ge – As: Количество фоновой примеси, которое перешло в монокристалл из расплава. Содержание In в шихте равно содержанию в расплаве. Количество носителей заряда в кристалле n-типа зависит от компенсации акцепторной фоновой примеси (In) однородной легирующей примесью (As). Пn = ND – NA ; Количество легирующей примеси в расплаве на 1 см3: Объем расплава: Количество легирующей примеси в расплаве объемом Vж [см3]: Масса легирующей примеси в расплаве (навеска): Получаем формулу: M(As) =74,92 г/моль – молекулярная масса примеси NАв = 6,022·1023 ат/моль – число Авогадро Задача 2 Дано: Выращивание монокристалла методом Чохральского Условия проведения процесса (см. зад. 1) Легирующая примесь As вводится в расплав в виде лигатуры из монокристаллического Ge. Материал: Ge Удельное сопротивление лигатуры: ρл = 4·10-3 Ом·см Подвижность носителей заряда в лигатуре: μл = 700 Масса расплава: mж = 2000 г Требуемая концентрация носителей в монокристалле n-типа: Пn = 5·1016 см-3 Найти: Массу вводимой лигатуры Млиг – удельная проводимость лигатуры – концентрация носителей в лигатуре Расплав содержит полупроводниковый материал Ge + лигатура ( монокристалл Ge + As) Количество примеси в расплаве: (1) – объем лигатуры, см3 – объем расплава, см3 – концентрация примеси в лигатуре, ат/см3 (2) – плотн. лигатуры (Ge) (3) – плотность расплава (Ge) = (4) – концентрация примеси в кристалле – количество доноров в кристалле Концентрация примеси в лигатуре: (5) С учетом формул (2 – 5) формула (1)примет вид: ; e = 1,6·10-19Кл – заряд носителей (электрона) Задача №3 Выращивание кристалла методом Чохральского Материал: Ge Донорная примесь: As Акцепторная примесь: In Положение p – n – перехода соответствует доле закристаллизовавшегося расплава: g = 0,1 Эффективный коэффициент распределения (Ge – As): KЭФ(Ge – As) = 0,15 Эффективный коэффициент распределения KЭФ(Ge – In) = 5,22·10-4 Определить отношение концентраций донорной и акцепторной примесей, введенной в расплав Сдон/Сакц Распределение донорной примеси As по монокристаллу Распределение акцепторной примеси In по монокристаллу На границе p – n – перехода: Для g = 0 < 0,1 Для g = 0,3 > 0,1 n–тип p–тип Задача 4 Дано: получение однородно легированного кристалла методом Чохральского Заданный уровень легирования: Ств = 5·1019 ат/см3 Однордно легированной считать часть монокристалла, в пределах которой разброс концентраций не превышает ±20% от заданного уровня δдоп. = ±20% Расчет провести для: Найти: выход однородно легированного монокристалла G 1-ый случай Kmax = K = 0,908 Распределение концентрации примеси по длине кристалла: (1) (2) (3) Разброс концентраций: Необходимо найти g соответствующее концентрации примеси в кристалле Подставляем Сmax в уравнение (3): ; g = 0,988 Выход однородно легированного монокристалла Если бы весь кристалл был однородно легирован на заданном уровне , то количество примеси перешедшей в кристалл равно: – начальный объем расплава – объем закристаллизовавшегося расплава В реальности мы имеем количество примеси в однородно легированной части кристалла объемом : (108%) 2-ой случай Kmin=K=0,014 Находим g соответствующей концентрации примеси Ств = Сmax 7,5·1019 = 5·1019·(1-g)0,014-1; g = 0,338 (50%)
|
|
|
|
|
|
|
|
|
|
|
|
Семинар №4 Структура реальных кристаллов.
Задача №1
 |
Дано:
Материал GaSb
Температура плавления
Тпл=985 К
Равновесная концентрация
Вакансий в п/решетке Sb
При Т=Тпл
Nv(1)=1,13*1011 см-3
При T=g Tпл
g = 0,70

Найти:
Концентрацию избыточных
вакансий при T= 0,7 Тпл
в монокристалле, полученном
кристаллизацией из расплава.
Решение:
Изменение термодинамического потенциала монокристалла при возникновении n вакансий в результате повышения температуры.
ΔG = ΔGреал – Gид = ΔH – TΔS
ΔG, ΔGид – термодинамич. потенциал реального и идеального кристалла соотв.
ΔH = n ΔHv
ΔHv – прирост энтальпии кристалла за счет образования одной вакансии.
ΔS = ΔSсм + ΔSкол
ΔSсм, ΔSкол – изменение энтропии смещения и колебания соотв.
ΔSсм = k ln( W’/W)
W’,W – вероятность состояний при наличии и отсутствии вакансий соответственно в идеальном кристалле W = 1
Пусть кристалл содержит Ns (в каждом из которых при 0 К находится атом). Далее, при образовании n вакансий общее число узлов (состояний)
равно (N + n )
ΔSсм = k ln W’ = k ln 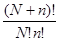 = - k ( N ln
= - k ( N ln 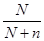 + n ln
+ n ln 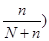 ;
;
ΔSкол = n ΔSv
ΔSv – изменение колебательной энтропии при введении в кристалл 1 вакансии.
ΔG = n(ΔHv – TΔS) + kT ( n ln 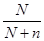 + n ln
+ n ln 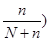
Абсолютная величина ΔHv положительна, так же как ΔSv , но | ΔSкол | < | ΔHv | в 6-8 раз. Можно пренебречь ролью ΔSv . Если учесь, что энтропия смешения (конфигурационная) уменьшается с ростом n, а энтальпия увеличивается. Так же как n << N ln 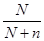 .
.
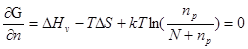
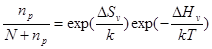
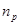 + N = Ns ,ΔSv - пренебрегаем
+ N = Ns ,ΔSv - пренебрегаем
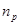 = Ns exp (
= Ns exp ( 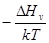 ) равновесная концентрация вакансий при температуре Т
) равновесная концентрация вакансий при температуре Т
Находим  с помощью
с помощью 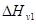 и
и 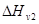 .
.
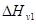 =
= 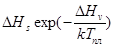 ;
; 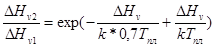 ;
;
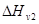 =
= 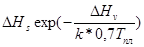 ;
; 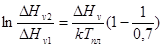
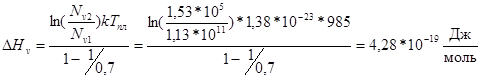
k – константа Больцмана.
R – универсальная газовая постоянная 8,31 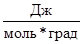
NA – число Авогадро ( 6*1023 ат/моль)
Зная 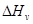 и
и 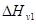 (или
(или 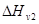 ) можно найти равновестную концентрацию вакансий при любой
) можно найти равновестную концентрацию вакансий при любой
температуре T = gTпл 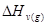 . В нашем случае расчет
. В нашем случае расчет 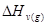 не требуется, так как g = 0,7.
не требуется, так как g = 0,7.
Избыточная концентрация вакансий возникает при быстром охлаждении м/кристалла от температуры Т=Тпл до Т=gТ, когда концентрация вакансий не успевает прийти к равновесному значению. Чтобы концентрации вакансий была равновесной при каждой температуре необходимо бесконечно медленное охлаждение от Т=Тпл .
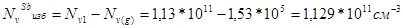
Избыточные вакансии приводят к образованию дивакансий и дислокаций.
Задача №2
Дано:
выращивание м/кристалла методом Чохральского.
Материал GaSb
Плоский фронт кристаллизации
Осевой температурный градиент в области пластической деформации dT/dZ = 80 град/см.
Температура плавления Тпл = 985 К.
Охлаждение монокристалла от Тпл до T=0,7 Тпл
Все избыточные вакансии равномерно поглощаются дислокациями.
Равновесная концентрация вакансий в п/решетке Sb
при Т=Тпл
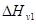 = 1,13*1011 см-3;
= 1,13*1011 см-3;
при T=g Тпл
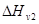 = 1,53*105 см-3;
= 1,53*105 см-3;
Равновесная концентрация вакансий в п/решетке Ga
при Т=Тпл
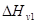 = 3,21*1012 см-3;
= 3,21*1012 см-3;
при T=g Тпл
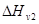 = 2,64*107 см-3;
= 2,64*107 см-3;
g = 0,7
Все дислокации краевые, ось дислокации совпадает с направлением 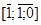 , а вектор Бюргерса с [1;1;0], т.е. перпендикулярен оси.
, а вектор Бюргерса с [1;1;0], т.е. перпендикулярен оси.
Плоскость скольжения (001)
Период решетки GaSb a=0,609593 нм = 0,609593*10-7 см.
Коэффициент линейного расширения 

Найти:
1) Плотность дислокаций в монокристалле, выращенном методом Чохральского.
2) Расстояние на которое переползет дислокация при охлаждении монокристалла от Т=Тпл до Т=0,7Тпл
Решение:
Источниками дислокаций могут быть термические напряжения в кристалле. В монокристаллах термические напряжения вызваны наличием осевых и радиальных температурных градиентов. В монокристалле с плоским фронтом кристаллизации радиальной градиент (dT/dR) → 0.
Приближенно плотность дислокаций, вызванная термическим напряжением равна

b – вектор Бюргерса ( модуль)
b = 
a – период решетки;
x , y , z – кристаллические индексы направления вектора Бюргерса, n – целое число.
В алмазной решетке min энергии обладает дислокация с вектором Бюргерса ½ <110>
Модуль вектора Бюргерса:
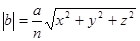
Для алмазной решетки полная дислокация с символом 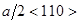 имеет длину
имеет длину
|b| = 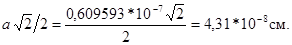
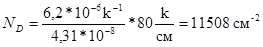
При охлаждении кристалла, образующиеся избыточные вакансии поглощаются дислокациями, что вызывает их переползание. Необходимо оценить концентрацию избыточных вакансий в обоих подрешетках.
В п/решетке Ga

В п/решетке Ga

Общее количество вакансий в кристалле:
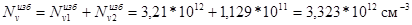
Дислокации движутся по плоскостям наименее густо засеянными атомами (100)
Следовательно
 ,
,
где l – расстояние (в см) на которое перепеползет дислокация.
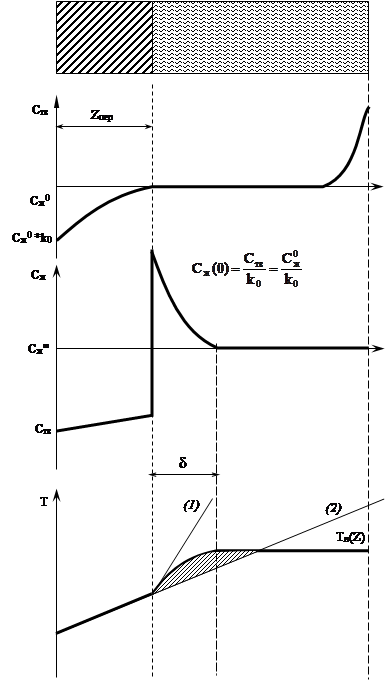
 Задача №3
Задача №3
Дано:
направленная кристаллизация
Материал Ge
Примесь Bi
Концентрация примеси
|
Ств = const.
Коэф. диффузии
примеси в жидкой фазе
D= 1*10-5 см2/с
Скорость кристаллизации
f = 100 мм/час = 10/3600 см/час.
Температура
|
Концентрация примеси в расплаве
Сж (0) = 0,10 ат.доли
Газовая постоянная
R=8,31 Дж/моль*К
Энтальпия плавления примеси
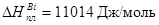

Найти:
величину температурного градиента
в расплаве, исключающего явление
концентрационного переохлаждения
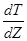
 |
Дифференциальное уравнение молекулярной диффузии в расплаве:
 ; t – время
; t – время
Рассмотрим стационарный процесс
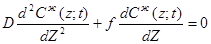 (1)
(1)
В стационарных условиях ( Zпер – расстояние, которое необходимо пройти ф.к. до наступления стационарного состояния) :

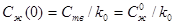
Решая уравнение (1) получим
 (2);
(2);
Уравнение (2) описывает распределение примести в расплаве у фронта кристаллизации.
Область кристаллизации определяется соотношением градиентов температуры в расплаве 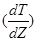 и температуры ликвидуса
и температуры ликвидуса 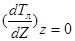
 обусловлен накоплением примеси в расплаве у ф.к. Расплав с повешенной концентрацией примеси в соответствии с диаграммой фазовых равновесий
обусловлен накоплением примеси в расплаве у ф.к. Расплав с повешенной концентрацией примеси в соответствии с диаграммой фазовых равновесий
( при k0 < 1) будет кристаллизоваться при более высокой температуре.
 , т.е.
, т.е. 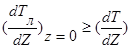 , получим неустойчивый ф.к. (
, получим неустойчивый ф.к. (  )
)
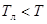 , т.е.
, т.е. 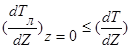 , получим устойчивый ф.к. (
, получим устойчивый ф.к. ( 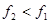 ).
).
При неустойчивом фронте кристаллизации наблюдается явление концентрационного переохлаждения (заштрихованная область)
 |
 (3)
(3)
Зависимость температуры от концентрации примеси в расплаве
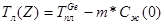 (4)
(4)
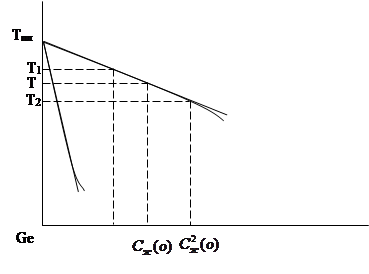
|
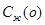 из ур (2), m – наклон ликвидуса.
из ур (2), m – наклон ликвидуса.
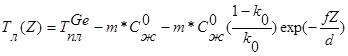
Дифференцируем
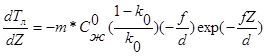
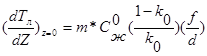
Для предотвращения концентрационного переохлаждения:

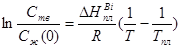 (4)
(4)
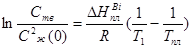 (5)
(5)
(4) – (5)
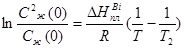
Нахождение линии наклона ликвидуса:
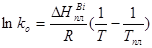
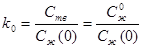
Из выражения (4) вычитаем (5):

Пусть кристаллизуется чистый компонент Ge, Ств (Bi) стремится к нулю. Приближенно Ств = const.
Температуру T1 возьмем равной Т + 5K, T2 = T - 5K;
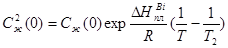

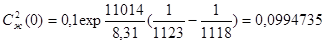
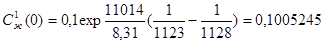
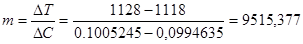 ; k0 = 0.28 ( в приближении идеального раствора)
; k0 = 0.28 ( в приближении идеального раствора)
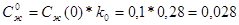
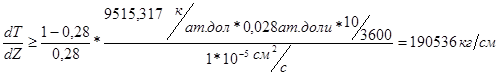
Дата добавления: 2018-09-22; просмотров: 176; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!

