Характеристика и особенности простых белков, их функции, примеры: гистоны, протамины, аутеллины, проламины, альбумины, глобулины.
Коллаген, эластин, кератины.
Характеристика сложных белков: строение, представители, функции. Хромопротеиды, металлопротеиды, нуклеопротеиды, гликопротеиды, липопротеиды. Привести конкретные примеры.
Белки – это высокомолекулярные азотсодержащие органические вещества, состоящие из аминокислот, соединённых в цепи с помощью пептидных связей и имеющих сложную структурную организацию. Белки составляют 25% сырой ткани и 45-50% сухой ткани.
Биологическая роль белков:
1. каталитическая (выполняют ферменты);
2. структурная, т.е. белки являются основным компонентом клеточных структур;
3. регуляторная (выполняют белки-гормоны);
4. рецепторная, т.е. рецепторы клеточных мембран имеют белковую природу;
5. транспортная – белки участвуют в транспорте липидов, токсических веществ, кислорода и т.д.;
6. опорная выполняет белок коллаген; эластин ит.д.
7. энергетическая. Заключается в том, что при окислении 1г белка выделяется 17,6 кДж (4,1ккал) энергии;
8. сократительная – её выполняют белки актин и миозин;
9. генно-регуляторная – её выполняют белки гистоны, участвуя в регуляции репликации;
10. имуннологическая – её выполняют белки антитела;
11. гемостатическая – участвуют в свёртывании крови, препятствуют кровотечению;
12. антитоксическая, т.е. белки связывают многие токсические вещества (особенно соли тяжёлых металлов) и препятствуют развитию интоксикации в организме.
|
|
|
Защитные системы высших организмов формируются защитными белками, к к-рым относятся иммуноглобулины (ответственны за иммунитет), белки комплемента(ответственны за лизис чужеродных клеток и активацию иммунологич. ф-ции), белки системы свертывания крови (см., напр., Тромбин, Фибрин) и противовирусный белок интерферон.
Принципы классификации белков. Простые и сложные белки. Фосфопротеины и металлопротеины, их роль в клетке.
В состав многих белков помимо пептидных цепей входят и неаминокислотные фрагменты, по этому критерию белки делят на две большие группы — простые и сложные белки (протеиды). Простые белки содержат только аминокислотные цепи, сложные белки содержат также неаминокислотные фрагменты. Эти фрагменты в составе сложных белков называются «простетическими группами». В зависимости от химической природы простетических групп среди сложных белков выделяют следующие классы:
Гликопротеиды, содержащие в качестве простетической группы связанные углеводные остатки и протеогликаны, с мукополисахаридными простетическими группами. Большая часть внеклеточных белков, иммуноглобулины — гликопротеиды. Протеогликаны являются основным компонентом межклеточного матрикса. Ig и гиалуроновая кислота – гликопротеины.
|
|
|

Липопротеиды, содержащие в качестве простетической части связанные липиды. Липопротеиды выполняют функцию транспорта липидов, гормоны стероидной природы. ЛПВП, ЛПНП, ЛПОНП
Металлопротеиды, содержащие негемовые координационно связанные ионы металлов. Среди металлопротеидов есть белки, выполняющие депонирующие и транспортные функции (ферритин и трансферрин) и ферменты (карбоангидраза и различные супероксиддисмутазы) Как правило, металлопротеины - ферменты.
Нуклеопротеиды, содержащие нековалентно связанные ДНК или РНК. Составные части клеточных ядер. Нуклеопротеиды являются важнейшей составной частью вирусов. НАДН, ФАДН (флавинадениндинуклеотид)
Фосфопротеиды, содержащие ковалентно связанные остатки фосфорной кислоты. В образовании сложноэфирной связи с фосфатом участвуют гидроксильные группы серина или треонина, фосфопротеинами являются казеин молока. Большое количество их содержится в ЦНС. Многие важные ферменты клетки активны только в фосфорилированной форме. Фосфопротеины являются источником энергетического и пластического материала.
Хромопротеиды. К ним относится множество белков с металлсодержащей порфириновой простетической группой, выполняющие разнообразные функции — гемопротеины, хлорофиллы; флавопротеиды с флавиновой группой, и др.
|
|
|
Принципы классификации белков. Характеристика простых белков.
1 .По функции выделяют:
1. Транспортные белки (гемоглобин )
2. Каталитические (ферменты),
3. Регуляторные (гормоны).
4. Структурные (белки соединительной ткани, мембранные белки).
5. Защитные (антитела).
6. Сократительные (актин, миозин).
7. Рецепторные участвуют в образовании рецепторов.
Простые белки по растворимости в воде и солевых растворах условно подразделяются на: протамины, гистоны, альбумины, глобулины, проламины, глютелины.
Простые белки по растворимости и пространственному строению разделяют на глобулярные и фибриллярные. Глобулярные белки отличаются шарообразной формой молекулы, растворимы в воде. К этой группе относятся все ферменты и БАВ.
Среди глобулярных белков можно выделить:
альбумины — растворимы в воде в широком интервале рН ( 4 -8,5), осаждаются 70-100% раствором сульфата аммония;
полифункциональные глобулины с большей молекулярной массой, труднее растворимы в воде, растворимы в солевых растворах, часто содержат углеводную часть;
|
|
|
гистоны — низкомолекулярные белки с высоким содержанием в молекуле остатков аргинина и лизина, что обусловливает их основные свойства;
протамины отличаются еще более высоким содержанием аргинина (до 85 %), как и гистоны, образуют устойчивые ассоциаты с нуклеиновыми кислотами, выступают как регуляторные и репрессорные белки — составная часть нуклеопротеинов;
проламины характеризуются высоким содержанием глутаминовой кислоты (30-45 %) и пролина (до 15 %), нерастворимы в воде, растворяются в 50-90 % этаноле;
глутелины содержат около 45 % глутаминовой кислоты, как и проламины, чаще содержатся в белках злаков.
Фибриллярные белки характеризуются волокнистой структурой, практически нерастворимы в воде и солевых растворах. Полипептидные цепи в молекулах расположены параллельно одна другой. Участвуют в образовании структурных элементов соединительной ткани (коллагены, кератины, эластины). Эти белки отличаются высокой механической прочностью. Они выполняют главным образом структурные функции: входят в состав сухожилий и связок (коллаген, эластин), образуют волокна шелка и паутины (фиброин), волосы, ногти, перья (кератин).
4. Структурная организация белков: характеристики первичной, вторичной, третичной и четвертичной структур.
Принято выделять четыре уровня структурной организации белковой молекулы: первичная, вторичная, третичная и четвертичная структура.
Первичной структурой белка называют последовательность чередования аминокислот в полипептидной цепи. Эту структуру формируют пептидные связи между α-амино- и α-карбоксильными группами аминокислот.
Процесс сворачивания полипептидной цепи в правильную трёхмерную структуру получил название фолдинг.
Вторичная структура белка представляет собой способ свёртывания полипептидной цепи в спиральную или иную конформацию. При этом образуются водородные связи между СО-и NH-группами пептидного остова одной цепи или смежных полипептидных цепей. Известно несколько типов вторичной структуры пептидных цепей, среди которых главными являются α-спираль и β-складчатый слой.
α-Спираль - жёсткая структура, имеет вид стержня. Внутреннюю часть этого стержня создаёт туго закрученный пептидный остов, радикалы аминокислот направлены наружу. При этом СО-группа каждого аминокислотного остатка взаимодействует с NH-группой четвёртого от него остатка. На один виток спирали приходится 3,6 аминокислотных остатка, а шаг спирали составляет 0,54 нм .
 Рисунок 2.1. α-Спираль.
β-Складчатый слой отличается от α-спирали тем, что имеет плоскую, а не стержневидную форму. Образуется при помощи водородных связей в пределах одной или нескольких полипептидных цепей.
Рисунок 2.1. α-Спираль.
β-Складчатый слой отличается от α-спирали тем, что имеет плоскую, а не стержневидную форму. Образуется при помощи водородных связей в пределах одной или нескольких полипептидных цепей.  Рисунок 2.2. β-Складчатый слой.
Тип вторичной структуры белка определяется его первичной структурой. Например, в месте расположения остатка пролина (атомы пирролидинового кольца в пролине лежат в одной плоскости) пептидная цепь делает изгиб, и водородные связи между аминокислотами не образуются. Поэтому белки с высоким содержанием пролина (например, коллаген) не способны образовывать а-спираль. Радикалы аминокислот, несущие электрический заряд, также препятствуют спирализации.
Третичная структура белка (глобула) - это распределение в пространстве всех атомов белковой молекулы, или иначе говоря, пространственная упаковка спирализованной полипептидной цепи. Основную роль в образовании третичной структуры белка играют водородные, ионные, гидрофобные и дисульфидные связи, которые образуются в результате взаимодействия между радикалами аминокислот.
Водородные связи образуются между двумя полярными незаряженными радикалами или между незаряженным и заряженным радикалами, например, радикалами серина и глутамина:
Рисунок 2.2. β-Складчатый слой.
Тип вторичной структуры белка определяется его первичной структурой. Например, в месте расположения остатка пролина (атомы пирролидинового кольца в пролине лежат в одной плоскости) пептидная цепь делает изгиб, и водородные связи между аминокислотами не образуются. Поэтому белки с высоким содержанием пролина (например, коллаген) не способны образовывать а-спираль. Радикалы аминокислот, несущие электрический заряд, также препятствуют спирализации.
Третичная структура белка (глобула) - это распределение в пространстве всех атомов белковой молекулы, или иначе говоря, пространственная упаковка спирализованной полипептидной цепи. Основную роль в образовании третичной структуры белка играют водородные, ионные, гидрофобные и дисульфидные связи, которые образуются в результате взаимодействия между радикалами аминокислот.
Водородные связи образуются между двумя полярными незаряженными радикалами или между незаряженным и заряженным радикалами, например, радикалами серина и глутамина:
 Ионные связи могут возникать между противоположно заряженными радикалами например, радикалами глутамата и аргинина:
Ионные связи могут возникать между противоположно заряженными радикалами например, радикалами глутамата и аргинина:
 Гидрофобные взаимодействия характерны для неполярных радикалов, например, валина и лейцина:
Гидрофобные взаимодействия характерны для неполярных радикалов, например, валина и лейцина:
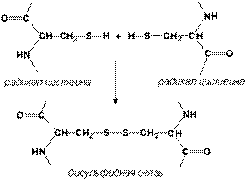
 Дисульфидные связи образуются между SH-группами двух радикалов цистеина, находящихся в разных участках полипептидной цепи: .
Дисульфидные связи образуются между SH-группами двух радикалов цистеина, находящихся в разных участках полипептидной цепи: .
 По форме молекулы и особенностям формирования третичной структуры белки делят на глобулярные и фибриллярные.
Четвертичная структура белка – (комплекс глобул) размещение в пространстве взаимодействующих между собой субъединиц, образованных отдельными полипептидными цепями белка. Четвертичная структура - высший уровень организации белковой молекулы, к тому же необязательный - более половины известных белков её не имеют. Белки, обладающие четвертичной структурой, называют также олигомерными белками, а полипептидные цепи, входящие в их состав, - субъединицами или протомерами. В некоторых белках такие субъединицы одинаковы или имеют сходное строение, а другие белки состоят из субъединиц с цепями разных типов.
Олигомерные белки могут существовать в виде нескольких устойчивых конформаций и обладают аллостерическими свойствами, то есть способны переходить из одной конформаций в другую с изменением своей функциональной активности. Примерами олигомерных белков могут служить эритроцитарный белок гемоглобин, и многие другие.
По форме молекулы и особенностям формирования третичной структуры белки делят на глобулярные и фибриллярные.
Четвертичная структура белка – (комплекс глобул) размещение в пространстве взаимодействующих между собой субъединиц, образованных отдельными полипептидными цепями белка. Четвертичная структура - высший уровень организации белковой молекулы, к тому же необязательный - более половины известных белков её не имеют. Белки, обладающие четвертичной структурой, называют также олигомерными белками, а полипептидные цепи, входящие в их состав, - субъединицами или протомерами. В некоторых белках такие субъединицы одинаковы или имеют сходное строение, а другие белки состоят из субъединиц с цепями разных типов.
Олигомерные белки могут существовать в виде нескольких устойчивых конформаций и обладают аллостерическими свойствами, то есть способны переходить из одной конформаций в другую с изменением своей функциональной активности. Примерами олигомерных белков могут служить эритроцитарный белок гемоглобин, и многие другие.
|
Дата добавления: 2018-08-06; просмотров: 1631; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
