На электродах протекают реакции 15 страница
Наряду с адсорбцией идет процесс десорбции:
Vдес. = kдес. × а. (13.23)
При равновесии Vaдc = Vдес или
kaдc × P × (am – a) = kдес. × а. (13.24)
Обозначим kдес./ kадс. = b, а а/аm = Q, где Q – относительное заполнение поверхности, получим:
 или
или  . (13.25)
. (13.25)
Это уравнение изотермы адсорбции называется уравнением Ленгмюра. Константа b носит название константы адсорбционного равновесия, или адсорбционного коэффициента.
Константа равновесия связана со стандартными изменениями энергии Гиббса. Если
RTlnb = –DGo, так как DGo = DHo + TDSo,
то
 . (13.26)
. (13.26)
Следовательно
 . (13.27)
. (13.27)
Таким образом, адсорбционный коэффициент b связан со стантартной энтропией DS° и со стандартной теплотой адсорбции q = –DH°.
Очень часто аm называют «емкость монослоя». На рис.13.3 показана кривая, выражающая изотерму адсорбции по Ленгмюру

Рис. 13.3. Изотерма адсорбции по Ленгмюру
При очень малых заполнениях и, следовательно, очень малых давлениях Р в знаменателе, согласно (13.25), bр<< 1. Поэтому в этой области а = аmbp, т.е. переходит в уравнение Генри. При очень высоких давлениях bp >> 1 и а = аm, т.е. величина адсорбции перестает зависеть от давления, поскольку все центры уже заняты.
Для расчета параметров am и b уравнение Ленгмюра представляют в виде
 . (13.28)
. (13.28)
Тангенс угла наклона этой линии равен 1/amb, а отрезок, отсекаемый на оси ординат, равен 1/am.
Уравнение Ленгмюра, полученное на основании модели локализованной адсорбции газов на поверхности твердого тела, часто хорошо описывает адсорбцию растворенных веществ на поверхности жидкости (поверхность раздела раствор/газ), при которой адсорбция не локализована, так как молекулы подвижны и образуют двумерную газо- или жидкообразную пленку.
Обусловлено это тем, что основные положения модели Ленгмюра соблюдаются при адсорбции из растворов: поверхность жидкости идеально однородна, взаимодействие адсорбированных молекул в адсорбционном слое мало отличается от их взаимодействия в растворе. Оно к тому же ослаблено за счет взаимодействия молекул растворенного вещества с молекулами растворителя и практически не влияет на адсорбцию.
Уравнение Ленгмюра связано с уравнением состояния адсорбционной пленки – уравнением Гиббса. Так,
 ,
,
а по уравнению Ленгмюра
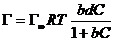 ;
;
тогда

или
 . (13.29)
. (13.29)
После интегрирования в пределах от sо до s и от 0 до С получим:
 ,
,
и, наконец,
 , (13.30)
, (13.30)
где Г¥ связано с площадью, занимаемой 1 моль адсорбированного вещества в мономолекулярном слое, следующим соотношением:  .
.
Основные напрвления исследований и задачи коллоидной химии Классификация коллоидных систем по кинетическим свойствам дисперсной фазы, по размеру частиц дисперсной фазы, по агрегатному состоянию дисперсной фазы и дисперсной среды Коллоидные растворы и их основные свойства Оптические свойства коллоидных растворов. Уравнение Рэллея и условия его применения. Основные положения теории Ми. Голубизна неба, красный закат как отражение оптических свойств коллоидных систем.
Дата добавления: 2018-02-28; просмотров: 403; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
